微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在硫酸的工业制法中,下列生产操作与说明的原因二者都正确的是
A.硫铁矿燃烧前需将矿粒粉碎,这样易于向沸腾炉中投料
B.炉气进入接触室之前需要净化、干燥,因为炉气中的杂质易与SO2反应
C.SO2氧化为SO3时需使用催化剂,这样可提高SO2的转化率
D.接触室的反应温度控制在400~500 ℃,因为在该温度范围内催化剂的活性较高
参考答案:D
本题解析:硫铁矿燃烧前需将矿粒粉碎,增大反应物的接触面积,反应速率加快,A不正确;炉气进入接触室之前需要净化、干燥的目的是防止催化剂中毒,B不正确;催化剂只能改变反应速率,但不能改变平衡状态,C不正确,所以正确的答案选D。
点评:该题是常识性知识的考查,主要是考查学生灵活运用基础知识解决生活以及生产中实际问题的能力,有利于激发学生的学习兴趣和学习求知欲,也有助于培养学生的逻辑思维能力和发散思维能力。
本题难度:一般
2、选择题 下列工业生产的有关说法正确的是
A.石油的分馏和干馏都是复杂的物理变化和化学变化
B.工业上生产酒精,可以用发酵法和乙烯水化法
C.工业生产聚氯乙烯的反应原理是利用缩聚反应
D.石油裂解气能使溴水褪色,但不能使酸性高锰酸钾褪色
参考答案:B
本题解析:略
本题难度:一般
3、填空题 (8分)2,4,5-三氯苯酚和氯乙酸反应可制造除草剂2,4,5-三氯苯氧乙酸。某生产该除草剂的工厂曾在一次事故中泄漏出有毒的二NF749英,简称TCDD。有关物质的结构式如下:
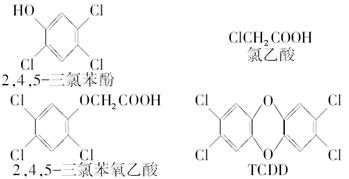
请写出:
(1)生成2,4,5-三氯苯氧乙酸的化学方程式: _________________________
(2)由2,4,5-三氯苯酚生成TCDD的化学方程式:_________________________
参考答案:(1)
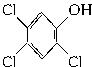 +ClCH2COOH→
+ClCH2COOH→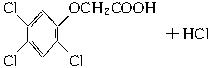
(2)
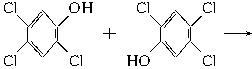
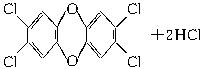
本题解析:本题旨在考查获取信息、处理信息的能力和有机反应的书写技能。由两种生成物的结构可知均需在2,4,5三氯苯酚、氯乙酸等原料的基础上通过去HCl,得到产物。如将TCDD对称地“一分为二”复原,即可找到反应方程式。?
本题难度:简单
4、填空题 减少SO2的排放、回收利用SO2成为世界性的研究课题。我国研究人员研制的利用低品位软锰矿浆(主要成分是MnO2)吸收废渣高温焙烧产生的SO2,制备硫酸锰的生产流程如下:
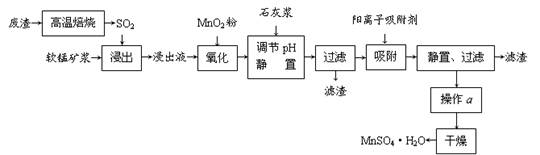
浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子。
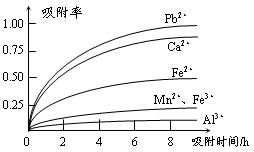
有关金属离子的半径以及形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见下图。
离子
| 离子半径(pm)
| 开始沉淀时的pH
| 完全沉淀时的pH
|
Fe2+
| 74
| 7.6
| 9.7
|
Fe3+
| 64
| 2.7
| 3.7
|
Al3+
| 50
| 3.8
| 4.7
|
Mn2+
| 80
| 8.3
| 9.8
|
Pb2+
| 121
| 8.0
| 8.8
|
Ca2+
| 99
| -
| -
|
?
已知PbO2的氧化性大于MnO2。请回答下列问题:
⑴ 写出浸出过程中主要反应的化学方程式?,氧化过程中主要反应的离子方程式?。
⑵ 在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至?。
⑶ 阳离子吸附剂用于除去杂质金属离子。决定阳离子吸附剂吸附效果的因素是?(填写序号)。
a.溶液的pH?b.金属离子的电荷?c.金属离子的半径?d.吸附时间
⑷ 操作a包括?等过程。
参考答案:
⑴ SO2+MnO2=MnSO4?2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O
⑵ 4.7~8.3
⑶ b c d
⑷ 蒸发浓缩结晶
本题解析:
本题以制备硫酸锰的生产流程为知识载体,考查化学反应的书写,及除杂中的问题。(1)从流程图看,浸出过程是软锰矿浆(MnO2)与SO2的反应。杂质离子中只有Fe2+具有还原性,可以被MnO2在酸性条件下氧化成Fe3+。(2)杂质中含有Fe2+、Al3+、Ca2+、Pb2+四种阳离子,由沉淀的pH范围知,Fe2+的沉淀与Mn2+离子的沉淀所需的pH接近,而Fe3+则相差很远,故可以将Fe2+氧化成Fe3+而除杂。从吸附率的图可以看出,Ca2+、Pb2+的吸附率较高,故只要调节pH值在4.7~8.3间,大于4.7可以将Fe3+和Al3+除去,小于8.3是防止Mn2+也沉淀。(3)结合半径,分析右图知,图中离子从上至下,半径有减小趋势,对应的吸附率减小。随着时间的递增,所有离子的吸附率均增大;另Fe3+和Al3+离子所带电荷数大,其吸附率低。(4)由于制取的MnSO4・H2O含有结晶水,故采用蒸发浓缩结晶的方法。
本题难度:一般
5、填空题 (14分)青铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)?冶炼铜的反应为
8CuFeS2 + 21O2 8Cu + 4FeO + 2Fe2O3 + 16SO2
若CuFeS2中Fe的化合价为+2,反应中被还原的元素是_________(填元素符号)。
(2)?上述冶炼过程产生大量SO2,下列处理方案中合理的是__________(填代号)。
a.?高空排放? b.用于制备硫酸
c.?用纯碱溶液吸收制Na2SO4? d.用浓硫酸吸收
(3)?过二硫酸钾(K2S2O8)具有强氧化性,可将I?氧化为I2:S2O82? + 2I? → 2SO42? + I2;通过改变反应途径,Fe3+、Fe2+均可催化上述反应,试用离子方程式表示Fe3+对上述反应催化的过程:__________、__________。
(4)?利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3,方法为:
①用稀盐酸浸取炉渣,过滤;②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
a.?除去Al3+ 的离子方程式是____________________________;
b.?选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸?稀硫酸? KSCN溶液? KMnO4溶液? NaOH溶液?碘水
所选试剂为__________,证明炉渣中含有FeO的实验现象为____________________。
参考答案:(1)? Cu、O? 2分? (2)? b、c? 2分
(3)?①2Fe3+ + 2I? → I2 + 2Fe2+?2分?②2Fe2+ + S2O82? → 2Fe3+ + 2SO42?2分
(4) a.? Al3+ + 4OH? → AlO2? + 2H2O?2分
b.?稀硫酸、KMnO4溶液?2分
用稀硫酸浸取炉渣,所得溶液与酸性KMnO4溶液反应,若溶液褪色则证明存在?2分
本题解析:(1)根据方程式可知,氧气是氧化剂,得到电子,因此被还原的元素是氧元素。CuFeS2中铜元素的化合价是+2价,而生成物中有单质铜生成,所以被还原的元素还有铜。
(2)SO2是一种酸性氧化物,能用于制备硫酸,b正确。SO2还是一种大气污染物,不能随意丢弃,a不正确,c正确。浓硫酸不能稀释SO2,d不正确,答案选bc。
(3)铁离子能把碘离子氧化生成单质碘,而在一定条件下,而S2O82?又能把亚铁离子氧化生成铁离子,方程式为2Fe3+ + 2I? → I2 + 2Fe2+、2Fe2+ + S2O82? → 2Fe3+ + 2SO42?。
(4)①由于氢氧化铝是两性氢氧化物,能溶于氢氧化钠中,所以方程式为Al3+ + 4OH?= AlO2? + 2H2O。
②因为氧化亚铁具有还原性,而酸性高锰酸钾溶液又具有氧化性,亚铁离子能使酸性高锰酸钾溶液褪色,据此可以检验,所以选择的试剂是稀硫酸、KMnO4溶液。实验现象是用稀硫酸浸取炉渣,所得溶液与酸性KMnO4溶液反应,若溶液褪色则证明存在。
本题难度:一般