微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 工业上合成NH3除了需要N2外,一定还需要
A.H2
B.O2
C.CO2
D.CO
参考答案:A
本题解析:根据氨气的组成可知,还需要氢气。答案是A。
本题难度:简单
2、选择题 化学工业在经济发展中的作用举足轻重。下列有关工业生产的叙述中,正确的是? (? )
A.硫酸生产中常采用高压条件来提高SO2的转化率
B.合成氨中采用及时分离液态氨来提高反应速率
C.电解精炼铜中,溶液中c(Cu2+)基本保持不变
D.氯碱工业中阳极得到氢氧化钠和氢气
参考答案:C
本题解析:2SO2+O2 2SO3,该反应在常压下转化率非常高,不需要采用高压来提高转化率;N2+3H2
2SO3,该反应在常压下转化率非常高,不需要采用高压来提高转化率;N2+3H2 2NH3,由于NH3液化后使混合气体中c(NH3)降低,引起v(正),v(逆)均降低;电解精炼铜时,阳极反应式为Cu-2e-=Cu2+,阴极反应式为Cu2++2e-=Cu,所以溶液中c(Cu2+)基本保持不变;
2NH3,由于NH3液化后使混合气体中c(NH3)降低,引起v(正),v(逆)均降低;电解精炼铜时,阳极反应式为Cu-2e-=Cu2+,阴极反应式为Cu2++2e-=Cu,所以溶液中c(Cu2+)基本保持不变;
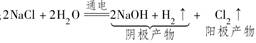 ?D错误。
?D错误。
本题难度:一般
3、选择题 化学与科学、技术、社会、环境密切相关,下列说法中正确的是
[? ]
A.绿色化学的核心是应用化学原理对环境污染进行治理
B.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
C.泄露在美国墨西哥湾海洋中的大量原油能被海洋生物迅速分解,不会导致生态灾难?
D.电镀废液中含浓度较高的含氮化合物,经中和后可直接用于浇灌农作物
参考答案:B
本题解析:
本题难度:简单
4、选择题 用接触法制5t98%的浓硫酸,在理论上需要含FeS2 70%(杂质不含硫元素)的硫铁矿为(?)
A.86t
B.8.6t
C.4.3t
D.43t
参考答案:C
本题解析:略
本题难度:一般
5、填空题 (15分)【化学---化学与技术】
某工业废水中含有CN-和Cr2O72-等离子,需经污水处理达标后才能排放,污水处理厂拟用下列流程进行处理:
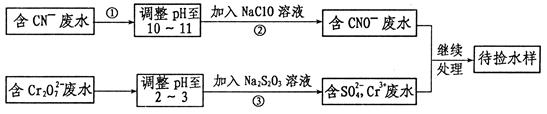
回答下列问题:
(1)上述处理废水流程中主要采用的方法是?。
(2)流程②中,反应后无气体放出,该反应的离子方程式为?。
(3)含Cr3+废水需进一步处理,请你设计一个处理方案:?
(4)反应③中,每消耗0.4 mol Cr2O72-转移2.4 mol e-,该反应离子方程式为:?。
(5)取少量待测水样于试管中,加入NaOH溶液观察到有蓝色沉淀生成,继续加至不再产生蓝色沉淀为止,再向溶液中加入足量Na2S溶液,蓝色沉淀转化成黑色沉淀,解释产生该现象的原因:?。
参考答案:(1)氧化―还原法(2分)?(2)CN-+ClO-?CNO-+Cl-(3分)
(3)调节废水pH,使其转化成Cr(OH)3沉淀除去(4分,其他合理答案也给分)
(4)3S2O32-+4Cr2O72-+26H+?6SO42-+8Cr3++13H2O(3分)
(5)Cu2++2OH-?Cu(OH)2↓ 、 Cu(OH)2(s)+S2-(aq)?CuS(s)+2OH-(aq)
或Ksp(CuS)<Ksp[Cu(OH)2],使沉淀向更难溶方向转化。(3分)
本题解析:(1)次氯酸或Cr2O72-都具有氧化性,所以处理废水都方法都是氧化―还原法。
(2)反应后无气体放出,说明次氯酸钠都还原产物是氯化钠,而不 是氯气,所以该反应的离子方程式为CN-+ClO-?CNO-+Cl-。
(3)处理废水中的Cr3+,可以通过沉淀法,即调节废水pH,使其转化成Cr(OH)3沉淀除去。
(4)每消耗0.4 mol Cr2O72-转移2.4 mol e-,说明反应中转移6个电子,因此其还原产物是Cr3+。由于氧化产物是SO42-,所以方程式为3S2O32-+4Cr2O72-+26H+?6SO42-+8Cr3++13H2O。
(5)蓝色沉淀是氢氧化铜,由于硫化铜的溶解度小于氢氧化铜的,所以根据沉淀转化的实质向更难溶方向转化,所以反应中生成硫化铜黑色沉淀。有关方程式为Cu2++2OH-?Cu(OH)2↓ 、 Cu(OH)2(s)+S2-(aq)?CuS(s)+2OH-(aq)。
本题难度:一般