微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 设NA为阿伏加德罗常数,下列说法正确的是
[? ]
A.电解精炼铜过程中,电路中每通过NA个电子,阳极溶解铜32g
B.11 2 mol/L的NH4Cl溶液中含NH4+数目为2NA
C.5.6g铁粉与硝酸反应失去的电子数一定为0.3NA
D.1 mol C20H42的分子中含有的共价键数目为61NA
参考答案:D
本题解析:
本题难度:简单
2、选择题 设NA为阿伏加德罗常数,下列叙述正确的是( )
A.11.2L氯气所含的分子数为0.5NA
B.2.4gMg与足量的盐酸反应失去的电子数为0.2NA
C.32g氧气中所含的氧原子数为NA
D.18g水中所含的电子数为8NA
参考答案:A、温度压强不知,11.2L氯气物质的量不是0.5mol;故A错误;
B、2.4gMg物质的量为0.1mol,每个镁原子最外层2个电子,与足量的盐酸反应失去的电子数为0.2NA,故B正确;
C、32g氧气物质的量为1mol,分子中所含的氧原子数为2NA,故C错误;
D、18g水物质的量为1mol,分子中所含的电子数为10NA,故D错误;
故选B.
本题解析:
本题难度:一般
3、选择题 设NA为阿伏加德罗常数的数值,则下列说法正确的是( )
A.2.24LCl2中含有的原子数一定为0.2×6.02×1023
B.在标准状态下,11.2L?NO与11.2L?O2混合后气体分子数为0.75NA
C.常温常压下,足量的Fe在1molCl2中充分燃烧,转移的电子数为2NA
D.106gNa2CO3固体中的阴离子数大于NA
参考答案:A、无温度和压强,2.24LCl2物质的量不一定是0.1mol;含有的原子数不一定为0.2×6.02×1023,故A错误;
B、在标准状态下,11.2L?NO物质的量为0.5mol,11.2L?O2物质的量为0.5mol,发生反应2NO+O2=2NO2;0.5mol一氧化氮反应生成二氧化氮0.5mol,剩余氧气0.25ml,由于二氧化氮和四氧化二氮存在化学平衡分子物质的量减少,最后气体分子数小于0.75NA,故B错误;
C、足量的Fe在1molCl2中充分燃烧,反应的电子转移可以以反应的氯气计算,转移的电子数为2NA,故C正确;
D、106gNa2CO3固体物质的量为1mol,固体中含阴离子1mol,故D错误;
故选C.
本题解析:
本题难度:一般
4、选择题 设NA为阿伏加德罗常数,下列说法中正确的是( )
A.1NA个氢气分子所占的体积为22.4L
B.2NA个二氧化碳分子的质量为44g
C.1000mL0.1mol/L的NaCl溶液中,Na+与Cl-离子总数为0.2N
D.17g氨气中所含原子数为NA
参考答案:A、1NA个氢气分子的物质的量为1mol,若处于标准状况,氢气体积约是22.4L,但氢气所处的状态不一定是标准状况,所以氢气体积可能是22.4L,也可能不是22.4L,故A错误;
B、2NA个二氧化碳分子的物质的量为2mol,其质量为2mol×44g/mol=88g,故B错误;
C、0.1mol/L的NaCl溶液中Na+与Cl-离子的浓度都是0.1mol/L,离子的总浓度为0.2mol/L,所以该溶液中含有的Na+与Cl-离子总数为1L×0.2mol/L×NAmol-1=0.2NA,故C正确;
D、17g氨气的物质的量为17g17g/mol=1mol,每个氨气分子含有4个原子,所以含有的原子数为1mol×4×NAmol-1=4NA,故D错误.
故选:C.
本题解析:
本题难度:一般
5、选择题 若设NA=1mol×6.02×1023mol-1,下列叙述中正确的是( )
A.将162.5gFeCl3转化为氢氧化铁胶体后,氢氧化铁胶体粒子数等于NA
B.标准状况下,22.4LCCl4中碳原子的个数约为NA
C.含有NA个氖原子的氖气在标准状况下的体积约为11.2L
D.标准状况下,用NaOH溶液吸收氯气22.4L,反应中转移的电子数目为NA
参考答案:A.胶体粒子是由多个“分子”组成的集合体,将162.5gFeCl3转化为氢氧化铁胶体后,氢氧化铁胶体粒子数小于NA,故A错误;
B.标准状况下CCl4为液体,无法计算22.4LCCl4的物质的量,故B错误;
C.氖气为单原子分子,含有NA个氖原子的氖气在标准状况下的体积约为22.4L,故C错误;
D.n(Cl2)=1mol,与NaOH反应的电子转移的方向和数目为
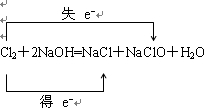
,反应中转移的电子数目为NA,故D正确.
故选D.
本题解析:
本题难度:一般