��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���л�ѧ����ʽ�У����������ӷ���ʽH++OH-��H2O��ʾ����
[? ]
A. 2NaOH + H2SO4 = NaSO4+2H2O
B. Ba��OH��2 +2 HCl = BaCl2+2H2O
C. Ba��OH��2 + H2SO4 = BaSO4��+2H2O
D. KOH+ HNO3 = KNO3+H2O
�ο��𰸣�C
���������
�����Ѷȣ���
2��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�����
A������ͨ���������������Һ�У� Cl2 + 2OH-��Cl- + ClO- + H2O
B��������ϡ���ᷴӦ��2Fe��6H+��2Fe3+��3H2��
C������������Һ��ϡ���ᷴӦ��Ba2+��SO42-��BaSO4��
D�����Ȼ�������Һ��ͨ��������Cl2��Fe2+��Fe3+��2Cl-
�ο��𰸣�A
���������A����ȷ
B������Ϊ�������ӣ�Fe��2H+��Fe2+��H2��
C�����ֲμӷ�Ӧ������δд����Ba2+�� 2OH-��2H++SO42-��BaSO4��+ 2H2O
D����ɲ��غ㣺Cl2��2Fe2+��2Fe3+��2Cl-
��ΪA
�����Ѷȣ���
3��ѡ���� �������ӷ���ʽ��д��ȷ����
A����NaHCO3��Һ�м���������Ba(OH)2��Һ
2HCO3- + Ba2+ + 2OH- = BaCO3�� + CO32- + 2H2O
B����ʯ��ʯ�еμ�ϡ����
CaCO3 + 2H+ = Ca2+ + CO2�� + H2O
C���ö��Ե缫���KOH��Һʱ�����缫��Ӧ
2H2O �C 4e- = O2 + 4H+
D��NaOH��Һ��ͨ�������������壺2OH- + H2S = S2 - + 2H2O
�ο��𰸣�BD
���������
��ȷ�𰸣�BD
A��HCO3- + Ba2+ +OH- = BaCO3��+H2O
B����ȷ��
C������ȷ�������õ��ӣ�2H2O��2e-=2OH�D��H2��
D����ȷ��
�����Ѷȣ���
4��ѡ���� ���з���ʽ����ȷ����
A��ʯ������Ca(OH)2�ĵ��룺Ca(OH)2(s) Ca2�� + 2OH��
Ca2�� + 2OH��
B����AgC1����Һ�еμ�Na2S��Һ������ɫ������2AgC1(s) + S2���� Ag2S(s) + 2C1��
C����NaHCO3��Һ�м��������ʯ��ˮ������ɫ������HCO3�� + Ca2�� + OH�� �� CaCO3��+ H2O
D��Fe (OH)3������Ʊ���FeCl3+ 3H2O 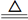 Fe (OH)3�����壩+3HCl
Fe (OH)3�����壩+3HCl
�ο��𰸣�A
���������A��Ca(OH)2Ϊǿ���ȫ���룬Ӧ���õȺţ�����B����AgC1����Һ�еμ�Na2S��Һ������ɫ������AgClת��Ϊ��Ag2S����ȷ��C����Ϊʯ��ˮ�������������ӷ���ʽ��OH?��ϵ��Ϊ1����ȷ��D��FeCl3��Һ�����ˮ�У����ȿ���ȡFe(OH)3���壬��ȷ��
�����Ѷȣ�һ��
5������� (����Ԥ����)(1)���ڵ��۵⻯����Һ�У��μ������������Ƽ�����Һ�������ῴ����Һ����ɫ��������Ϊ________�����ӷ���ʽΪ__________________________��
���ڵ�͵����γɵ���ɫ��Һ�У��μ��������Ƽ�����Һ��������ɫ����ʧ��������Ϊ______________________________�����ӷ���ʽ��_______________________________��
�۶ԱȢٺ͢�ʵ�����õĽ������I2��ClO����SO42������ǿ������˳������Ϊ_____________________________��
(2)������Ƭ��ͭƬ�����ʵ��֤��������ʵ����д����Ӧ�Ļ�ѧ����ʽ��
��Ũ����������Ա�ϡ����ǿ��________________________________��
���Ȼ�����Һ��Fe3���������Ա�����ͭ��Һ�е�Cu2��ǿ��__________________________��
�����Ļ�ԭ�Ա�ͭǿ��
___________________________________________________________��
�ο��𰸣�(1)��NaClO��KI����������I2
ClO����2I����H2O=I2��Cl����2OH��
��I2��Na2SO3��ԭ������
SO32����2OH��=SO42������H2O
��ClO����I2��SO42��
(2)��Cu��Ũ���ᷴӦ����ϡ�����Ӧ��
Cu��2H2SO4(Ũ)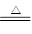 ?��SO2����2H2O
?��SO2����2H2O
��Cu����FeCl3��Һ��Ӧ��
2FeCl3��Cu=2FeCl2��CuCl2
��Fe����CuSO4��Һ��Ӧ�û���Cu��
Fe��CuSO4=FeSO4��Cu(�𰸲�Ψһ����������)
���������(1)���õ�����I2������������֤NaClO�������Ժ�Na2SO3�Ļ�ԭ�ԣ���д��ѧ����ʽʱע����Һ����Ϊ���ԡ�(2)�оٳ�����Ӧ��ʵ���ɡ�
�����Ѷȣ�һ��