微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 某原电池总反应的离子方程式为Zn+Cu2+═Zn2++Cu,该原电池的正确组成是( )
| 正极 | 负极 | 电解质溶液
A
Cu
Zn
ZnCl2
B
Cu
Zn
CuCl2
C
Zn
Cu
ZnCl2
D
Zn
Cu
CuCl2
|
A.A
B.B
C.C
D.D
参考答案:由电池反应式Zn+Cu2+═Zn2++Cu知,锌失电子发生氧化反应,失电子的物质的负极上发生氧化反应,所以锌作负极;不如锌活泼的金属或导电的非金属作正极,可用铜作正极;正极上铜离子得电子发生还原反应,所以电解质溶液中应含有铜离子,可用含有铜离子的盐溶液作电解质溶液,故选B.
本题解析:
本题难度:一般
2、填空题 (10分)如图所示:已知甲池的总反应式为:2CH3OH+3O2+4KOH?2K2CO3+6H2O
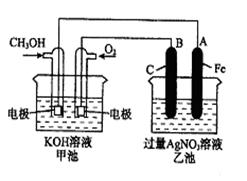
(1)请回答图中甲、乙两池的名称。甲池是?装置,乙池是?装置。
(2)B(石墨)电极的名称是?。在图中标明电子移动的方向。
(3)通入O2的电极的电极反应式是?。
(4)乙池中反应的化学方程式为?。
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2?mL(标准状况下)
参考答案:(14分)(1)原电池(化学能转变成电能)?电解池(电能转变成化学能)(2)阳极
(3)O2+2H2O+4e-=4OH-
(4)4AgNO3+2H2O 4Ag+4HNO3+O2↑?(5)280
4Ag+4HNO3+O2↑?(5)280
本题解析:(1)根据装置可知,甲是原电池,乙是电解池。
(2)原电池中负极失去电子,正极得到电子。所以甲中通入甲醇的是负极,通入氧气的是正极。则B是阳极。电子从原电池的负极经导线传递到电解池的阴极,从电解池的阳极经导线传递到原电池的正极。
(3)氧气得到电子,电极反应式为O2+2H2O+4e-=4OH-。
(4)乙中阴极氢离子放电生成氢气,阳极是银离子放电生成银,所以总反应式为
4AgNO3+2H2O 4Ag+4HNO3+O2↑。
4Ag+4HNO3+O2↑。
(5)铁电极形成的是银,物质的量是5.40g÷108g.mol=0.05mol,转移电子是0.05mol,所以根据电子得失守恒可知,消耗氧气是0.05mol÷4=0.0125mol,标准状况下的体积是0.0125mol×22.4L/mol=0.280L=280ml。
本题难度:一般
3、填空题 (9分)砷(As)广泛分布与自然界,砷与氮同主族,比氮多两个电子层。
(1)砷位于元素周期表中_____周期________族,其气态氢化物的稳定性比NH3_______(填“强”或“弱”);
(2)砷的常见酸性氧化物有As2O3和As2O5,请根据图中信息写出As2O3分解为As2O5的热化学方程式:________________________;

(3)已知:将酸滴入砷酸盐与KI混合的溶液中发生反应:AsO43-+2I
参考答案:
本题解析:
本题难度:一般
4、选择题 铅蓄电池用途极广,电解液为30%?H2SO4?溶液,电池的总反应式可表示为: Pb(s)+PbO2(s)+2H2SO4(aq)? 2PbSO4(s)+2H2O(l) 下列有关叙述正确的是
2PbSO4(s)+2H2O(l) 下列有关叙述正确的是
[? ]
A.放电时电解液的浓度不断增大?
B.放电时电子从Pb通过导线转移到PbO2
C.充电时Pb极与外电源的负极相连?
D.充电时PbO2电极发生还原反应,Pb电极上发生氧化反应
参考答案:BC
本题解析:
本题难度:一般
5、选择题 下列各组的电极材料和电解液,不能组成原电池的是( )
A.铜片、石墨棒,稀硫酸
B.铜片、石墨棒,硝酸银溶液
C.锌片、铜片,稀盐酸
D.铜片、银片,FeCl3溶液
参考答案:A、铜片和稀硫酸不能自发的发生氧化还原反应,所以不能构成原电池,故A符合;
B、两电极的活泼性不同,且铜片与硝酸银溶液能自发的发生氧化还原反应,所以能构成原电池,故B不符合;
C、两金属的活泼性不同,且锌片与稀盐酸能自发的发生氧化还原反应,所以能构成原电池,故C不符合;
D、两金属的活泼性不同,且铜片与氯化铁溶液能自发的发生氧化还原反应,所以能构成原电池,故D不符合;
故选A.
本题解析:
本题难度:一般