微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列物质的水溶液能发生离子反应的是(?)
A.Ba(NO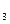 )
)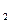 溶液与NaOH溶液
溶液与NaOH溶液
B.Na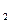 CO
CO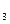 溶液与稀硫酸溶液
溶液与稀硫酸溶液
C.稀硫酸溶液与KCl溶液
D.KNO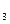 溶液与Na
溶液与Na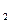 SO
SO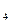 溶液
溶液
参考答案:B
本题解析:若通过离子交换能产生沉淀、气体或难电离物质,则能发生离子反应。综合比较,只有B选项中Na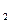 CO
CO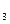 电离出来的CO
电离出来的CO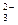 与稀H
与稀H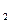 SO
SO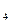 电离出来的H+反应可生成CO
电离出来的H+反应可生成CO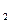 气体和H
气体和H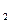 O,符合复分解反应发生的条件。
O,符合复分解反应发生的条件。
本题难度:一般
2、填空题 已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ・mol-1。回答有关中和反应的问题。
(1)用0.1 mol Ba(OH)2配成稀溶液与足量稀硝酸反应,能放出________kJ热量。
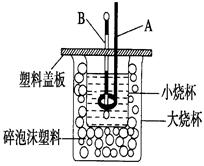
(2)如图装置中仪器A的名称是 ,碎泡沫塑料的作用是 。
(3)若通过实验测定中和热的ΔH,其结果常常大于-57.3 kJ・mol-1,其原因可能是
。
(4)用相同浓度和体积的氨水(NH3・H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 (填“偏大”、“偏小”、“无影响”)。
参考答案:(1)11.46
(2)环形玻璃搅拌棒;隔热,减少热量散失
(3)实验过程中难免有热量散失(合理答案均可)
(4)偏小
本题解析:(1)由H+(aq)+OH-(aq)
本题难度:一般
3、填空题 A、B、C、X、Y、Z元素的原子序数依次增大,根据信息完成问题:
元素A
| 各能级上的电子数相等
|
元素C
| 某种核素原子的质量数为18,中子数为10
|
元素X
| 单质是良好的半导体材料
|
元素Y
| 其单质为淡黄色晶体,常用来处理打碎的水银温度计
|
元素Z
| 3d能级上有4个未成对电子
|
(1)Z元素在周期表中的位置 ,其电子排布式 。
(2)AO2的熔点远低于XO2熔点的主要原因是 。
(3)X的氧化物和NaOH溶液反应的化学方程式 。
(4)B、C气态基态原子的第一电离能的大小关系为 。
(5)请用离子方程式表达Na2Y溶液呈碱性的原因 。
(6)已知CH3COOH(aq) H+(aq)+CH3COO―(aq) △H=+akJ/mol
H+(aq)+CH3COO―(aq) △H=+akJ/mol
CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l) △H=―bkJ/mol
则中和热的△H= kJ/mol
参考答案:(1)第四周期第Ⅷ族 (2分) 1s22s22p63s23p63d64s2 或[Ar]3d64s2 (2分)
(2)SiO2形成的是原子晶体,CO2形成的是分子晶体(2分)
(3)SiO2+2NaOH=Na2SiO3+H2O (2分)(4)N>O (2分)
(5)S2―+H2O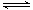 HS―+OH― HS―+H2O
HS―+OH― HS―+H2O H2S+OH―(2分)
H2S+OH―(2分)
(6)―(a+b)(2分)
本题解析:根据各能级上的电子数相等可推出A为C元素;根据某种核素原子的质量数为18,中子数为10可推出质子数为8,则C为O元素;根据原子序数依次增大可推出B为N元素;元素X的单质是良好的半导体材料,说明X为Si元素;元素Y的单质为淡黄色晶体,常用来处理打碎的水银温度计,说明Y为S元素;3d能级上有4个未成对电子,则Z为Fe。
(1)Z元素为Fe,在元素周期表中位于第四周期 Ⅷ族;电子排布式为:1s22s22p63s23p63d64s2。
(2)CO2形成分子晶体,分子间以分子间作用力结合,SiO2是原子晶体,原子间以共价键结合,共价键作用远远大于分子间作用力,所以CO2的沸点远低于SiO2的沸点。
(3)SiO2为酸性氧化物,与NaOH反应生成Na2SiO3和H2O:SiO2+2NaOH=Na2SiO3+H2O
(4)N原子2P轨道排布3个电子,为半充满状态,为较稳定状态,失电子较难,所以第一电离能:N>O
(5)S2?水解使溶液显碱性:S2―+H2O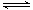 HS―+OH― HS―+H2O
HS―+OH― HS―+H2O H2S+OH―
H2S+OH―
((6)中和热为反应:H++OH?=H2O的?H,根据盖斯定律,?H=-?H1+?H2=―(a+b)kJ?mol?1。
考点:本题考查元素的推断、电子排布、沸点的比较、方程式的书写、盖斯定律的应用。
本题难度:困难
4、选择题 下列物质中,有极性共价键的是
A.氯化镁
B.溴化钾
C.水
D.单质碘
参考答案:C
本题解析:考查化学键的判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。所以选项A~D中含有的化学键分别是离子键、离子键、极性键、非极性键。所以答案选C。
本题难度:简单
5、填空题 (8分)现有①BaCl2 ②金刚石 ③NH4Cl ④Na2SO4 ⑤干冰 ⑥碘?⑦二氧化硅晶体七种物质,按下列要求回答(将物质的序号填入下列空格中):
(1)属于原子晶体的化合物是_____________。
(2)固态时属于分子晶体的是____________。
(3)熔化时需要破坏共价键的是___________,熔点最低的是___________。
(4)既含有离子键又含有共价键的是__________。
参考答案:(8分)(1)⑦(1分)(2)⑤⑥(2分)(3)②⑦;⑤(3分)(4)③④。(2分)
本题解析:(1)二氧化硅是空间网状结构的晶体即原子晶体且为化合物;(2)干冰是固态二氧化碳分子,碘是I2分子,故均为分子晶体;(3)熔化时破坏共价键的是原子晶体金刚石和二氧化硅;熔点最低的是分子晶体,二氧化碳常温下为气体,碘常温下为固体,熔点低的是干冰;(4)是离子化合物的是氯化钡和氯化铵,氯化钡中只有离子键,氯化铵中铵根离子中氮和氢原子之间形成共价键。
本题难度:一般