��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ʽΪC10H14�ĵ�ȡ������������ܵĽṹ��
A.2��
B.3��
C.4��
D.5��
�ο��𰸣�C
����������������������ʽΪC10H14�ĵ�ȡ��������ȡ�����Ļ�ѧʽ�ǣ�C4H9����ȡ�����Ƕ��������ڶ�����4�֣����Է���ʽΪC10H14�ĵ�ȡ������������ܵĽṹ��4�֣���ѡC��
���㣺����ͬ���칹����ж�
�������������е��Ѷȵ����⣬���������ǿ����Ҫ�ǿ���ѧ���Ա�����ͬϵ��ṹ�Լ�ͬ���칹���жϵ��˽����ճ̶ȣ�����������ѧ���Ĵ���˼ά������Ҳ���������ѧ��������û���֪ʶ���ʵ�������������
�����Ѷȣ�һ��
2��ѡ���� ���и��������У���Ϊ�������һ����
A.��ơ��ɱ�
B.ʯ�͡�Һ��
C.Na2CO3?10H2O��Na2CO3
D.ʯ��ʯ����ˮ
�ο��𰸣�C
������������������ݴ��������Լ����ʵijɷ��жϣ�
������������ֻ���������������ɵģ�����ϡ����һ��������ɵģ�������Ϊ���Դ���������
��ۣ���һ��������ɵ����ʣ�
�ۣ���ͬ�ַ��ӹ��ɣ�
��ɹ̶����й̶����������ʺͻ�ѧ���ʵ����ʣ���ר�ŵĻ�ѧ���ţ�
���A������ǵ�ľƾ���Һ���ǻ�����A����
B��ʯ����Ҫ�ɷ��Ǹ������������������������Ļ�����B����
C��Na2CO3?10H2O��Na2CO3����ѧ��ɹ̶���ʹ�ô������C��ȷ��
D����ˮ�ǰ���ˮ��Һ�����ڻ�����D����
��ѡ��C��
���������鴿����ĸ���ѶȲ���ע����մ���������ۣ���һ��������ɵ����ʣ��ۣ���ͬ�ַ��ӹ��ɣ���ɹ̶����й̶����������ʺͻ�ѧ���ʵ����ʣ���ר�ŵĻ�ѧ���ţ�
�����Ѷȣ�һ��
3��ѡ���� ��4Zn+10HNO3�T4Zn��NO3��2+NH4NO3+3H2O��Ӧ�У�����ԭ��HNO3��δ����ԭ��HNO3������֮��Ϊ
A.1��9
B.9��1
C.4��10
D.5��2
�ο��𰸣�A
�����������������4Zn+10HNO3�T4Zn��NO3��2+NH4NO3+3H2O��Ӧ�У��������Ϊ���Ժ������ԣ���Ӧ������������Ӵ��ڵ�Ϊδ����ԭ�����ᣬ��笠����Ӵ��ڵ�Ϊ����ԭ����������ɲ��
�����4Zn+10HNO3�T4Zn��NO3��2+NH4NO3+3H2O��Ӧ�У��������Ϊ���Ժ������ԣ���1mo��Դ:91������ www.91exAm.orgl����μӷ�Ӧʱ������NH4+Ϊ����ԭ�����ᣬΪ1mol��Zn��NO3��2��NH4NO3�й�����9molNO3-��δ����ԭ������Ϊ���ԣ���ԭ��HNO3��δ����ԭ��HNO3������֮��Ϊ1��9��
��ѡA��
���������⿼��������ԭ��Ӧ�ļ��㣬��Ŀ�ѶȲ������Ĺؼ�����ȷ�ж�Ԫ�ػ��ϼ۵ı仯����ȷ��Ӧ����������ʣ�ע�������Ӧ���ص㣮
�����Ѷȣ���
4��ѡ���� ��11.2g��Mg-Cu�������ȫ�ܽ��������������У��ռ���Ӧ������X���壨�ٶ�����������ȫ���ݳ���������������Һ�м���������NaOH��Һ������21.4g����������X�ijɷֿ�����
A.0.3mo1NO2��0.3mo1NO
B.0.1mol NO��0.2mol NO2��0.05mol N2O4
C.0.2mo1NO2��0.1mo1N2O4
D.0.6mo1NO
�ο��𰸣�B
�����������������Mg-Cu����������������ᷴӦ������Һ�м���������NaOH��Һ������21.4g����Ϊ������þ��������ͭ�����Գ�����������������Ϊ21.4g-11.2g=10.2g�����ʵ���Ϊ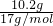 =0.6mol�����ݵ���غ��֪��11.2g��Mg-Cu�ṩ�ĵ���Ϊ0.6mol�����ѡ����ݵ���ת���غ��жϣ�
=0.6mol�����ݵ���غ��֪��11.2g��Mg-Cu�ṩ�ĵ���Ϊ0.6mol�����ѡ����ݵ���ת���غ��жϣ�
�����Mg-Cu����������������ᷴӦ������Һ�м���������NaOH��Һ������21.4g����Ϊ������þ��������ͭ�����Գ�����������������Ϊ21.4g-11.2g=10.2g�����ʵ���Ϊ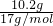 =0.6mol�����ݵ���غ��֪��11.2g��Mg-Cu�ṩ�ĵ���Ϊ0.6mol��
=0.6mol�����ݵ���غ��֪��11.2g��Mg-Cu�ṩ�ĵ���Ϊ0.6mol��
A������0.3mo1NO2��0.3mo1NO��NԪ�ػ�õ���Ϊ0.3mol����5-4��+0.3mol����5-2��=1.2mol����ʧ���Ӳ���ȣ���A����
B������0.1mol NO��0.2mol NO2��0.05mol N2O4��NԪ�ػ�õ���Ϊ0.1mol����5-2��+0.2mol����5-4��+0.05mol��2����5-4��=0.6mol����ʧ������ȣ���B��ȷ��
C������0.2mo1NO2��0.1mo1N2O4��NԪ�ػ�õ���Ϊ0.2mol����5-4��+0.1mol��2����5-4��=0.4mol����ʧ���Ӳ���ȣ���C����
D������0.6molNO��NԪ�ػ�õ���Ϊ0.6mol����5-2��=1.8mol����D����
��ѡ��B��
��������������ļ��㡢������ԭ��Ӧ����ȣ��Ѷ��еȣ���������ṩ�ĵ��ӵ����ʵ����ǽ���Ĺؼ���ע���غ�˼������ã�
�����Ѷȣ���
5��ѡ���� �������ӷ���ʽ��д��ȷ����
A.����ͭ��Һ������������Һ��Ӧ��SO42-+Ba2+��BaSO4��
B.ϡ�����м�������̼��������FeCO3+2H+��Fe2++CO2��+H2O
C.���������Һ�е��뼸������������Һ��H++OH-�TH2O
D.����̼������Һ��ͨ�������̼���壺2Na++CO32-+CO2+H2O�T2NaHCO3��
�ο��𰸣�CD
���������������A��©д����������ͭ�����ӷ�Ӧ��
B������������ԭ��Ӧ��������NO��������̼��ˮ��
C�����뼸������������Һ���ȷ������������ķ�Ӧ��
D������̼������Һ������̼�����ƣ����ܽ��С���������壮
���A������ͭ��Һ������������Һ��Ӧ�����ӷ�ӦΪCu2++2OH-+SO42-+Ba2+�TBaSO4��+Cu��OH��2������A����
B��ϡ�����м�������̼�����������ӷ�ӦΪ3FeCO3+NO3-+10H+�T3Fe3++3CO2��+5H2O+NO������B����
C�����������Һ�е��뼸������������Һ�����ӷ�ӦΪH++OH-�TH2O����C��ȷ��
D������̼������Һ��ͨ�������̼��������ӷ�ӦΪ2Na++CO32-+CO2+H2O�T2NaHCO3������D��ȷ��
��ѡCD��
���������⿼�����ӷ�Ӧ����ʽ����д����ȷ�����Ļ�ѧ��Ӧ�ǽ����Ĺؼ���ע��ѡ��BΪ�����ѵ㣬ѡ��DΪ�״��㣬��Ŀ�Ѷ��еȣ�
�����Ѷȣ�һ��