��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��1��д����ҵ�ô��ʯ��ʯ��ʯӢ����ͨ�����Ļ�ѧ����ʽ______��
��2�����ɰ�ɫFe��OH��2�����IJ������ó��ι���ȡ����O2��NaOH��Һ������FeSO4��ҺҺ���£��ټ���NaOH��Һ��ԭ����______���û�ѧ����ʽ��ʽ����
��3����100mLˮ��Ͷ��Na��Al��16�ˣ���ַ�Ӧ�����ʣ�����1g������ų�H2�����Ϊ______������״���£�
��4������0.3mol��NaAlO2��Һ�еμ�1mol/LHCl��������7.8�˳���ʱ��������������Ϊ______mL��
��5����һ������Fe��Fe2O3��CuO�����Ͷ��120mL2.2mol/L��������Һ�У���ַ�Ӧ������896mL��״���µ����壬�ò�����1.28g�����˺�����Һ�м���2mol/L��NaOH��Һ������40mLʱ��ʼ���ֳ���������Һ��FeSO4�����ʵ���Ũ��Ϊ______������Һ���Ϊ120mL��mol/L��
�ο��𰸣���1�������£�̼���ơ�̼��Ʒֱ�Ͷ������跴Ӧ���ɹ����κͶ�����̼����Ӧ����ʽ�ֱ�Ϊ��Na2CO3+SiO2 ����.Na2SiO3+CO2����CaCO3+SiO2����.CaSiO3+CO2�����ʴ�Ϊ��Na2CO3+SiO2 ����.Na2SiO3+CO2����CaCO3+SiO2����.CaSiO3+CO2����
��2���������������ȶ����ױ���������������������Ӧ����ʽΪ��4Fe��OH��2+O2+2H2O=4Fe��OH��3���ʴ�Ϊ��4Fe��OH��2+O2+2H2O=4Fe��OH��3��
��3��Al��ˮ����Ӧ������ʣ�����Ӧ����Al����Ӧ����ʽΪ2Na+2H2O=2NaOH+H2����2Al+2NaOH+2H2O=2NaAlO2+3H2�������Եó���ϵʽNa��NaOH��Al������뷴Ӧ��Na��Al������֮��Ϊ23��27��Na��Al��������Ϊ15g������n��Na��=15g23+27��2323g/mol=0.3mol��n��Al��=15g23+27��2727g/mol=0.3mol������Na��Al������֮��Ĺ�ϵʽ���������=��0.3mol��0.5+0.3mol��1.5����22.4L/mol=13.44L��
�ʴ�Ϊ��13.44��
��4��n��Al��OH��3��=7.8g78g/mol=0.1mol��0.3mol��һ������ǣ���Ԫ�ش�����ƫ�����ƺ����������У�
��ʱ����������ֻ�ܳ���һ����AlO2-������NaAlO2+HCl+H2O=Al��OH��3��+NaCl�ã�n��HCl��=n��Al��OH��3��=0.1mol�����������=0.1mol1mol/L=100mL��
��һ���������Ԫ�ش������Ȼ��������������У���ʱ����϶࣬�Ȱ�AlO2-ȫ�����������ֽ����ֳ����ܽ⣬��������������Ҫn��HCl��=n��NaAlO2��=n��Al��OH��3��=0.3mol���ܽ�Al��OH��3�����Ȼ�����Ҫ�����n��HCl��=3n��AlCl3��=3����0.3-0.1��mol=0.6mol��������Ҫ�������=0.3mol+0.6mol1mol/L=900mL��
�ʴ�Ϊ��100��900��
��5�����������ϡ���ᷴӦ���й���ʣ�࣬˵����Һ�в����������ӣ�����Һ�м������2mol/L��NaOH��Һ������40mLʱ��ʼ���ֳ�����˵��������ʣ�࣬���Ⱥ�ͭ���Ӻ�������ӷ����û���Ӧ��������Һ�е����������ᡢ����������n��H2SO4��=2.2mol/L��0.12L=0.264mol��
���������Ʒ�Ӧ����������ʵ���=12n��NaOH��=12��2mol/L��0.04L=0.04mol��
ʣ�����������ʵ���=0.264mol-0.04mol=0.224mol��
ʣ����������巴Ӧ����������������������������������Ĺ�ϵʽ�����������������ʵ���Ũ��=0.224mol0.12L=1.87mol/L��
�ʴ�Ϊ��1.87��
���������
�����Ѷȣ�һ��
2������� �Լ�����FeSO4��Һ�м���NaOH��Һʱ�ķ�Ӧ����д���йط�Ӧ�Ļ�ѧ����ʽ��
�ο��𰸣���FeSO4��Һ�м���NaOH��Һ�ᷢ����Ӧ��FeSO4+2NaOH�TFe��OH��2��+Na2SO4�����ɰ�ɫ��Fe��OH��2��������ɫ��Fe��OH��2���ױ�������������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ��Fe��OH��3����Ӧ��4Fe��OH��2+O2 +2H2O�T4 Fe��OH��3��
�����ɰ�ɫ������Ѹ�ٱ�Ϊ����ɫ�����ձ�Ϊ���ɫ��FeSO4+2NaOH�TFe��OH��2��+Na2SO4��4Fe��OH��2+O2 +2H2O�T4Fe��OH��3��
���������
�����Ѷȣ�һ��
3������� ij�о���ѧϰС�����о���Fe2+�Ʊ�Fe��OH��2�Ĺ����У����������ʵ�鷽����
��ʵ����ơ�
����һ������ͼ1����ʵ�飬����A�еķ�Ӧ��ʼʱ�����ɼ�C���ڴ�״̬��һ��ʱ��رյ��ɼ�C������A�еķ�Ӧ���ڽ��У�������______�����й۲쵽��ɫ��������ʵ�����漰���Ļ�ѧ����ʽ�У�______��
����������ͼ2����ʵ�飬���������������Һ�����ȹ۲쵽��ɫ������������ṩ���Լ���缫������ѡ����ȷ��������ں����ϣ��ٴ�ˮ��NaCl��Һ��NaOH��Һ�����Ȼ�̼��CuCl2��Һ���Ҵ���Fe����ֲ���͢�̼��
aΪ______��bΪ______��cΪ______��dΪ______��������ţ�
��̽��˼����
ʵ���������ʵ���г��ְ�ɫ�ij�������ת��Ϊ����ɫ����ɫ����ô��ν��ͳ��ֻ���ɫ����ɫ�������أ�
��1����ͬѧ�������Ϻõ�Fe��OH��2������Ϣ��
| �������� | ������������ | ��ѧ��������
����ѧ�ǵ䡷���������࣬1989���P637
��ɫ���η�ĩ���ɫ������ɫ��������
������Ӵ��ױ���������ϸ�����ڿ����У�������ȼ�ճ���
����ѧ��ͨ��ѧ���²ᣩ����ӥ��P637
��ɫ����
�˳����ױ���������ɫFe3��OH��8
����ͨ��ѧ�̡̳����²ᣩP788
��ɫ
��ǿ������O2��Ѹ�ٱ����ɫ
Fe��OH��3����ʱ��Ϊ�������м����Ϊ����ɫ�����к���Fe2+��Fe3+��
|
�Ķ������Ϻ��������ʵ���г��ֻ���ɫ����ɫ������Ľ����ǣ�______���������ἰ����ɫFe3��OH��8�������������ʽ��ʾ��д��______��
��2����ͬѧ������ɫԭ������ɫ����ɫ�����ܵ������ɫ�����ɫ�ij�ʶ����Ϊ��ɫ�������γ�Fe��OH��2?nH2O���£�����ˮԡ�ķ�ʽ���ȡ�����һ�������ɵ���ɫ�������۲쵽�������̱�����ƣ�����ʱ��������һ���е��ɼ�CӦ����______������رա���״̬������A�еķ�Ӧ�봦��______���ֹͣ����������״̬��д����ʵ����֧����ͬѧ�۵�Ļ�ѧ����ʽ______��
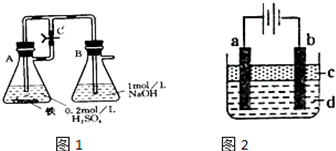
�ο��𰸣���ʵ����ơ�
����һ���رջ���C��Aƿ��������ϡ���ᷴӦ�ų������������ų���ʹƿ���������ӣ�ѹǿ�����ѷ�Ӧ���ɵ�����������Һѹ��Bƿ�ڣ�������������������������Ӧ�����������������ij�������ˣ���Bƿ�ڹ۲쵽�����������漰�ķ�Ӧ�У�Fe+H2SO4=FeSO4+H2����FeSO4+2NaOH=Fe��OH��2��+Na2SO4��H2SO4+2NaOH=Na2SO4+2H2O��
�ʴ�Ϊ��B��Fe+H2SO4=FeSO4+H2����FeSO4+2NaOH=Fe��OH��2��+Na2SO4��H2SO4+2NaOH=Na2SO4+2H2O��
����������ͼ2����ʵ�飬���������������Һ�����ȹ۲쵽��ɫ�����������������ŵ������������ӣ���������������������ķǽ���������������ѡ������ʯī��
�����������ӷŵ�ͬʱ���������������ɣ����Կ���ѡ������������Һ���Ȼ�����Һ��Ϊ��ֹ�������ӱ���������C���ܶ�С��ˮ���ܶȣ�����C����ѡ��ֲ���ͣ�
�ʴ�Ϊ���ߣ����ߣ��ࣻ�ڻ�ۣ�
��̽��˼����
��1����������Ϣ��֪������������Ϊ��ɫ����������Ϊ��ɫ�����ߵĻ������ֳ���ɫ�����ʵ���г��ֻ���ɫ����ɫ������Ӧ�����ɵ�Fe��OH��2���ֱ�����������������Fe��OH��3��Ե�ʣ��������ἰ����ɫFe3��OH��8��������ΪFe��OH��2��Fe��OH��3�Ľ�����һ�����ʣ����м���+2����Ҳ��+3��������˸�дΪ���������ʽʱ��8����ԭ��Ӧ��ϳ�4H2O������Ӧд�ɣ�FeO?Fe2O3?4H2O��
�ʴ�Ϊ������Fe��OH��2���ֱ�����������������Fe��OH��3��FeO?Fe2O3?4H2O��
��2����֤��ͬѧ�IJ²�Ҫ��ֹFe ��OH��2?nH2O��������������˻���CӦ���ڴ�״̬������A�еķ�ӦҲҪ�������У�Fe ��OH��2?nH2O���ȷֽ�����������������ˮ��
�ʴ�Ϊ����������Fe��OH��2?nH2O��.Fe��OH��2+nH2O��
���������
�����Ѷȣ�һ��
4��ѡ���� ����ʵ��װ��ͼ������ȷ���ǣ�������
A��
�����������ƹ���
B��
����150mL?0.10mol?L-1����
C��
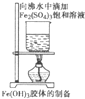
Fe��OH��3Һ����Ʊ�
D��
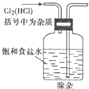
����
�ο��𰸣�C
���������
�����Ѷȣ���
5��ѡ���� �������ʼ��ת���У������в���ͨ��һ����Ӧʵ�ֵ��ǡ�
[? ]
A��Fe �� FeCl2 �� Fe(OH)2 �� Fe(OH)3
B��Al �� Al2O3 �� Al(OH)3 �� NaAlO2
C��S �� SO2 ��H2SO4 �� MgSO4
D��N2 �� NO �� NO2 �� HNO3
�ο��𰸣�B
���������
�����Ѷȣ���