| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《盐类水解的原理》高频试题预测(2017年最新版)(六)
参考答案:A 本题解析:A中只有水分子,B中含有水分子和一水合氨分子,C中含有水分子和次氯酸分子,D中含有水分子和HF分子。答案选A。 本题难度:一般 2、选择题 25℃时,a mol・L-1一元酸HA与b mol・L-1NaOH等体积混合后,pH为7,则下列关系一定正确的是 |
参考答案:C
本题解析::若HA为强酸,a=b;若HA为弱酸,则a>b,但无论HA是强酸还是弱酸,均有电荷守恒:
c(Na+)+ c(H+)=c(A-)+ c(OH―),pH=7,c(H+)= c(OH―),所以c(A-) = c(Na+)。
考点:离子浓度比较
点评:本题可直接根据电荷守恒解答。
本题难度:一般
3、填空题 常温下,向25 mL 0.1 mol/L MOH溶液中逐滴加入0.2 mol/L HA溶液,曲线如图所示(体积变化忽略不计)。回答下列问题:
(1)写出MOH在水溶液中的电离方程式
(2)MOH与HA恰好完全反应时,溶液呈_____性(填“酸”、“碱”或“中”),理由是(用离子方程式表示)__ _____;此时,混合溶液中由水电离出的c(H+)__ _ 0.2 mol/L HA溶液中由水电离出的c(H+)(填“>”“<”或“=”)。
(3)写出B点混合溶液中各离子浓度的大小关系_________ _;
(4)D点时,溶液中c(A-)+c(HA)________2 c(M+)(填“>”“<”或“=”);若此时测得混合溶液的pH = 3,则 c(HA) + c(H+) = __________mol/L(数字表达式,不必具体算出结果)
参考答案:(11分) (1)MOH=M+ + OH-(若写可逆号扣1分)(2分)
(2)碱(1分) A- + H2O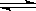 HA + OH-(2分) > (1分)
HA + OH-(2分) > (1分)
(3)[M+] = [A-]>[H+]=[OH-] (2分)
(4) = (2分) 0.05 + 10-11 (若只写0.05不得分)(2分)
本题解析:(1)根据图像可知,当加入13mlHA时,HA是过量的,但溶液显中性,这说明MOH一定是强碱,而HA是弱酸,则MOH在水溶液中的电离方程式为MOH=M+ + OH-。
(2)由于HA是弱酸,MOH是强碱,则MOH与HA恰好完全反应时,生成的MA水解,溶液呈碱性,水解方程式是A- + H2O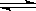 HA + OH-。HA是弱酸,抑制水的电离,而水解促进水的电离,所以混合溶液中由水电离出的c(H+)>0.2 mol/L HA溶液中由水电离出的c(H+)。
HA + OH-。HA是弱酸,抑制水的电离,而水解促进水的电离,所以混合溶液中由水电离出的c(H+)>0.2 mol/L HA溶液中由水电离出的c(H+)。
(3)B点溶液显中性,则根据电荷守恒可知[M+]=[A-]>[H+]=[OH-]。
(4)D点溶液中的溶质是MA和HA,且二者的浓度是相等的,所以根据物料守恒可知,c(A-)+c(HA)=2 c(M+)。有电荷守恒可知c(A-)+c(OH-)=c(M+)+c(H+),则c(HA) + c(H+)=c(OH-)+ c(M+)=10-11+0.05。
考点:考查弱电解质的电离、盐类水解、溶液中离子浓度大小比较和有关计算
点评:该题是中等难度的试题,试题贴近高考,综合性强,试题基础性强,侧重能力的培养和解题方法的指导,主要是考查学生分析和解决问题的能力,有利于培养学生的逻辑思维能力和发散思维能力。该题的关键是明确溶液中离子的几种守恒关系,即电荷守恒、物料守恒及质子守恒。
本题难度:困难
4、选择题 下列溶液中粒子的物质的量浓度关系正确的是
A.0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)
B.20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L盐酸混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+)
C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-)
D.0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH)
参考答案:B
本题解析:A.0.1 mol/L NaHCO3溶液与0.1 mol/L NaOH溶液等体积混合,二者恰好反应生成碳酸钠和水。碳酸根水解溶液显酸性,且碳酸根水解分步进行,则所得溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-),A错误;B.20 mL 0.1 mol/L CH3COONa溶液与10 mL 0.1 mol/L盐酸混合后,二者反应生成醋酸和氯化钠,其中醋酸钠过量一般,所得溶液呈酸性,这说明溶液中醋酸的电离程度大于醋酸根的水解程度,因此所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+),B正确;C.氨水是弱碱,盐酸是强酸,则室温下,pH=2的盐酸与pH=12的氨水等体积混合后氨水过量,溶液显碱性,则所得溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+),C错误;D.0.1 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合二者恰好反应生成醋酸钠,醋酸根水解溶液显碱性,则根据质子守恒可知所得溶液中:c(OH-)=c(H+)+c(CH3COOH),D错误,答案选B。
考点:考查溶液中离子浓度大小比较
本题难度:困难
5、选择题 下列事实不能用勒夏特列原理解释的是
A.将氯化铁溶液加热蒸干最终得不到氯化铁固体
B.钢铁在潮湿的空气中容易生锈
C.温度过高对合成氨不利
D.常温下,将 1 mL PH = 3的醋酸溶液加水稀释至100mL,测得其PH<5
参考答案:B
本题解析:A、FeCl3+3H2O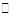 Fe(OH)3+3HCl,加热时HCl受热挥发,降低了生成物的浓度,使平衡右移,符合勒夏特列原理;B、钢铁生锈,是电化学没有可逆反应,不符合勒夏特列原理;C、合成氨是放热反应,升高温度,平衡左移,符合勒夏特列原理;D、CH3COOH
Fe(OH)3+3HCl,加热时HCl受热挥发,降低了生成物的浓度,使平衡右移,符合勒夏特列原理;B、钢铁生锈,是电化学没有可逆反应,不符合勒夏特列原理;C、合成氨是放热反应,升高温度,平衡左移,符合勒夏特列原理;D、CH3COOH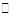 CH3COO-+H+,加水稀释离子浓度降低,平衡正向移动,符合勒夏特列原理。因此答案选B。
CH3COO-+H+,加水稀释离子浓度降低,平衡正向移动,符合勒夏特列原理。因此答案选B。
考点:考查化学反应原理等相关知识。
本题难度:一般
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高中化学知识点大全《氯气的化学.. | ||