��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �״�����Ϊȼ�ϵ�ص�ԭ�ϣ���CH4��H2OΪԭ�ϣ�ͨ�����з�Ӧ��Ӧ���Ʊ��״���
��ӦI��CH4?��g��+H2O?��g��=CO?��g��+3H2?��g����H=+206.0kJ?mol-1
��ӦII��CO?��g��+2H2?��g��=CH3OH?��g����H=-129.0kJ?mol-1
��1��CH3OH?��g����H2��g����Ӧ����CH4��g����H2O��g�����Ȼ�ѧ����ʽΪ______��
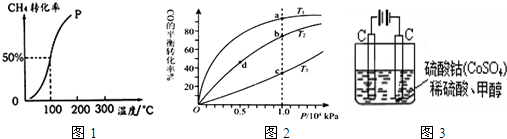
��2����1.0mol?CH4��2.0mol?H2O?��?g?��ͨ���ݻ��̶�Ϊ10L�ķ�Ӧ�ң���һ�������·�����ӦI�������һ����ѹǿ��CH4��ת�������¶ȵĹ�ϵ��ͼ1��
�ټ���100��ʱ�ﵽƽ�������ʱ��Ϊ5min������H2��ʾ�÷�Ӧ��ƽ����Ӧ����Ϊ______��
��100��ʱ��ӦI��ƽ�ⳣ��Ϊ______��
�ۿ������жϸ÷�Ӧ�ﵽƽ��״̬�ı�־��______��������ĸ��
A��CO�ĺ������ֲ���?
B��������CH4Ũ����COŨ�����
C�������л��������ܶȱ��ֲ���?
D��3V����CH4��=V�棨H2��
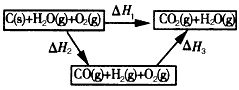
��3�����շ�ӦII�����ɼ״���������ͬ�����ʵ���Ͷ�ϣ����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ2��ʾ������˵����ȷ����______
A���¶ȣ�T1��T2��T3
B������Ӧ���ʣ��ͣ�a�����ͣ�c����?�ͣ�b�����ͣ�d��
C��ƽ�ⳣ����K��a����K��c����?K��b��=K��d��
D��ƽ��Ħ��������M��a����M��c����?M��b����M��d��
��4����ҵ�����ü״��Ʊ������ij��÷���֮һΪ���״��������������÷��е�һ����Ҫ��ӦΪCH3OH��g��?CO��g��+2H2��g�����˷�Ӧ���Է����е�ԭ����______��
��5���״���ˮ�ʻ����һ������Ⱦ����һ�ֵ绯ѧ��������������Ⱦ����ԭ���ǣ�ͨ���Co2+������Co3+��Ȼ����Co3+����������ˮ�еļ״�������CO2��������ʵ������ͼ3װ��ģ���������̣�
��д�������缫��Ӧʽ______��
��д����ȥ�״������ӷ���ʽ______��
����3ͼװ���еĵ�ԴΪ�״�-����-KOH��Һ��ȼ�ϵ�أ����ظ����ĵ缫��ӦʽΪ��______��
�ο��𰸣���1��I��CH4 ��g��+H2O ��g��=CO ��g��+3H2 ��g����H=+206.0kJ?mol-1
II��CO ��g��+2H2 ��g��=CH3OH ��g����H=-129.0kJ?mol-1
���ݸ�˹���ɢ�+��õ�CH4��g��+H2O��g��=CH3OH ��g��+H2��g������H=+77kJ?mol-1
����CH3OH ��g����H2��g����Ӧ����CH4��g����H2O��g�����Ȼ�ѧ����ʽΪ��CH3OH ��g��+H2��g��=CH4��g��+H2O��g����H=-77.0 kJ?mol-1
�ʴ�Ϊ��CH3OH?��g��+H2��g��=CH4��g��+H2O��g����H=-77.0?kJ?mol-1
��2����1.0mol CH4��2.0mol H2O �� g ��ͨ���ݻ��̶�Ϊ10L�ķ�Ӧ�ң���һ�������·�����ӦI��ͼ�������֪100��C����ת����Ϊ50%�����ݻ�ѧƽ������ʽ��ʽ
? ?CH4 ��g��+H2O ��g��=CO ��g��+3H2 ��g��
��ʼ����mol��?1.0? 2.0? 0? 0
�仯����mol�� 1.0��50%? 0.5? 0.5? 1.5
ƽ������mol�� 0.5? 1.5? 0.5? 1.5
�ټ���100��ʱ�ﵽƽ�������ʱ��Ϊ5min������H2��ʾ�÷�Ӧ��ƽ����Ӧ����=1.5mol10L5min=0.03 mol?L-1?min-1
�ʴ�Ϊ��0.03?mol?L-1?min-1
��100��ʱ��ӦI��ƽ��Ũ��Ϊc��CH4��=0.05mol/L��c��H2O��=0.15mol/L��c��CO��=0.05mol/L��c��H2��=0.15mol/L��
ƽ�ⳣ��K=c(CO)c3(H2)c(CH4)c(H2O)=0.05��0.1530.05��0.15=2.25��10-2
�ʴ�Ϊ��2.25��10-2?
��CH4 ��g��+H2O ��g��=CO ��g��+3H2 ��g��
A��CO�ĺ������ֲ��䣬˵����Ӧ�ﵽƽ�⣬��A��ȷ��
B��������CH4Ũ����COŨ����ȣ�������������ʼ���йط�Ӧ��һ���ﵽƽ�⣬��B����
C����������������䣬������䣬��Ӧ�������ܶȲ��䣬�����л��������ܶȱ��ֲ��䲻��˵����Ӧ�ﵽƽ�⣬��C����
D����Ӧ����֮�ȵ��ڻ�ѧ����ʽϵ��֮��������Ӧ����֮�ȣ�3V����CH4��=V����H2������3V����CH4��=V�棨H2��˵��V����H2��=V�棨H2��˵����Ӧ�ﵽƽ�⣬��D��ȷ��
�ʴ�Ϊ��A?D��?
��3��A���÷�ӦΪ���ȷ�Ӧ���¶�Խ�ͣ�CO��ת����Խ����T1��T2��T3����A����
B����ͼ��֪��a��c����ѹǿ��ͬ��ƽ��ʱa��COת���ʸ��ߣ��÷�ӦΪ���ȷ�Ӧ���¶�Խ�ͣ�CO��ת����Խ���¶�T1��T3���¶�Խ�ߣ���Ӧ����Խ�죬�ʦԣ�a�����ԣ�c����b��d�����¶���ͬ��ѹǿԽ��Ӧ����Խ��b�����d��ѹǿ����v��b����v��d������B����
C����ͼ��֪��a��c����ѹǿ��ͬ��ƽ��ʱa��COת���ʸ��ߣ��÷�ӦΪ���ȷ�Ӧ�����¶�T1��T3�������¶�ƽ��������Ӧ�����ƶ�����K��a����K��c����ƽ�ⳣ��ֻ���¶��йأ�b��d�����¶���ͬ��ƽ�ⳣ����ͬ����K��b��=K��d������C��ȷ��
D��COת���ʵ�Խ��n��ԽС����M=mn��֪��a��n��С����M��a����M��c����M��b����M��d������D����
��ѡC��
��4���״��������������÷��е�һ����Ҫ��ӦΪCH3OH��g��?CO��g��+2H2��g������Ӧ��H��0����Ӧ�Է�������Ҫ�����H-T��S��0�����Է�Ӧ�Է���������Ϊ�÷�Ӧ��������ķ�Ӧ��
�ʴ�Ϊ���÷�Ӧ��һ�������ķ�Ӧ����S��0��
��5�����١�ͨ���Co2+������Co3+������������ʧ���ӷ���������Ӧ���缫��ӦΪCo2+-e-=Co3+��
�ʴ�Ϊ��Co2+-e-=Co3+��
�ڡ���Co3+����������ˮ�еļ״�������CO2����������������ԭΪCo2+�����ԭ���غ������غ��֪����ԭ����H+����ƽ��д���ӷ���ʽΪ��6Co3++CH3OH+H2O=CO2��+6Co2++6H+��
�ʴ�Ϊ��6Co3++CH3OH+H2O=CO2��+6Co2++6H+����
����3ͼװ���еĵ�ԴΪ�״�-����-KOH��Һ��ȼ�ϵ�أ��״��ڸ���ʧ���ӷ���������Ӧ���ڼ���Һ������̼���Σ����ظ����ĵ缫��ӦʽΪCH3OH-6e-+8OH-�TCO32-+6H2O��
�ʴ�Ϊ��CH3OH-6e-+8OH-�TCO32-+6H2O��
���������
�����Ѷȣ�һ��
2������� ��֪��
�ٽ�úת��Ϊˮú������Ҫ��ѧ��ӦΪC(s)+H2O(g) CO(g)+H2(g)��
CO(g)+H2(g)��
��C(s)��CO(g)��H2(g)��ȫȼ�յ��Ȼ�ѧ����ʽ�ֱ�Ϊ��
C(s) +O2(g)=CO2(g) ��H=-393.5 kJ/mol
CO(g) +l/2O2(g)=CO2(g) ��H= -283.0 kJ/mol
H2(g) +l/2O2(g)=H2O(g) ��H= -242.0 kJ/mol
��ش�
(1)����������Ϣ��д��C(s)��ˮ������Ӧ���Ȼ�ѧ����ʽ��________________________��
(2)�ȽϷ�Ӧ�����ݿ�֪��1 mol CO(g)��1 mol H2(g)��ȫȼ�շų�������֮�ͱ�1 mol C(s)��ȫȼ�շų��� �����ࡣ��ͬѧ�ݴ���Ϊ��úת��Ϊˮú������ʹúȼ�շų����������������ͬѧ���ݸ�˹����������ͼ��ʾ��ѭ��ͼ�����ݴ���Ϊ��úת��Ϊˮú����ȼ�շų���������úֱ��ȼ�շų���������ȡ���
(3)
��������ס�����ͬѧ�۵���ȷ����_____���� ���ס����ҡ������жϵ�������_____________��
(3)��úת��Ϊˮú����Ϊȼ�Ϻ�úֱ��ȼ������кܶ��ŵ㣬���о����е������ŵ�____________��
�ο��𰸣�(1)C(s) +H2O(g)=CO(g) +H2(g) ��H= +131.5 kJ/mol
(2)�ң���ͬѧ������úת��Ϊˮú��Ҫ������������ ��H1= ��H2+ ��H3���ҡ�H2 >0��
(3)������Ⱦ��ȼ�ճ�֣������䣩
���������
�����Ѷȣ�һ��
3��ѡ���� 2008��9���ҹ������ߡ��������գ��й�����Աʵ���״�̫�����ߣ����ػ����ԭ�����£�N2H4����Ϊ��������ȼ�ϣ�NO2Ϊ����������Ӧ���ɵ�����ˮ��������֪��
N2(g)+2O2(g)�T2NO2(g)����H=+67.7kJ/mol
N2H4(g)+O2(g)�TN2(g)+2H2O(g)����H=-534kJ/mol
�����ж���ȷ���ǣ� ? ��
A���������������������Ļ�ѧ��Ӧ���Ƿ��ȷ�Ӧ
B��N2H4��ȼ����Ϊ534kJ/mol
C������NO2��Ӧ���Ȼ�ѧ����?2N2H4��g��+2NO2��g���T3N2��g��+4H2O��g������H=-1135.7kJ/mol
D��.3.2g����ȫ��Ӧת�Ƶĵ�����Ϊ0.6mol
�ο��𰸣�C
���������
�����Ѷȣ���
4������� ������ҵ���ҹ������д���ʮ����Ҫ��λ�ã���ҵ�ϲ��ø�¯ұ�������ó�����̿���������ۼ���ʯ��ʯ����ԭ�ϣ���֪������ԭ����ԭʱ�����еģ���ԭʱ�¶ȼ�CO��CO2ƽ����������CO����������Ĺ�ϵ��ͼ��
��1������Ԫ�����ڱ���λ��______����______�壮
��2�����¶ȵ���570��ʱ����ԭ��������ɣ����¶ȸ���570��ʱ�����η����Ļ�ԭ��Ӧ�У�______��ѡ����ͼ�е�a��b��c��d��գ���
��3��Ϊ���ٸ�¯ұ��ʱ����CO��β���ŷţ������о�����ȡ����______��
��a�������������䣬���Ӹ�¯�ĸ߶�
��b�����ڻ�ԭʱ��¯��
��c������ԭ���н�̿�������ı���
��d�������ɵ���ˮ��ʱ�Ƴ�
��4����֪���з�Ӧ��ֵ��
| ��Ӧ��� | ��ѧ��Ӧ | ��Ӧ��
��
Fe2O3��s��+3CO��g��=2Fe��s��+3CO?2��g��
��H1=-26.7kJ?mol-1
��
3Fe2O3��s��+CO��g��=2Fe3O4��s��+CO2��g��
��H2=-50.8kJ?mol-1
��
Fe3O4��s��+CO��g��=3FeO��s��+CO2?��g��
��H3=-36.5kJ?mol-1
��
FeO��s��+CO��g��=Fe��s��+CO2��g��
��H4
|
��Ӧ�ܡ�H4=______kJ?mol-1��
��5��1100��ʱ��FeO��s��+CO��g��?Fe��s��+CO2��g����ƽ�ⳣ��K=0.4������һ�ܱ������У�����7.2gFeO��ͬʱͨ��4.48LCO�����ۺ�Ϊ��״�������������µ�1100�棬��ά���¶Ȳ��䣬��ƽ��ʱ��FeO��ת����Ϊ��______��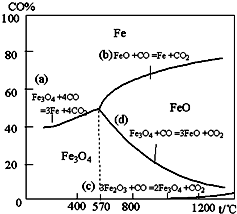
�ο��𰸣���1������26��Ԫ�أ�λ��Ԫ�����ڱ���λ�� �������ڵڢ��壮
�ʴ�Ϊ���ġ�����
��2����ͼ��֪���¶ȵ���570��ʱ��������Ӧbcd������Ԫ�صĻ��ϼ۽��Ϳ�֪�����η����Ļ�ԭ��Ӧ��
3Fe2O3+CO=2Fe3O4+CO2��Fe3O4+CO=3FeO+CO2��FeO+CO=Fe+CO2���ʷ�Ӧ˳��Ϊcdb��
�ʴ�Ϊ��cdb��
��3��
��a�������������䣬���Ӹ�¯�ĸ߶ȣ���Ӱ��ƽ���ƶ������ܼ�Сһ����̼���ŷţ���a����
��b����ӦΪ���ȷ�Ӧ�����ڻ�ԭʱ��¯�£�������ƽ��������Ӧ���У�����һ����̼�ĺ�������b��ȷ��
��c����̿��������ǹ��壬����ԭ���н�̿�������ı�������Ӱ��ƽ���ƶ������ܼ�Сһ����̼���ŷţ���c����
��d�����ɵ���ˮΪҺ̬�������ɵ���ˮ��ʱ�Ƴ�����Ӱ��ƽ���ƶ������ܼ�Сһ����̼���ŷţ���d����
��ѡ��acd��
��4����֪����Fe2O3��s��+3CO��g��=2Fe��s��+3CO?2��g����H1=-26.7kJ?mol-1��
��3Fe2O3��s��+CO��g��=2Fe3O4��s��+CO2��g����H2=-50.8kJ?mol-1��
��Fe3O4��s��+CO��g��=3FeO��s��+CO2?��g����H3=-36.5kJ?mol-1��
�ɸ�˹���ɿ�֪���١�3-��-�ۡ�2��6FeO��s��+6CO��g��=6Fe��s��+6CO2��g����H=3��H1-��H2-2��H1��
���ԡ�H4=16��H=16��3��H1-��H2-2��H1��=16��[3����-26.7kJ?mol-1��-��-50.8kJ?mol-1��-2����-36.5kJ?mol-1��]=
7.3kJ?mol-1��
�ʴ�Ϊ��7.3��
��5��4.48LCO�����ۺ�Ϊ��״�������ʵ���Ϊ4.48L22.4L/mol=0.2mol����ת���ʵ�CO�����ʵ���Ϊxmol����
? FeO��s��+CO��g��?Fe��s��+CO2��g����
��ʼ��mol����0.2? 0
�仯��mol����x? x
ƽ�⣨mol����0.2-x? x
һ����̼��ϵ�����ڶ�����̼��ϵ�����ʿ��������ʵ�������Ũ�ȼ���ƽ�ⳣ����
����x0.2-x=0.4�����x=235mol
�ɷ���ʽ��֪��ת����FeO�����ʵ���n��FeO��=n��CO��=235mol��
����FeO��ת����Ϊ235mol?��72g/mol7.2g��100%=57.1%��
��FeO��ת����Ϊ57.1%��
���������
�����Ѷȣ�һ��
5������� �ο�����ͼ�����й�Ҫ��ش����⡣
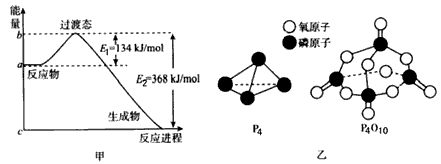
(1)��ͼ��l mol NO2(g)��1mol CO(g)��Ӧ����CO2��NO�����������仯ʾ��ͼ�����ڷ�Ӧ��ϵ�м����������Ӧ��������E1�ı仯��____����H�ı仯��____ ���������С�����䡱������д��
NO2��CO��Ӧ���Ȼ�ѧ����ʽ��____________________��
(2)�״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ���ǣ�
��CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ��H=+49.O kJ/mol
��CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g)��H=-192.9 kJ/mol
��֪��H2O(g)=H2O(l) ��H=-44 kJ/mol
��״���ȼ���Ȼ�ѧ����ʽΪ____________________��
(3)�±��Dz��ֻ�ѧ���ļ�������

��֪����ȼ����Ϊd kJ/mol����������ȫȼ�յIJ���ṹ����ͼ��ʾ�����ϱ���x=________kJ/mol���ú���a��b��c��d�Ĵ���ʽ��ʾ��
�ο��𰸣�(1)��С�����䣻NO2(g)+CO(g)=CO2(g)+NO(g) ��H=-234kJ/mol
(2)CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ��H=-764.7kJ/mol
(3)-(12b-d-6a-5c)��(d+6a+5c-12b)
���������
�����Ѷȣ�һ��