��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��б���������ת��Ϊ��������������仯ͼ��ͼ��ʾ��
����˵����ȷ����
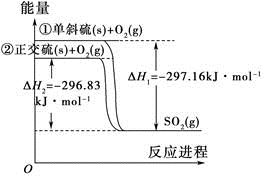
A��S(s����б)=S(s������) ��H����0.33 kJ��mol��1
B��������ȵ�б���ȶ�
C����ͬ���ʵ�����������ȵ�б�������е�������
D����ʽ��ʾ����1 mol O2�еĹ��ۼ������յ��������γ�1 mol SO2�еĹ��ۼ����ų���������297.16 kJ
�ο��𰸣�B
����������٣��ڵã�S(s����б)=S(s������) ��H����0.33 kJ��mol��1��A�����֪��б��ת��Ϊ������ʱҪ�ų������������������Ҫ�ͣ����ȶ���B����ȷ����ͬ���ʵ�����������Ӧ�ñȵ�б�������е�����Ҫ�ͣ�C�����ʽ��ʾ����1 mol S��1 mol O2�еĹ��ۼ������յ��������γ�1 mol SO2�еĹ��ۼ����ų���������297.16 kJ��D�����
�����Ѷȣ�һ��
2��ѡ���� ��֪��ѧ��Ӧ2C��s��+O2��g��
2CO��g����2CO��g��+O2��g��2CO2��g�����Ƿ��ȷ�Ӧ���ݴ��ƶϣ�����˵������ȷ���ǣ���ͬ�����£���������
A��56g CO��32g O2���������������88g CO2�����������
B��12g C�����е�����һ������28g CO�����е�����
C��12g C��32g O2���������������44g CO2�����������
D��������̼ȼ�գ�����CO2�ķ�Ӧ������CO�ķ�Ӧ�ų���������
�ο��𰸣�A����2CO+O2�T2CO2�Ƿ��ȷ�Ӧ������56gCO��32gO2�����е�����������88gCO2�����е�������������Ӧ������������������������������A��ȷ��
B����2C+O2=2CO�Ƿ��ȷ�Ӧ������12gC��16gO2�����е�������һ������28gCO�����е�������������12g C�����е���������28g CO�����е���������B����
C����2C+O2��ȼ.2CO��2CO+O2��ȼ.2CO2���Ƿ��ȷ�Ӧ������C+O2��ȼ.CO2Ҳ�Ƿ��ȷ�Ӧ������12gC��32O2�����е�������һ������44gCO2�����е�����������C��ȷ��
D����������ȫȼ�շų��������Ȳ���ȫȼ�շų������࣬����һ��������̼ȼ�գ�����CO2������COʱ�ų��������࣬��D��ȷ��
��ѡB��
���������
�����Ѷȣ���
3��ѡ���� ����˵���������(? )
A����ʯȼ�����κ������¶���ȼ��
B����ʯȼ����ȼ�չ������ܲ�����Ⱦ������CO��SO2���к�����
C��ֱ��ȼ��ú���罫ú������ӹ�����ȼ�յ�Ч����
D������ú��Ϊ��̬ȼ�Ϻ�ȼ��Ч�ʽ�����
�ο��𰸣�AD
������������⿼��ȼ�ϳ��ȼ�յ���������Դ���ۺ����õ�֪ʶ�㡣
��ʯȼ��ֻ����һ�����¶Ⱥ��������ڵ�����²���ȼ�ա���ʯȼ�ϲ�����ӹ�����ֱ��ȼ�տɲ�����Ⱦ��CO��SO2���к����塣ú��ʯ�͵Ȼ�ʯȼ�Ͼ���ӹ����Ϊ����ȼ�ϣ�����������SO2�Դ�������Ⱦ�����������ȼ��Ч�ʣ�Ҳ�������͡�
�����Ѷȣ���
4��ѡ���� ��֪�����£�N2(��)��H2(��)����2mol NH3(��)�ų�92.4 kJ���������мס��������ݻ���ͬ�Һ��ݵ��ܱ��������ڳ����£������ܱ���������ͨ��1 molN2��3 mol H2���ﵽƽ��ʱ�ų�����Q1kJ�������ܱ���������ͨ��0.5 mol N2��1.5 mol H2���ﵽƽ��ʱ�ų�����Q2kJ�������й�ϵʽ��ȷ����(? )
A��Q1=2Q2=92.4
B��92.4 >Ql>2Q2
C��92.4=Q1>2Q2
D��92.4 >Q1=2Q2
�ο��𰸣�B
���������������ɵ��Ȼ�ѧ����ʽ��N2(��)+3H2(��)  2 NH3(��) ��H����92.4 kJ/mol . �����ܱ���������ͨ��1 molN2��3 mol H2�����ڸ÷�Ӧ�ǿ��淴Ӧ����Ӧ�ﲻ������ȫת��Ϊ��������Դﵽƽ��ʱ�ų�����Q1kJ<92.4 kJ��2�������ڷ�Ӧ�����ݻ���ͬ�Һ��ݵ��ܱ������н��С���ƽ�ⲻ�����ƶ����������ʵ���Ϊ�ٵ�һ�룬�ų�������Ҳ��ԭ����һ�롣�������ڸ÷�Ӧ������Ӧ�����������С�ķ�Ӧ�����ʵ������٣�ѹǿ��С������ƽ���ƶ�ԭ������Сѹǿ����ѧƽ�����淴Ӧ�����ƶ������Էų�������Ҫ��һ���١����������ϵΪ92.4 >Ql>2Q2����ѡ��ΪB��
2 NH3(��) ��H����92.4 kJ/mol . �����ܱ���������ͨ��1 molN2��3 mol H2�����ڸ÷�Ӧ�ǿ��淴Ӧ����Ӧ�ﲻ������ȫת��Ϊ��������Դﵽƽ��ʱ�ų�����Q1kJ<92.4 kJ��2�������ڷ�Ӧ�����ݻ���ͬ�Һ��ݵ��ܱ������н��С���ƽ�ⲻ�����ƶ����������ʵ���Ϊ�ٵ�һ�룬�ų�������Ҳ��ԭ����һ�롣�������ڸ÷�Ӧ������Ӧ�����������С�ķ�Ӧ�����ʵ������٣�ѹǿ��С������ƽ���ƶ�ԭ������Сѹǿ����ѧƽ�����淴Ӧ�����ƶ������Էų�������Ҫ��һ���١����������ϵΪ92.4 >Ql>2Q2����ѡ��ΪB��
�����Ѷȣ�һ��
5��ѡ���� ��ѧ��ӦA2��B2===2AB�������仯��ͼ��ʾ��������˵����ȷ����(����)
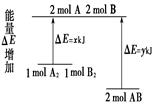
A���÷�Ӧ�����ȷ�Ӧ
B������1 mol A��A ����1 mol B��B ���ų�x kJ����
C������2 mol A��B ����Ҫ����y kJ������
D��2 mol AB������������1 mol A2��1 mol B2��������
�ο��𰸣�C
�������������ͼ�������ı仯��֪����Ӧ���������������������������������Ƿ��ȷ�Ӧ�����A��D������ȷ���ϼ������ȣ��γɻ�ѧ�����ܷ��ȣ�����ѡ��B����ȷ��C��ȷ����ѡC��
�����Ѷȣ�һ��