微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 根据酸碱质子理论,凡是能给出质子的分子或离子都是酸,凡是能结合质子的分子或离子都是碱。按照这个理论,下列微粒属于两性物质的是:
①HS-②CO32-③H2PO4-④NH3⑤H2S⑥CH3COOH⑦OH-⑧H2O⑨NO2- ⑩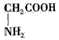
[? ]
A.①⑤
B.③⑥
C.①②⑨
D.①③⑧⑩
2、填空题 弱酸及其盐在水中存在着多种平衡关系。
(1)已知NaA水溶液呈碱性,常温下将0.10mol NaA和0.05 mol HCl溶于水,得到1L溶液。
①已知该混合溶液为弱酸性,则溶液中各离子浓度由大到小的顺序为________________;
②向上述混合液中再加入0.03mol NaOH,溶液中n(A-)+n(OH-)-n(H+)=________mol。
(2)二氧化碳在水中除了存在H2CO3和HCO3-的电离平衡外,还存在着如下平衡:人体血液的pH通常稳定在7.35~7.45之间,这是多种因素共同作用的结果。其中,血液中存在的H2CO3-NaHCO3环境是血液pH保持稳定的重要因素,据此回答。
①当c(H+)增大时,血液中消耗H+的离子方程式为___________________________;
②当c(OH-)增大时,血液的pH也能保持基本稳定,试结合电离方程式简要说明。
___________________________________
3、选择题 常温下,0.2mol/L?CH3COOH溶液与0.1mol/L?NaOH溶液等体积混合后(忽略混合前后溶液体积的变化),溶液的pH<7,则下列有关此溶液叙述正确的是( )
A.溶液中由水电离产生的H+浓度为1×10-7mol/L
B.c(CH3COOˉ)+c(CH3COOH)-c(Na+)=0.05mol/L
C.溶液中CH3COOH的电离程度小于CH3COONa的水解程度
D.溶液中离子浓度的大小关系为:c(Na+)>c(CH3COOˉ)>c(H+)>c(OHˉ)
4、选择题 下列各溶液中,微粒物质的量浓度关系正确的是( )
A.0.1mol?L-1Na2CO3溶液中:[OH-]=[HCO3]+[H+]>[C
]
B.0.1mol?L-1(NH4)2SO4溶液中:[S]>[N]>[H+]>[OH-]
C.0.1mol?L-1NaHCO3溶液中:[Na+]>[OH-]>[HC]>[H+]
D.0.1mol?L-1Na2S溶液中:[Na+]=2[S2-]+2[HS-]+2[H2S]
5、填空题 FeCl3的水溶液呈______(填“酸”、“中”、“碱”)性,原因是(用离子方程式表示):______,实验室在配制FeCl3的溶液时,常将FeCl3固体先溶于______中,然后再用蒸馏水稀释到所需的浓度,以______(填“促进”、“抑制”)其水解,否则得到的是浑浊的溶液.