微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法正确的是
A. O、
O、 O为不同的核素,有不同的化学性质
O为不同的核素,有不同的化学性质
B.根据分散系是否具有丁达尔效应,将分散系分为溶液、胶体和浊液
C.醋酸和硬脂酸互为同系物,C2H6和C9H20也一定互为同系物
D.在稀硫酸中加入铜粉,铜粉不溶解;再加入硝酸钠固体,铜粉仍不溶解
参考答案:C
本题解析:A、 O、
O、 O为不同的核素,核外电子数相同,有相同的化学性质,错误;B、根据分散系是否分散质粒子直径大小来分,错误;C、结构相似,通式相同,差若干个-CH2 -,正确 ;D、稀硫酸电离出的H+和硝酸钠电离出的NO3-相当于稀HNO3,铜粉溶于稀HNO3,错误。
O为不同的核素,核外电子数相同,有相同的化学性质,错误;B、根据分散系是否分散质粒子直径大小来分,错误;C、结构相似,通式相同,差若干个-CH2 -,正确 ;D、稀硫酸电离出的H+和硝酸钠电离出的NO3-相当于稀HNO3,铜粉溶于稀HNO3,错误。
本题难度:一般
2、选择题 废切削液中含2%―5%的NaNO2,直接排放会造成环境污染,下述试剂中能使其转化为无污染的N2的是
A.H2O2
B.NH4Cl
C.NaCl
D.浓H2SO4
参考答案:B
本题解析:由NaNO2 转化为N2 ,是利用了NaNO2 的氧化性,应找出具有还原性的物质与它反应,NH4Cl中的氮是最低价具有还原性,可以与NaNO2?反应生成氮气,H2O2、NaCl 的还原性比较弱不能反应,浓硫酸具有强氧化性也不可能。选B。
本题难度:一般
3、简答题 某同学将一定量铜粉与10mL的浓硫酸充分反应,生成的气体为1.12L(已换算为标准状况下).
(1)反应消耗铜的质量为______g.
(2)若往反应后溶液中滴加5mol?L-1NaOH溶液至铜离子恰好全部转变为Cu(OH)2沉淀,消耗NaOH?52mL,则原浓硫酸的浓度为______mol?L-1.
(3)测得原硫酸溶液的密度为1.8g?cm-3,则原硫酸的质量分数为______.
参考答案:(1)n(SO2)=1.12L22.4L/mol=0.05mol,
Cu+2H2SO4(浓)?△?.?CuSO4+SO2↑+2H2O
1?1
n(Cu)? 0.05mol
n(Cu)=0.05mol,
m(Cu)=0.05mol×64g/mol=3.2g,
故答案为:3.2;
(2)由反应H2SO4+2NaOH=Na2SO4+H2O,CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
可知:若往反应后溶液中滴加5mol?L-1NaOH溶液至铜离子恰好全部转变为Cu(OH)2沉淀,反应后溶液溶质为Na2SO4,
且n(Na2SO4)=12×n(NaOH)=12×0.052L×5mol/L=0.13mol,
则根据S元素守恒可知原浓硫酸溶液中:n(H2SO4)=n(Na2SO4)+n(SO2)=0.13mol+0.05mol=0.18mol,
则原浓硫酸的浓度为:c(H2SO4)=0.18mol0.01L=18mol/L,
故答案为:18;
(3)溶质的质量为:0.18mol×98g/mol=17.64g,
溶液的质量为:10ml×1.8g/ml=18g,
则原硫酸的质量分数为:17.64g18g×100%=98%,
故答案为:98%.
本题解析:
本题难度:一般
4、选择题 离子反应、复分解反应、置换反应和氧化还原反应之间可以用集合关系表示。
下列表示正确的是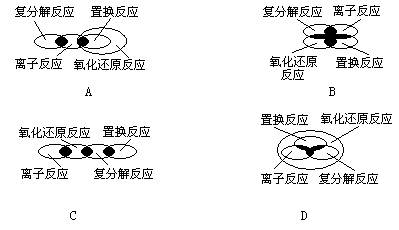
参考答案:A
本题解析:略
本题难度:简单
5、选择题 下列用来表示物质变化的化学用语中,正确的是
A.氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH-
B.电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2 ↑
C.表示乙炔“燃烧热”对应的热化学方程式:
C2H2(g)+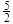 O2(g)=2CO2(g)+H2O(g) ?△H=-1 256 kJ/mol
O2(g)=2CO2(g)+H2O(g) ?△H=-1 256 kJ/mol
D.M与N是同素异形体,由M=N△H=+119 kJ/mol可知,N比M稳定
参考答案:B
本题解析:略
本题难度:简单