微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列每组各有三种物质,它们都不能用分液漏斗分离的是:
A.乙酸乙酯和水,酒精和水,苯和水;
B.二溴乙烷和水、溴苯和水、乙醛和水
C.硝基苯和苯、甲苯和苯、乙酸和乙醇;
D.甘油和水、油脂和水,已烷和汽油
参考答案:C
本题解析:A、乙酸乙酯和水不相溶,苯和水不相溶,可以用分液漏斗分离,酒精和水相溶,不能用分液漏斗分离,故A错误;
B、二溴乙烷和水不相溶,溴苯和水不相溶,乙醛和水相溶,不能用分液漏斗分离,故B错误;
C、硝基苯和苯相溶,甲苯和苯相溶,乙酸和乙醇相溶,不能用分液漏斗分离,故C正确;
D、甘油和水相溶,已烷和汽油相溶,不能用分液漏斗分离,油脂和水不相溶,可以用分液漏斗分离,故D错误。
故选C。
点评:本题考查学生物质分离方法中的分液法,熟记物质的溶解性是解题的关键,难度不大。
本题难度:简单
2、选择题 以下说法错误的是
A.摩尔是物质的量的单位,简称摩,符号为mol
B.1molNaOH的质量是40g
C.硫酸和磷酸的摩尔质量相等
D.硫酸的摩尔质量是98g
参考答案:D
本题解析:分析:A、摩尔是物质的量的单位.
B、根据m=nM计算氢氧化钠的质量.
C、摩尔质量在数值上等于其相对分子质量.
D、摩尔质量的单位是g/mol.
解答:A、物质的量是一定数量粒子的集合体,单位是摩尔,简称摩,符号为mol,故A正确.
B、m=nM=1mol×40g/mol=40g,所以1mol氢氧化钠的质量是40g,故B正确.
C、摩尔质量在数值上等于其相对分子质量,硫酸和磷酸的相对分子质量相等,所以硫酸和磷酸的摩尔质量相等,故C正确.
D、硫酸的摩尔质量是98g/mol,故D错误.
故选D.
点评:本题考查了物质的量的单位和摩尔质量,难度不大,明确摩尔只能用来计量微观粒子不能计量宏观物质.
本题难度:困难
3、选择题 阿伏加德罗常数值是NA,标准状况下,若某氧气和氮气的混合气体mg含有b个分子,则ng该混合气体在标准状况下的体积是
A.
B.
C.
D.
参考答案:A
本题解析:分析:正确理解气体摩尔体积,阿伏加德罗常数,先求出ng该混合气体含有的分子数,再求出其物质的量,最后根据气体体积公式求出体积.
解答:根据其组分及其含量相同,所以其质量与分子数成正比,设ng该混合气体含有的分子数为:x个,质量与分子数的比列式为:mg:b个=ng:x个,
x= =
= 个;?
个;?
ng该混合气体含有的物质的量为:n=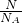 =
=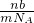 mol
mol
其体积为:V=n×Vm =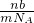 mol×Vm =
mol×Vm = L
L
故选:A
点评:本题考查的是物质的量、质量、气体摩尔体积之间的关系,灵活运用公式是解题的关键,这种类型的题在高考选择题中经常出现.
本题难度:困难
4、选择题 限用一种试剂, 经过一次性实验就能鉴别下列四种溶液:Na2CO3、(NH4)2SO4、NH4Cl、KNO3, 应选用:
A.AgNO3溶液
B.NaOH溶液
C.盐酸
D.Ba(OH)2溶液
参考答案:D
本题解析:硝酸银和前三种都反应生成白色沉淀,A不正确。氢氧化钠和铵盐反应,和碳酸钠、硝酸钾不反应,B不正确。又是只和碳酸钠反应,C不正确。氢氧化钡和碳酸钠反应产生白色沉淀,和硫酸铵反应生成白色沉淀和氨气,和氯化铵反应只生成氨气,和硝酸钾不反应,所以选项D正确,答案选D,
本题难度:简单
5、填空题 物质的分离提纯:
(1)下列各组混和物的分离提纯或是检验应采用什么方法?
①实验室中的石灰水久置,液面上常悬浮有CaCO3微粒.可用______的方法除去Ca(OH)2溶液中悬浮的CaCO3微粒.
②鉴别胶体和溶液的一般方法是______.
③除去乙醇中溶解的微量食盐可采用______的方法.
④从碘水中提取碘可采用______的方法.
⑤除去氧化钙中的碳酸钙可用______的方法.
(2)填表.
| 混合物(括号内为杂质) | 提纯用试剂 | 发生反应的离子方程式
Na2SO4(MgSO4)
______
______
KOH(Ba(OH)2)
______
______
NaCl(NaOH和Na2CO3)
______
______
参考答案:(1)①根据CaCO3的溶解性,是不溶于水的物质,要和石灰水分离,可以采用过滤的方法,故答案为:过滤;
②胶体具有丁达尔现象,溶液不能发生丁达尔现象,利用丁达尔现象鉴别溶液和胶体,故答案为:丁达尔效应;
③乙醇的沸点低,氯化钠的沸点高,可以利用蒸馏的方法分离出乙醇,故答案为:蒸馏;
④碘微溶于水,碘易溶于苯、四氯化碳等有机溶剂,且苯、四氯化碳与水互不相溶,可用萃取法分离,故答案为:萃取;
⑤碳酸钙受热分解为氧化钙、二氧化碳,而氧化钙受热稳定,故可以用加热分解法来分离,故答案为:加热分解;
(2)Na2SO4(MgSO4),杂质MgSO4可以和碱反应生成沉淀,加入NaOH溶液,过滤得到硫酸钠溶液;反应的离子方程式为:Mg2++2OH-=Mg(OH)2↓;
KOH(Ba(OH)2),杂质氢氧化钡中的钡离子可以用硫酸根离子除去,所以和硫酸钾溶液反应生成硫酸钡沉淀除去,同时生成氢氧化钾,过滤得到氢氧化钾溶液,反应离子方程式为:Ba2++SO42-=BaSO4↓;
NaCl(NaOH和Na2CO3),杂质可以加入盐酸到不再生成气体为止得到氯化钠溶液,反应的离子方程式为:OH-+H+=H2O;CO32-+2H+=CO2↑+H2O;
故答案为:
混合物(括号内为杂质)提纯用试剂发生反应的离子方程式Na2SO4(MgSO4)NaOH溶液Mg2++2OH-=Mg(OH)2↓KOH(Ba(OH)2)K2SO4溶液Ba2++SO42-=BaSO4↓NaCl(NaOH和Na2CO3)稀盐酸OH-+H+=H2O;CO32-+2H+=CO2↑+H2O
本题解析:
本题难度:一般
|