微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列微粒中,最外层是8个电子,并与Li+相差两个电子层的是( )
A.F-
B.Mg2+
C.S2-
D.Na+
参考答案:C
本题解析:
本题难度:简单
2、填空题 (选修三)【物质结构与性质】
(1)氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。写出铬元素的基态原子核外电子排布式:_________________;与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有_______(填名称);CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是______(填“极性”或“非极性”)分子。
(2)在①苯、②CH3OH、③HCHO、④H2S四种分子中,属于非极性分子的是___________,分子间能形成氢键的是___________(以上两空填序号);H2S分子的空间构型是_______,HCHO分子中σ键与π键的个数比是____________。
(3)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。 A和B的单质单位质量的燃烧热大,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如表所示:

①某同学根据上述信息,推断B元素基态原子的核外电子排布如图所示,该同学所画的电子排布图违背了________________,
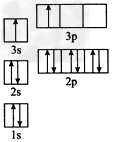
②根据等电子原理,推测A和氟元素形成的简单分子的等电子体有_______ (任写一个);
③根据对角线规则,A的化学性质与_____ 元素相似;试写出A与氢氧化钠溶液反应的离子方程式:_______________。
参考答案:(1)1s22s22p63s23p63d54s1{或[Ar]3d54s1};钾、铜;非极性
(2)①;②;角形(或V形或折线形);3:1
(3)①能量最低原理;②CO2、N2O、N3-;③Al(或铝);Be+2OH-=BeO22-+H2↑
本题解析:
本题难度:一般
3、选择题 与氖的核外电子排布相同的阴离子及阳离子所构成的化合物可能是( )
A.溴化镁
B.氧化钠
C.氯化钾
D.硫化钠
参考答案:B
本题解析:
本题难度:简单
4、填空题 某元素最外层只有1个电子,最高能层n=4。问:
(1)符合上述条件的元素,可以有_______个;原子序数分别为_____________。
(2)写出相应元素原子的电子排布式,并指出在周期表中的位置(周期、族)_____________。
参考答案:(1)3;19、24、29
(2)K、[Ar]4s1、第四周期IA族,Cr、[Ar]3d54s1、第四周期ⅥB族;Cu、[Ar]3d104s1、第四周期IB族
本题解析:
本题难度:一般
5、填空题 目前科学家们正在研究开发新型制冷剂,如“磁制冷剂”。已知磁制冷剂的原子中常具有较多的未成对电子,在磁场作用下,电子自旋方向从一致到不一致就会从环境吸热而制冷。美、中等国家已开始这方面的研究,并于2002年制成第一台磁冰箱。研究者最先采用的磁制冷剂是稀土金属钆(64Gd),我国有丰富的储藏。已知54号元素是Xe。请你帮助分析为什么电子自旋方向发生变化能制冷,写出稀土金属钆的核外电子排布式和轨道表达式,并确定未成对电子数。
__________________________________________
参考答案:1s22s22p63s23p63d104s24p64d104f75s25p65d16s2或[Xe] 4f75d16s2
其轨道表示式为:[Xe] 
未成对电子数为8个
本题解析:
本题难度:一般