��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ʵ�����������᳧����(��Ҫ�ɷ�Ϊ���������P����FeS��SiO2��)�Ʊ�����(��ʽ�������ľۺ���)���̷�(FeSO4��7H2O)����������£�
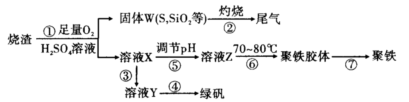
(1)���̢��У�FeS��O2��H2SO4��Ӧ�Ļ�ѧ����ʽΪ?��
(2)���̢��в�����β����Դ��������Ⱦ����ѡ�������Լ��е�?���ա�
a��ŨH2SO4? b������ˮ? c��NaOH��Һ? d��Ũ����
(3)���̢��У���Ҫ���������������?
(4)���̢ܵ�ʵ�������?
(5)���̢��У�����ҺZ���ȵ�70��80�棬Ŀ����?��
(6)ʵ����Ϊ�ⶨ���õ��ľ�����Ʒ����Ԫ�ص�������������������ʵ�顣���÷�����ƽ��ȡ��Ʒ2.700 g���ڽ���Ʒ����������������������Ȼ�����Һ���۹��ˡ�ϴ�ӡ�����������ù�������Ϊ3.495 g�����þ�����Ҫ�ɷ�Ϊ[Fe(OH)SO4]n����þ�������Ԫ�ص���������Ϊ?��
�ο��𰸣�
��1��4FeS+3O2+6H2SO4=2Fe2(SO4)3+6H2O+4S��2�֣�
��2��c��2�֣�?��3������2�֣�
��4��������Ũ����������ȴ���ᾧ�����ˡ�ϴ�ӣ�4�֣�Ũ������ȴ��д���Բ��۷֣�
��5���ٽ�Fe3+��ˮ�⣨2�֣�
��6��31.11%��3�֣�
���������
��1�����ݹ���W�ijɷ��д���S���Ƴ�FeS��O2��H2SO4����������ԭ��Ӧ��FeS����ԭ����O2����������������Fe2(SO4)3��S��H2O��
��2����Ⱦ����SO2���ü�Һ���ա�
��3����ҺX�е�����Fe3+���̷��е���ΪFe2+����Ӧ����Fe�ۣ���Fe3+��ԭΪFe2+��
��4�������γɽᾧˮ���������Һ���ܲ�ȡֱ�����ɵİ취��ȡ���塣
��5�������¶ȣ��ٽ�Fe3+��ˮ�⡣ ��6���۵õ��ij�����BaSO4��n(BaSO4) =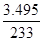 =0.015mol�����ݾ�����Ҫ�ɷ�Ϊ[Fe(OH)SO4] n���Ƴ�n(Fe3+)=0.015mol����m(Fe3+)=0.84g����Ԫ�ص���������:��(Fe)=(0.84g/2.700g)��100%=31.11%��
=0.015mol�����ݾ�����Ҫ�ɷ�Ϊ[Fe(OH)SO4] n���Ƴ�n(Fe3+)=0.015mol����m(Fe3+)=0.84g����Ԫ�ص���������:��(Fe)=(0.84g/2.700g)��100%=31.11%��
�����Ѷȣ�һ��
2��ѡ���� ���ж������ᡢ�������ʶ����ȷ����(?)
A��Ũ�����Ũ���ᶼ����������
B��ͭ��Ũ����ķ�Ӧ�����û���Ӧ
C����ͭ��Ũ����ķ�Ӧ�У�����ֻ�����������ԣ�û����������
D������������������ʢװϡ����
�ο��𰸣�A
��������������ѣ���������ᡢ����Ļ�ѧ���ʵ����⣬Ũ�����Ũ���ᶼ��ǿ�������ᣬ��ǿ�����Ա�����+6�۵�SԪ�ء�+5�۵�NԪ���õ����ϡ�ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽΪ��2H2SO4(Ũ) + CuCuSO4 + 2H2O + SO2������Ȼ�����û���Ӧ�����������ķ�Ӧ�У���������е�NԪ�صĻ��ϼ۽��������������ǿ�����ԣ���������е�NԪ�ز�û����ȫ����ԭ���ڷ�Ӧ�����л���NO3������������������ȱ����������ԣ������������ԡ�ͭ��Ũ���ᷴӦ�Ļ�ѧ����ʽΪ��Cu��4HNO3(Ũ)��Cu(NO3)2��2NO2����2H2O���ɿ�������ȱ����������ԣ������������ԡ��ڳ����£�Ũ�����Ũ������ʹ�������Ƚ����ۻ����ڽ����������γ�һ�����ܵ�����Ĥ�����������ڳ����¾�����ϡ���ᷴӦ�����Բ�����������������ʢװϡ���ᡣ
�����Ѷȣ�һ��
3������� ������ҵ�Դٽ����ú���ᷢչ������Ҫ���á�



 ��1��������¯��Ϊ�岿�֣�����ʯ�����ú����Ҫ��?���ַ�����Ӧ����?���ֿ�ʼ��������¯����
��1��������¯��Ϊ�岿�֣�����ʯ�����ú����Ҫ��?���ַ�����Ӧ����?���ֿ�ʼ��������¯����
 ��2������ʱ�����Ļ�ѧ����ʽΪ?��
��2������ʱ�����Ļ�ѧ����ʽΪ?��
 ����衢�̺�����Ŀ����?��
����衢�̺�����Ŀ����?��
 ��3������ֺ��е�CrԪ���������ֹ��̵�����?���ǰ�������룬ԭ����?��
��3������ֺ��е�CrԪ���������ֹ��̵�����?���ǰ�������룬ԭ����?��
 ��4�����������������У�β�������е���Ҫ��Ⱦ����?��
��4�����������������У�β�������е���Ҫ��Ⱦ����?��
 �ӻ����;��ýǶȿ��ǣ�����β��������������?��
�ӻ����;��ýǶȿ��ǣ�����β��������������?��
�ο��𰸣���1��¯��?¯��

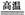 ��2��2P+5FeO+3CaO? Ca3(PO4)2+5Fe?�����͵����ֵijɷ�
��2��2P+5FeO+3CaO? Ca3(PO4)2+5Fe?�����͵����ֵijɷ�
 ��3����?����Cr��������������ǰ����Cr���γ�¯������ȥ����
��3����?����Cr��������������ǰ����Cr���γ�¯������ȥ����
 ��4��CO?ȼ�ϣ���ԭ����
��4��CO?ȼ�ϣ���ԭ����
��������� ��1����¯����������ʯ����Ҫ��Ӧ����¯�����ַ�������¯��������������¯����
��1����¯����������ʯ����Ҫ��Ӧ����¯�����ַ�������¯��������������¯����

 ��2�������е��Ļ�ѧ����ʽΪ2P+5FeO+3CaO? Ca3��PO4��2+5Fe������衢�̺�����Ŀ������ȥ���͵������еijɷ֡�
��2�������е��Ļ�ѧ����ʽΪ2P+5FeO+3CaO? Ca3��PO4��2+5Fe������衢�̺�����Ŀ������ȥ���͵������еijɷ֡�
 ��3��Ϊ�˷�ֹCrԪ�ر������µ���������Ӧ����������롣
��3��Ϊ�˷�ֹCrԪ�ر������µ���������Ӧ����������롣



 ��4������ʱ�õ�C��ȼ������CO����ԭ��������ʱ���б�������C����˶���CO��������CO���ж����壬�Ի�������Ⱦ��ͬʱCO����ȼ������CO2��
��4������ʱ�õ�C��ȼ������CO����ԭ��������ʱ���б�������C����˶���CO��������CO���ж����壬�Ի�������Ⱦ��ͬʱCO����ȼ������CO2��
�����Ѷȣ�һ��
4��ѡ���� Ϊ�ⶨijһ����ʯ��Ʒ�е���Ԫ�ص�����������ȡ3.702 g������ʯ(����Fe2O3��ʽ����,�������ʲ�����)����Ũ�������У�ϡ����250 mL������ȡ��25 mL��Һ�������´�������������İ�ˮ��ʹ����������������ʽ���������������ˣ�ϴ�������գ�ʹ֮��ȫת��Ϊ���������й�ʵ�����ݣ�����������15.286 1 g����һ�����պ����������������15.620 9 g���ڶ������պ����������������15.620 5 g�����������պ����������������15.620 5 g��������ʯ�е���Ԫ�ص���������Ϊ��?��
A��63.2%
B��90.3%
C��6.32%
D��34.4%
�ο��𰸣�A
���������������Ҫ����ʵ�����ݷ�����������������������һ�����պ����������������15.620 9 g�����ã�������������������15.620 5 g��15.286 1 g��0.334 4 g����������ʯ��Ʒ��Fe2O3��������3.344 g����Ԫ�ص�����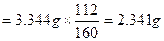 ����Ԫ�ص���������
����Ԫ�ص���������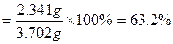 ��
��
�����Ѷȣ�һ��
5��ѡ���� ��Fe2(SO4)3��CuCl2�����Һ��Ͷ�����������۳�ַ�Ӧ�õ��Ĺ��徭���ˡ�������أ������ù�����������������۵�������ȣ���ԭ��Һ��c(SO42��)��c(Cl��)֮��Ϊ��
A��3�U14
B��1�U7
C��2�U7
D��3�U2
�ο��𰸣�A
������������ݷ���ʽ��2Fe2(SO4)3+2Fe="3" Fe2(SO4)3��������ȫ�ܽ⣬������������112g��? 14Fe+14CuCl2=14FeCl2+14Cu ��������������112g������c(SO42��)��c(Cl��)֮��Ϊ��6:28=3:14����ȷ��ΪA��
�����Ѷȣ�һ��