微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 实验室保存下列试剂,其中保存方法和理由描述都正确的是(? )
编号
| 试剂
| 保存方法
| 理由
|
A
| 钠
| 保存在煤油中
| 防止与空气中水、氧气接触发生反应
|
B
| 液溴
| 密封保存在细口瓶中
| 防止升华
|
C
| 浓硝酸
| 密封保存在铁器中
| 避免见光分解
|
D
| 烧碱
| 存放在磨口玻璃塞的广口瓶中
| 防止与空气中氧气接触被氧化
|
?
参考答案:A
本题解析:升华是固体直接变气体,液溴易挥发而不是升华,B错误;浓硝酸应保存在棕色试剂瓶中,C错误;烧碱不能被氧气氧化,烧碱易腐蚀玻璃,应用橡胶塞,D错误。
本题难度:简单
2、选择题 下列实验现象或结论错误的是
选项
| 实?验
| 现象或结论
|
A
| 取少量某溶液,滴加过量的稀盐酸无明显现象,再滴加BaCl2溶液
| 出现白色沉淀,则该溶液中含有SO42-
|
B
| 相同温度下,取两份等质量的锌粒分别与足量稀酸反应,向其中一份中加入几滴CuSO4溶液
| 加入ZnSO4溶液的产生氢气快,最终二者生成氢气的量相同
|
C
| 相同温度下,等质量的大理石与等体积、等浓度的盐酸反应
| 反应速率:粉状大理石>块状大理石
|
D
| 向Na2S溶液中滴入ZnSO4溶液有白色沉淀生成,再加入几滴ZnSO4溶液
| 沉淀由白色转化为黑色,说明溶度积(Ksp):ZnS>CuS
|
?
参考答案:B
本题解析: B项,滴加过 CuSO4溶液的样品由于一部分锌置换了CuSO4中的铜,形成原电池,使反应速率加快,但产生氢气的量减少。
本题难度:一般
3、简答题 (1)在烧杯或试管里进行固体物质的溶解时,为了加快溶解速度,常采用的方法有______、______、______等.
(2)根据实验测定硫酸铜晶体中结晶水含量的实验,填写以下空白.
①从以下仪器中选出所需仪器(用字母填写)______.
(A)托盘天平;(B)研钵;(C)试管夹;(D)酒精灯;(E)蒸发皿;(F)玻璃棒;(G)坩埚;(H)干燥器;(I)泥三角;?(J)石 棉网;(K)三角架;(L)药匙;?(M)坩埚钳.
②实验后得到以下数据:
a、加热前质量:W1(容器)=5.4g;W2(容器十晶体)=7.9g;
b、加热后质量:W3(容器十无水硫酸铜)=6.8g.
请写出结晶水含量--质量分数的计算式(用Wl、W2、W3表示):______
这一结果是偏高还是偏低?______.
③从下列分析中选出造成实验误差的原因可能是(填写字母)______.
A.加热前称量时容器未完全干燥 ? B.最后两次加热后质量相差较大(>0.1g)
C.加热后容器未放入干燥器中冷却 ?D.加热过程中晶体有少量溅失.
参考答案:(1)搅拌、升温都能加快水分子运动速度,也就能加快食盐与水的接触机会,从而加快了食盐的溶解速率,固体颗粒大小决定了固体与水的接触面积的大小,也能改变溶解速率,将固体研碎增加了固体与水的接触面积,也就加快了固体的溶解速率.故答案为:将固体研碎;加热;搅拌;
(2)①测定硫酸铜晶体(CuSO4?5H2O)里结晶水的含量,实验步骤为:①研磨?②称量空坩埚和装有试样的坩埚的质量?③加热?④冷却?⑤称量?⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止?⑦根据实验数据计算硫酸铜结晶水的含量.所需仪器是托盘天平、研钵、酒精灯、玻璃棒、坩埚、干燥器、泥三角、三角架、药匙、坩埚钳.
故答案为:ABDFGHIKLM;
②结晶水含量-质量分数=W2-W3W2-Wl;结晶水含量-质量分数=7.9g-6.8g7.9g-5.4g×100%=44%,而纯硫酸铜晶体中结晶水质量分数=5×(16+1×2)64+32+16×4+5×(16+1×2)×100%=36%,所以这一结果偏高;故答案为:W2-W3W2-Wl;偏高;
③A、加热前所用的容器未完全干燥.加热后水挥发,导致水的质量测定结果偏大,故A正确;
B、最后两次加热后质量相差较大说明结晶水还没有完全失去,会导致水测定结果偏小,故B错误;
C、加热后容器未放入干燥器中冷却会导致测定的水的质量偏小,故C错误;
D、加热过程中晶体有少量溅失会导致测定的水的质量偏大,故D正确.
故答案为:AD.
本题解析:
本题难度:一般
4、选择题 化工厂里运输浓硫酸的铝罐上经常贴有下列危险品标识,其中正确的是(?)

A.剧毒品
B.遇湿易燃物品
C.腐蚀品
D.有害品(远离食品)
参考答案:C
本题解析:略
本题难度:简单
5、选择题 由草木灰提取钾盐并检验钾元素存在的下列实验操作中,错误的是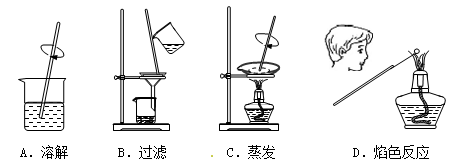
参考答案:D
本题解析:由草木灰提取钾盐的操作步骤为:溶解,过滤,蒸发;检验钾元素用焰色反应进行,但要透过蓝色的钴玻璃观察,若火焰呈紫色即有钾元素,否则没有;
本题难度:简单