| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ����ɡ��й�������ԭ��Ӧ�ļ��㡷��Ƶ������ѵ��2017�����°棩(��)
�ο��𰸣�D ���������A�����������Ӧ֪��Na2O2����Ԫ�ػ��ϼ���-1�۽�Ϊ-2�ۣ�����ԭ��Na2O2Ϊ������������B��Fe2O3����Ԫ�ػ��ϼ���+3������Ϊ+6�ۣ��ڷ�Ӧ��ʧȥ���ӣ�����C����Ӧ��Na2O2����Ԫ�ػ��ϼ���-1�۽�Ϊ-2�ۣ�3molNa2O2������Ӧ����6mol����ת�ƣ�����D��Na2FeO4��FeΪ+6�ۣ�����ǿ�����ԣ�������ɱ����������ȷ�� �����Ѷȣ�һ�� 4������� ��֪Cl2��70���NaOHˮ��Һ�У���ͬʱ������������������ԭ��Ӧ����Ӧ��ȫ������Һ��NaClO��NaClO3�����ʵ���֮��Ϊ4��1������49.7g?Cl2������ͨ�뵽����70���NaOHˮ��Һ�У���Ӧ��ȫ��õ�500mL��Һ�� �ο��𰸣���1���ڲ�ͬ�������£��������������Ƶķ�ӦΪ��Cl2+2NaOH=NaClO+NaCl+H2O��3Cl2+6NaOH���ȣ�=NaClO3+5NaCl+3H2O��Cl2��70���NaOHˮ��Һ�з�Ӧ������������Ӧ���ۺϹ��̣���������Ӧ��ӵã�4Cl2+6NaOH=NaClO+NaClO3+6NaCl+4H2O����Ӧ��ȫ������Һ��NaClO��NaClO3�����ʵ���֮��Ϊ4��1ʱ���Է���ʽ��ƽ��õ���7Cl2+14NaOH=4NaClO+NaClO3+9NaCl+7H2O���ʴ�Ϊ��7Cl2+14NaOH=4NaClO+NaClO3+9NaCl+7H2O�� ��������� �����Ѷȣ�һ�� 5������� ������������Դ�������ȷ������Ź㷺����;��ʪ�����ɷ��Ʊ��������ε�ԭ�����±���ʾ�� 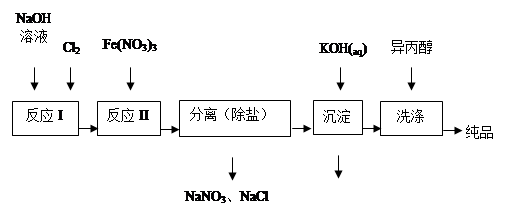 ��ϴ�Ӵ�Ʒʱѡ�������������ˮ�������ǣ� �� ��ϴ�Ӵ�Ʒʱѡ�������������ˮ�������ǣ� ���ڷ�ӦI�Ļ�ѧ����ʽΪ �� �۷�ӦII�����ӷ���ʽΪ �� ����֪25��ʱFe(OH)3��Ksp = 4.0��10-38����ӦII�����Һ��c(Fe3+)=4.0��10-5 mol/L,����Ҫ����pH= ʱ����ʼ����Fe(OH)3����������Һ����ı仯���� ��2��������ͼ�ɼ���ʪ���Ʊ��������ʱ�������Ƶø������ƣ�Ȼ��������������м��뱥��KOH��Һ����������������ء� �ټ��뱥��KOH��Һ��Ŀ���ǣ� �� ����������Ϣ��֪��������ص��ܽ�ȱȸ������� �����С������
��3���ɷ��Ʊ�K2FeO4�ķ�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ �� �ο��𰸣�����15�֣�����1����3��������ÿ��2�֣� ��������� �����Ѷȣ����� |
|
||
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | ||
| ��һƪ�����л�ѧ֪ʶ���ܽᡶ�й�������.. | ||
| �����Ŀ |