微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 LiFePO4新型锂离子电池因其原材料丰富、对环境友好、循环性能和安全性能好的特点,具有广阔的应用前景。已知该电池放电时的电极反应式为:
正极:FePO4+Li++e-=LiFePO4,负极:Li-e-=Li+,下列说法中正确的是
A.充电时阳极反应为Li++e-=Li
B.充电时动力电池上标注“-”的电极应与外接电源的负极相连
C.放电时电池内部Li+向负极移动
D.放电时,在正极上是Li+得电子被还原
参考答案:B
本题解析:充电时电源正极变为阳极,与外接电源的正极相连,A错,B正确;放电时负极:Li-e-=Li+,Li+向正极移动,C错,正极:FePO4+Li++e-=LiFePO4,Li的化合价不变,Fe的降低,故D不正确。
本题难度:简单
2、填空题 (15分)2013年以来,我国多地频现种种极端天气。二氧化碳、氮氧化物、二氧化硫是导致极端天气的重要因素。
(1)用钌的配合物作催化剂,一定条件下可直接光催化分解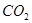 ,发生反应:
,发生反应: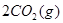 =2CO(g)+
=2CO(g)+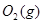 △H>0,该反应的
△H>0,该反应的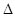 S 0(填“>”“<”或“=”),在低温下,该反应 (填“能”或“不能”)自发进行。
S 0(填“>”“<”或“=”),在低温下,该反应 (填“能”或“不能”)自发进行。
(2)活性炭可用于处理大气污染物NO。在1 L恒容密闭容器中加入0.100 mol NO和2.030 mol固体活性炭(无杂质),生成气体E和气体F。当温度分别在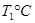 和
和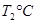 时,测得平衡时各物质的物质的量如下表:
时,测得平衡时各物质的物质的量如下表:
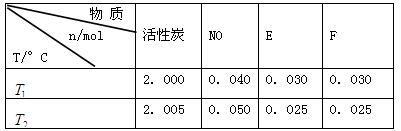
①请结合上表数据,写出NO与活性炭反应的化学方程式: 。
②上述反应在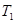 ℃时的平衡常数为
℃时的平衡常数为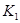 ,在
,在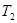 ℃时的平衡常数为
℃时的平衡常数为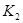 。
。
计算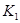 = 。根据上述信息判断,
= 。根据上述信息判断,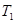 和
和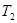 的关系是 。
的关系是 。
a.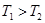 b.
b.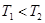 c.无法比较
c.无法比较
③在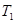 ℃下反应达到平衡后,下列措施不能改变NO的转化率的是____。
℃下反应达到平衡后,下列措施不能改变NO的转化率的是____。
a.增大c(NO) b.增大压强 c.升高温度 d.移去部分F
(3)碘循环工艺不仅能吸收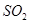 降低环境污染,同时又能制得氢气,具体流程如下:
降低环境污染,同时又能制得氢气,具体流程如下:

①用离子方程式表示反应器中发生的反应 。
②用化学平衡移动的原理分析,在HI分解反应中使用膜反应器分离出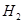 的目的是: 。
的目的是: 。
(4)开发新能源是解决大气污染的有效途径之一。直接甲醇燃料电池(简称DMFC)由于结构简单、能量转化率高、对环境无污染,可作为常规能源的替代品而越来越受到关注。DMFC工作原理如图所示:
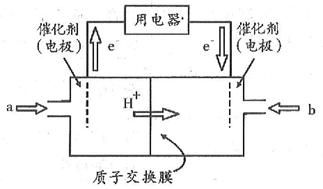
通过a气体的电极是原电池的 极(填“正”或“负”),其电极反应式为 。
参考答案:(15分)
(1) > 不能
(2)①C+2NO=N2+CO2 ②9/16 C ③a、b
(3) ①SO2+I2+2H2O = SO42-+2I-+4H+ ②降低生成物的浓度,使平衡向正方向移动
(4) 负 CH3OH-6e-+H2O = CO2 +6H+
本题解析:(1)根据化学反应可知,该反应是熵增的化学反应,所以△S>0,根据反应自发进行的判据,△ H-T△S<0反应能自发进行,该反应是熵增的吸热反应,在低温下不能自发进行。
(2)①根据活性炭可用于处理大气污染物NO,说明两者反应生成氮气和CO2,反应的化学方程式为C+2NO=N2+CO2;
②根据表格提供的信息,上述反应在T1℃时的平衡常数为K1(0.030×0.030)÷(0.040×0.040)=9/16,根据上述信息,没有温度大小,没有反应的热效应,无法比较T1和T2的关系,选c;③a.增大c( NO),相当于增大压强,平衡不移动,不能增大NO的转化率,b.该反应是反应前后气体体积不变的化学反应,增大压强,平衡不移动,不能增大NO的转化率,c.如果该反应是吸热反应,升高温度,平衡正向移动,能增大NO的转化率, d.移去部分F,平衡右移,能增大NO的转化率,选a、b。
(3)①根据流程图可知,SO2通入碘水中生成硫酸和氢碘酸,则反应器中发生反应的离子方程式为:SO2+I2+2H2O = SO42-+2I-+4H+,②根据化学反应2HI(g) I2(g)+H2(g),分离出H2,降低生成物的浓度,使平衡向正方向移动,加速碘的生成。
I2(g)+H2(g),分离出H2,降低生成物的浓度,使平衡向正方向移动,加速碘的生成。
(4)根据甲醇燃料电池的工作原理图可知,在a电极,失去电子,且H+由左向右迁移,所以a电极是负极,甲醇在负极失电子生成CO2和水,则电极反应式为CH3OH-6e-+H2O = CO2 +6H+。
考点:考查化学反应自发进行的判断,SO2污染的工业治理及甲醇燃料电池。
本题难度:困难
3、选择题 以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是
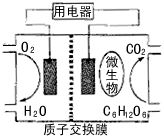
[? ]
A.该电池能够在高温下工作
B.电池的负极反应为:C6H12O6+6H2O-24e-→6CO2↑+24H+
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1mol氧气,理论上能生成标准状况下CO2气体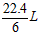
参考答案:B
本题解析:
本题难度:一般
4、选择题 下列电池工作时,O2在正极放电的是

参考答案:B
本题解析:氢氧燃料电池,氧气在正极通入,氢气在负极通入,故答案选B,
考点:燃料电池
本题难度:简单
5、选择题 LiFePO4新型锂离子动力电池是奥运会绿色能源的新宠。已知该电池放电时的电极反应式为:正极
FePO4+Li++e-==LiFePO4,负极 Li-e-==Li+下列说法中正确的是
[? ]
A.充电时电池反应为FePO4+Li = LiFePO4
B.充电时动力电池上标注“+”的电极应与外接电源的正极相连
C.放电时电池内部Li+向负极移动
D.放电时,在正极上是Li+得电子被还原
参考答案:B
本题解析:
本题难度:一般