��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ȼ�ϵ�������ں���ɻ�����30% KOH��ҺΪ�������Һ�����ֵ����ʹ��ʱ�ĵ缫��Ӧ���£�2H2+4OH-4e-=4H2O?O2+2H2O+4e-=4OH-�ݴ������жϣ�����˵���д������
[? ]
A��H2�ڸ�������������Ӧ
B������ʱ���ܷ�ӦΪ��2H2+O2=2H2O
C������Ϊ����Ⱦ��ˮ�����ڻ����Ѻõ��
D��ȼ�ϵ�ص�����ת���ʿɴ�100%
�ο��𰸣�D
���������
�����Ѷȣ�һ��
2������� ��10�֣���ѧ�ܺ͵��ܵ��ת����������ת������Ҫ��ʽ֮һ����ͼ����ʵ��װ����ʵ�ֻ�ѧ�ܺ͵����ת����װ�á�
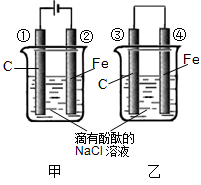
��1���ѻ�ѧ��ת��Ϊ���ܵ�װ����?����ס����ҡ�����
��2���ܵ缫�ϵĵ缫��ӦʽΪ?
��3���ٵ缫�ϵĵ缫��ӦʽΪ??��
����õ缫��Ӧ����ķ�����?
(4)д��װ�üķ�Ӧ�ܻ�ѧ����ʽ??��
�ο��𰸣��ң���2��Fe �C 2e- = 2Fe2+? (3) 2Cl- 2e- = Cl2����ʪ��ĵ���KI��ֽ���飬������ɫ��Ϊ����
��4��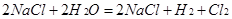 ��
��
�����������1���ѻ�ѧ��ת��Ϊ���ܵ�װ����ԭ��أ�����װ�ã�
��2����װ��Ϊԭ���װ�ã��۵缫Ϊ���������������һ����������ԭ��Ӧ�����ܵ缫�ǵ���������һ��������������Ӧ���缫��Ӧ����ʽΪ��Fe �C 2e- = 2Fe2+��
��3����װ��Ϊ����װ�ã��ٵ缫Ϊ������ʧȥ���ӵ�һ��������������Ӧ���缫��ӦʽΪ��2Cl- 2e- = Cl2��������õ缫��Ӧ����ķ�������ʪ��ĵ���KI��ֽ���飬������ɫ��Ϊ������
��4��д��װ�üķ�Ӧ�ܻ�ѧ����ʽΪ��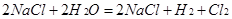
�����Ѷȣ���
3������� �ݱ��������Ħ��������˾�з���һ���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ������ɴ�����ʹ�õ������ػ�﮵�ص�ʮ����������ʹ��һ���²ų�һ�ε磮���ط�ӦΪ��2CH3OH+3O2+4OH-
2C+6H2O����
��1���ŵ�ʱ�缫��Ӧ����ʽ������______������______��
��2�����ʱ�������Һ��pH��______��������С�������ʱÿ����1molCH3OHת��______?mol���ӣ�
�ο��𰸣���1���ŵ�ʱ���൱��ԭ��صĹ���ԭ�������������������õ��ӵĻ�ԭ��Ӧ����O2+2H2O=4OH-+4e-�������Ǽ״�����ʧ���ӵ�������Ӧ����CH3OH+8OH-=6H2O+CO32-+6e-���ʴ�Ϊ��O2+2H2O=4OH-+4e-��CH3OH+8OH-=6H2O+CO32-+6e-��
��2�����ʱ���൱�ڵ��صĹ���ԭ�������ݷ�Ӧ����ʽ���ִ�ʱ���������������ӣ����Ե������Һ��pH������ÿ����2molCH3OHת�Ƶ���12mol�����Գ��ʱÿ����1molCH3OHת��6mol���ӣ��ʴ�Ϊ������6��
���������
�����Ѷȣ���
4��ѡ���� Ǧ��ɳ�������ִ��������й㷺Ӧ�ã����ij�ŵ練Ӧ����ʽ���У�
2PbSO4+2H2O  ?Pb+PbO2+2H2SO4�������жϲ���ȷ���ǣ�?��
?Pb+PbO2+2H2SO4�������жϲ���ȷ���ǣ�?��
A�����������Ϊ���أ��ŵ������Ϊԭ���
B�����ʱ��PbSO4������ת��ΪPbO2
C���ŵ�ʱ��Pb��Ϊ����
D���ŵ�ʱ��PbO2������ԭ��Ӧ
�ο��𰸣�B
���������Ǧ�����зŵ��൱��ԭ��أ�����൱�ڵ��أ�A��ȷ�����ݷ�Ӧʽ��֪�����ʱ�����ǵõ����ӵģ�����PbSO4������ת��ΪPb��B����ȷ��ԭ����и���ʧȥ���ӣ�����������Ӧ�������õ����ӣ�������ԭ��Ӧ�����ѡ��CD������ȷ�ģ���ѡB��
�����Ѷȣ���
5��ѡ���� ��ͼװ���У�AΪǦ���أ�C1��C2Ϊʯī�缫��B�ձ�����Ũ�Ⱦ�Ϊ0.1mol/L��H2SO3��KI�Ļ����Һ100mL������˵����ȷ����?
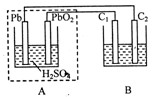
A��Ǧ���ع���һ��ʱ���A����Һ��PH��С
B����B�ձ���I-��Ũ�Ƚ�Ϊ0.05mol/Lʱ��A�����ĵ�
H2SO3�����ʵ���Ϊ0.025mol
C����C1��C2��������ʼ��������ʱ����������3.6��1022�����Ӵӵ�·������
D��Ǧ���ع���ʱ�������缫��ӦʽΪ��PbO2��2e -+ H2SO3 ��PbSO4+2H2O +SO42-
�ο��𰸣�B
�����������
�����Ѷȣ���