��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����һ������̼��Ԫ�ص���(? )
A�����ѵõ�����Ҳ��ʧ���ӵ�ԭ��
B�����γ�RO2��Ԫ��
C���������ˮ���ﻯѧʽΪH2RO3��Ԫ��
D���������������۾���ֵ�IJ�Ϊ���Ԫ��(H����)
�ο��𰸣�D
������������⿼��̼��Ԫ�ؼ��仯��������ʺ�����ص㣬ͬʱ����˼ά�������Ժ�ȷ�ԡ�ϡ������Ԫ�ص�ԭ�Ӳ����ѵõ��Ӷ�����ʧ���ӣ������ǵڢ�A�壬��ѡ��A�������γ��������һ�ѧʽΪRO2���еڢ�A����A����A�IJ���Ԫ�أ���SO2��NO2�ȣ�����ѡ��BҲ������Ԫ��Ҳ���γɻ�ѧʽΪH2RO3�������ˮ�������Ԫ�ز����ǵڢ�A��Ԫ�أ���ѡ��ؼ���û�н���������������Ӧ��ˮ�����ѡ��CҲ�Ǵ���ģ��ڢ�A��Ԫ�ص��������Ϊ+4�������Ϊ-4������ֵ�IJ�Ϊ�㣬��ѡ��D��ȷ��
�����Ѷȣ���
2��ѡ���� ���������������������ԭ����(? )
A��������ˮ����Ӧ����
B������Ӧ��ˮ�����ǿ�����ǿ��
C������ǿ����Һ��Ӧֻ�����κ�ˮ
D�����Ƿǽ���������
�ο��𰸣�C
���������������������ָ�ܹ���Ӧ�����κ�ˮ�����������2NaOH+SiO2�T�TNa2SiO3+H2O������˵SiO��Դ:91������ 91Exam.org2�����������
�����Ѷȣ���
3��ѡ���� ������ѧ�����л����Ӻ�������״����C60�״��Ƴ��ˡ����׳���(��ͼ)��ÿ�������׳�������һ���л����Ӻ�4��������״���ӡ���װ�����ɡ������׳��������������䵥�����л����ӣ��������ӵIJ��Ϻ�ҩ���Ϊ�������������е����ù��ߡ�����˵����ȷ����
A�����ǿ���ֱ�������������ؿ������֡����׳������˶�
B�������׳����ĵ�����˵��������ݷ��ӵļ�������һ���½�
C��C60��һ�����ͻ�����
D��C60�۵�Ƚ��ʯ�۵��
�ο��𰸣�B
���������A��������������Ϊ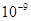 �ף��������۹۲죻B��ȷ��C����C60��һ�ֵ��ʣ�D����C60�Ƿ��Ӿ��壬�����ʯ��ԭ�Ӿ��壬ԭ�Ӿ�����۵���ڷ��Ӿ��壻
�ף��������۹۲죻B��ȷ��C����C60��һ�ֵ��ʣ�D����C60�Ƿ��Ӿ��壬�����ʯ��ԭ�Ӿ��壬ԭ�Ӿ�����۵���ڷ��Ӿ��壻
�����Ѷȣ�һ��
4������� ��5�֣��밴Ҫ��ش���������:
��1��ʢ���ռ�Һ���Լ�ƿ�����ò���������Ϊ�˷�ֹ����?��Ӧ���û�ѧ����ʽ��ʾ������ʹƿ����ƿ��ճ��һ��;
��2�����ȷ�Ӧ�ڹ�ҵ�����е���Ҫ��;֮һ��?;
��3���� ����ϡ��ֱ���Ϊ��Ϣ���ϡ����й㷺���ڹ��ά�IJ�����?���ѧʽ����ͬ�����㷺�������켯�ɵ�·�IJ�����?;
�ο��𰸣�
��1��SiO2 + 2NaOH = Na2SiO3 + H2O��2�֣�
��2�����Ӹֹ죨��ұ�����۽��������ƻ����������𰸣���1�֣�
��3��SiO2?��1�֣�? Si ��1�֣�
�����������
�����Ѷȣ���
5�������� ��10�֣�����SiO2��ʯ��ʯ5 g��0.267 L 0.5 mol��L-1�����ᷴӦ������CO2�ڱ�״���µ����Ϊ1 064 mL��
(1)Ҫ�к�ʣ������ᣬ��1 mol��L-1��NaOH��Һ��������ٺ�����
(2)�������ֲ�����ʯ��ʯ1 t������������������Ƕ��٣�
�ο��𰸣�(1)38.5 mL? (2)0.582 t
���������CO2�����ʵ���Ϊ1.064 L/22.4 L��mol-1="0.047" 5 mol����5 gʯ��ʯ��̼��ƣ�0.047 5 mol��100 g��mol-1="4.75" g���������0.047 5 mol��2="0.095" mol��ʣ�����0.267 L��0.5 mol��L-1-0.095 mol="0.133" 5 mol-0.095 mol="0.038" 5 mol��Ҫ�к�ʣ������ᣬ��1 mol��L-1��NaOH��Һ�����Ϊ0.038 5 mol/1 mol��L-1="0.038" 5 L="38.5" mL���������ֲ�����ʯ��ʯ1 t�����������������Ϊ1 t��[(5-4.75)/5]+1 t��(4.75/5)��(56/100)="0.582" t��
�����Ѷȣ���