微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (6分) 氯气在生产生活中应用广泛。
(1)工业上可用MnSO4溶液吸收氯气,获得Mn2O3,Mn2O3广泛应用于电子工业、印染工业等领域。请写出该化学反应的化学方程式 。
(2)海底蕴藏着丰富的锰结核矿,其主要成分是MnO2 。1991年由Allen等人研究,用硫酸淋洗后使用不同的方法可制备纯净的MnO2,其制备过程如下图所示:
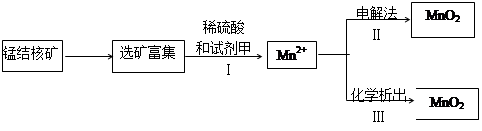
①步骤I中,试剂甲必须具有的性质是 (填序号)。
a. 氧化性 b.还原性 c.酸性
②步骤Ⅲ中,以NaClO3为氧化剂,当生成0.050 mol MnO2时,消耗0.10 mol・L-1的NaClO3溶液200 mL ,该反应的离子方程式为________________。
参考答案:(1) 2MnSO4+Cl2+3H2O="=" Mn2O3+2H2SO4+2HCl(2分)
(2)① b(1分)
② 2ClO3-+5Mn2++4H2O=5MnO2+Cl2↑+8H+(3分)
本题解析:(1) 氯气与MnSO4溶液反应,氯气作为氧化剂,MnSO4被氧化为Mn2O3,方程式为:2MnSO4+Cl2+3H2O="=" Mn2O3+2H2SO4+2HCl;
(2)MnO2具有强氧化性,转化为锰离子,说明加入的物质具有还原性;当把锰离子转化为二氧化锰,生成0.050 mol MnO2,失去0.1mol电子,消耗0.020 molNaClO3,得到0.1mol电子,则1个NaClO3得到5个电子,即1个Cl降低5价,生成的应该是Cl2,反应如下:2ClO3-+5Mn2++4H2O=5MnO2+Cl2↑+8H+。
考点:考查氧化还原反应方程式书写及计算。
点评:根据题给信息书写氧化还原反应方程式是学生的难点,本题难度较大。
本题难度:困难
2、选择题 等质量的下列烃完全燃烧,消耗O2最多的是( )
A.C3H6
B.C2H6
C.C6H6
D.C3H8
参考答案:B
本题解析:
本题难度:简单
3、选择题 下列化学用语正确的是
A.甲醇钠的结构式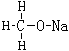
B.羟基的电子式
C.碳-12原子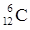
D.乙烯的结构简式 H2C=CH2
参考答案:D
本题解析:甲醇钠中存在的是阴阳离子,不可能是O―Na共价键;羟基中氧原子外层是7个电子;碳-12原子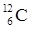 ,故选D
,故选D
本题难度:一般
4、选择题 下列物质的工业生产过程中,其主要反应不涉及氧化还原反应的是?
A.氨气
B.漂白粉
C. 烧碱
烧碱
D.纯碱
参考答案:D
本题解析:略
本题难度:简单
5、选择题 下列化学用语使用正确的是?(?)
A.Na2O2的电子式:Na:O::O:Na
B.表示中和热的热化学方程式:NaOH+HC1=NaC1+H2O △H="―" 57.3kJ/mol
C.苯酚钠溶液中通入CO2的离子方程式:C6H5O―+CO2+H2O=C6H5OH+HCO3―
| | |
D.CH3―CH―CH―CH―CH3的名称:2―甲基―3,4―二乙基戊烷CH3 CH3C2H5
参考答案:C
本题解析:略
本题难度:一般