微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、计算题 将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:3A(g)+B(g)  xC(g)+2D(g),经5min后,测得D的浓度为0.5 mol·L-1,C的平均反应速率是0.1 mol·L-1·min-1,且c(A)﹕c(B)=3﹕5。求:
xC(g)+2D(g),经5min后,测得D的浓度为0.5 mol·L-1,C的平均反应速率是0.1 mol·L-1·min-1,且c(A)﹕c(B)=3﹕5。求:
⑴、此时A的浓度c(A)=?____ mol·L-1;
⑵、反应开始前放入容器中B物质的量n(B)=?____ mol;
⑶、B的平均反应速率v(B)=?___ mol·L-1·min-1;
⑷、x=?____ 。
参考答案:⑴、c(A)= 0.75 mol·L-1?
⑵、n(B)=?3?mol
⑶、v(B)=?0.05?mol·L-1·min-1?
⑷、x=?2
本题解析:
本题难度:一般
2、选择题 一定温度下,在一密闭容器中加入1molPCl5,发生反应PCl5(g) PCl3(g)+Cl2 (g)充分反应平衡后,测得PCl5的分解率为a%, 此时,再向密闭容器中加入1mol PCl5 ,充分反应,再次平衡后,下列有关说法正确的是(?)
PCl3(g)+Cl2 (g)充分反应平衡后,测得PCl5的分解率为a%, 此时,再向密闭容器中加入1mol PCl5 ,充分反应,再次平衡后,下列有关说法正确的是(?)
A.PCl5的分解率大于a%
B.PCl5的分解率小于a%
C.达到平衡后正逆反应速率比原平衡状态时大
D.达到平衡后正逆反应速率比原平衡状态时小
参考答案:BC
本题解析:因为反应物只有一种,增加反应物的量,都相当于是增大压强,平衡将向条件减小的方向移动。所以PCl5的分解率降低,但由于浓度增大,因此反应速率将加快。所以正确的答案是BC。
本题难度:一般
3、选择题 已知某物质颜色的强度与该物质的浓度成正比、与观察者的视程中的物质厚度成正比。在注射器中,存在NO2与N2O4的混合物,气体呈棕色,现将注射器的针筒慢慢往外拉,保持温度不变,此时混合物的颜色为

A.从针筒的顶端方向观察,气体颜色变深
B.从针筒的顶端方向观察,气体颜色变浅
C.从针筒的垂直方向观察,气体颜色没有变化
D.从针筒的垂直方向观察,气体颜色变深
参考答案:A
本题解析:NO2为红棕色气体,N2O4无色
对于可逆反应2NO2 N2O4,向外拉针筒时,相当于减压,平衡逆向移动,生成更多的NO2(但两物质的浓度是减小的)。
N2O4,向外拉针筒时,相当于减压,平衡逆向移动,生成更多的NO2(但两物质的浓度是减小的)。
故从针筒的顶端方向观察,NO2的浓度减小,但厚度增大,总体来说,气体颜色加深;但从针筒的垂直方向观察,NO2的浓度减小,厚度不变,气体的颜色变浅,答案为A
本题难度:一般
4、计算题 (7分)某固定容积的2L密闭容器中进行反应 :?起始时加入的N2、H2、NH3均为2mol,5min后反应达到平衡, NH3的物质的量为3mol,求:
:?起始时加入的N2、H2、NH3均为2mol,5min后反应达到平衡, NH3的物质的量为3mol,求:
(1)这5分钟内用N2来表示该反应的反应速率(请写出计算过程,下同)
(2)求平衡时H2的物质的量浓度
(3)平衡时容器的压强为初始时的几分之几?
参考答案:(1)(2分)0.05mol/(L·min)?
(2)(2分)0.25mol/L
(3)(3分)5/6
本题解析:略
本题难度:简单
5、选择题 N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)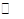 4NO2 +O2(g)△H>0,T1温度下的部分实验数据为:
4NO2 +O2(g)△H>0,T1温度下的部分实验数据为:
t/s
| 0
| 500
| 1000
| 1500
|
c(N2O5)mol/L
| 5.00
| 3.55
| 2.50
| 2.50
|
?
下列说法中,正确的是:
A.当反应体系内气体的平均相对分子质量不再发生变化时则该反应达到了平衡
B.T1温度下的平衡常数为K1=125,500s时N2O5的转化率为71%:
C.其他条件不变时,T2温度下反应到2000s时测得N2O5 (g)浓度为2.78mol/L, 则T1<T2
D.T1温度下的平衡常数为K1,若维持T1温度不变,增加体系压强,达到新的平衡时,平衡常数为K2,则K2>K1
参考答案:A
本题解析:? 2N2O5(g)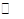 4NO2 +O2(g)△H>0
4NO2 +O2(g)△H>0
C始(mol/L)? 5.00? 0? 0
C改变(mol/L)? 2.50? 5.0? 2.5
C末(mol/L)? 2.50? 5.0? 2.5
B.T1温度下的平衡常数为K1= =250,500s时N2O5的转化率为
=250,500s时N2O5的转化率为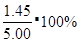 =29%:C.其他条件不变时,T2温度下反应到2000s时测得N2O5 (g)浓度为2.78mol/L,根据勒夏特列原理,应该采用了降温措施, T1>T2;D.化学平衡常数只跟温度有关,温度不变,化学平衡常数不变。
=29%:C.其他条件不变时,T2温度下反应到2000s时测得N2O5 (g)浓度为2.78mol/L,根据勒夏特列原理,应该采用了降温措施, T1>T2;D.化学平衡常数只跟温度有关,温度不变,化学平衡常数不变。
本题难度:一般