��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� I. һ�������£������Ϊ3 L���ܱ������У�һ����̼��������Ӧ���ɼ״�������ΪCu2O/ZnO����CO��g����2H2��g��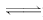 CH3OH��g����
CH3OH��g����
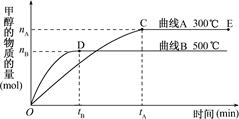
�������������ͼ��������и��⣺��Ӧ�ﵽƽ��ʱ��ƽ�ⳣ������ʽK��?��
��2�������¶ȣ�Kֵ??���������С�����䡱����
II. ���淴Ӧ��aA��g��+ bB��g��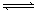 cC��g��+ dD��g��������ͼ�ش�
cC��g��+ dD��g��������ͼ�ش�
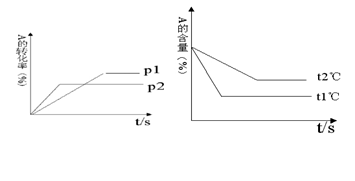
��1��ѹǿ P1��P2?������С������2����a +b���ȣ�c +d��?������С����
��3���¶�t1���t2��?�����ͣ�����4������ӦΪ?��Ӧ��
�ο��𰸣�I��1�� ����2����С?II��1��С��2��С?��3���ߣ�4������
����2����С?II��1��С��2��С?��3���ߣ�4������
���������I.��1����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը��ݷ���ʽ��֪ƽ�ⳣ������ʽK�� ��
��
��2������ͼ���֪���¶�Խ�ߣ��״������ʵ���Խ�٣���˵�������¶�ƽ�����淴Ӧ�����ƶ������������¶�ƽ�ⳣ����С��
II��1��ѹǿΪP2ʱ���ȴﵽƽ��״̬������ѹǿ P1��P2С��
��2��ѹǿ�ߣ���Ӧ���ת���ʵͣ���˵������ѹǿƽ�����淴Ӧ�����ƶ�����������Ӧ���������Ŀ��淴Ӧ����a +b���ȣ�c +d��С��
��3���¶�Ϊt1ʱ���ȴﵽƽ��״̬�����¶�t1���t2��ߡ�
��4���¶ȸ߷�Ӧ���ת���ʵͣ���˵�������¶�ƽ�����淴Ӧ�����ƶ�����������Ӧ�Ƿ��ȷ�Ӧ��
�������������е��Ѷȵ����⣬���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ��������Ĺؼ�����ȷ��Ӧ���ʺ�ƽ�ⳣ���ĺ����Լ�Ӱ�����أ�Ȼ������ͼ��ͷ���ʽ���������������ԭ���жϼ��ɡ�����������ѧ�������������������ѧ�����������ɡ��ܽ������������
�����Ѷȣ�һ��
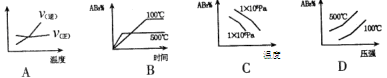
2��ѡ���� ���ڿ��淴Ӧ2AB3(g)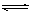 A2(g) +3B2(g)������Ӧ���ȣ�����ͼ����ȷ����
A2(g) +3B2(g)������Ӧ���ȣ�����ͼ����ȷ����
�ο��𰸣�B
����������ӷ���ʽ�ɿ������ÿ��淴Ӧ������Ӧ��һ�����������������ȷ�Ӧ��������������ԭ��������ѹǿ����ѧƽ�����淴Ӧ�����ƶ��������¶ȣ���ѧƽ��������Ӧ�����ƶ��������¶ȣ���ѧ��Ӧ���ʼӿ죬�ﵽ��ѧƽ����Ҫ��ʱ���Խ�١�Aͼ���淴Ӧ��ƽ��������¶ȣ�����V(��)��v(��)����ѧƽ�����淴Ӧ�����ƶ���������Ŀ������Ӧ������Υ��������B�����¶ȣ���ѧƽ��������Ӧ�����ƶ�����Ӧ���ת����Խ�ߣ��ﵽƽ��ʱ���ĺ�����Խ�٣���ȷC����ѹǿ����ѧƽ�����淴Ӧ�����ƶ��� AB3Ӧ��Խ�࣬��ѡ����ѹǿ��ʱ��Ӧ�����ƽ��ʱ���������٣�����Dͼ �����¶ȣ�ƽ��ʱ��Ӧ��ĺ�����Խ�ߣ����뻯ѧƽ��������ʱ������Ӧ�����ƶ���Υ��������
�����Ѷȣ�һ��
3������� ij��ѧ��Ӧ2A (g) �P B(g) + D(g) ��4�ֲ�ͬ�����½��У�B��D����ʼŨ��Ϊ0 ����Ӧ��A ��Ũ��(mol?L-1) �淴Ӧʱ�� (min) �ı仯������±���?
?
ʵ��
���
|  Ũ�� Ũ��
ʱ��
�¶�
| 0
| 10
| 20
| 30
| 40
| 50
| 60
|
1
| 800��
| 1.0
| 0.80
| 0.67
| 0.57
| 0.50
| 0.5 0 0
| 0.50
|
2
| 800��
| 1.0
| 0.60
| 0.50
| 0.50
| 0.50
| 0.50
| 0.50
|
3
| 800��
| C3
| 0.92
| 0.75
| 0.63
| 0.60
| 0.60
| 0.60
|
4
| 820��
| 1.0
| 0.40
| 0.25
| 0.20
| 0.20
| 0.20
| 0.20
|
�����������ݣ����������գ�
��1��ʵ��1�ﵽƽ���ʱ����?min��ʵ��4�ﵽƽ���ʱ����?min��C3??1.0 mol?L-1���< ������ > ���� = �� ����
��2��ʵ��4��ʵ��1�ķ�Ӧ����?����족����������ԭ����?��
��3�����2A (g) �P B(g) + D(g) ��һ�����ȷ�Ӧ����ôʵ��4��ʵ��1��ȣ�??�ų��������࣬������?��
�ο��𰸣���1��40?��? > ?
��2����?��?�¶Ƚϸߡ�
��3�� 4 ����Ӧ�����϶�
�����������
�����Ѷȣ���
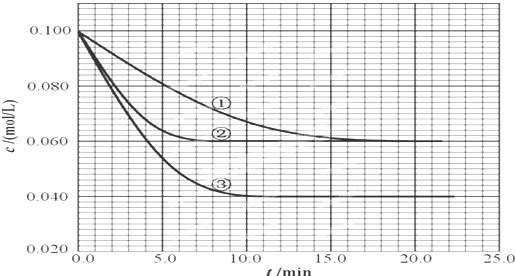
4������� ��2.00L���ܱ������У���Ӧ2A��g��?B��g��+C��g���ֱ������ֲ�ͬʵ�������½��У�����ʼŨ����ͬ����Ϊc��A��=0.100mol/L��c��B��=0.020mol/L��c��C��=0.020mol/L����Ӧ��A��Ũ����ʱ��ı仯����ͼ��ʾ��
��ش��������⣺
��1������˵����˵���÷�Ӧ�Ѵﵽƽ��״̬���ǣ�______������ţ�
��c��A����c��B����c��C��=2��1��1
��v��A��=2v��B��
����ϵ��ѹǿ���ٸı�
��A�������������ٸı�
�ݻ��������ܶȲ��ٸı�
��2������ʵ��ۻش𣺷�Ӧ��ʼ��4.0minʱ��Ӧ��A��ת����Ϊ______��Bƽ����Ӧ����Ϊ______��
��3����ٱȽϣ��ں͢۷ֱ���ı�һ�ַ�Ӧ���������ı�������ǣ���______����______��
��4��ʵ��������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��ֵ��______����ʵ��ٵ���ƽ���ά����ϵ�¶Ȳ��䣬����������Ͷ��0.028molB��0.028molC������ƽ��ʱ��ϵ��A�����ʵ���Ũ�ȣ���д��������̣�
�ο��𰸣���1����ƽ��ʱ�����ʵ����ʵ����Ķ���ȡ������ʼ����ת���ij̶ȣ�������Ϊ�жϴﵽƽ������ݣ��ʴ���
���κ�ʱ��v��A��=2v��B����������Ϊ�жϴﵽƽ������ݣ��ʴ���
�۷�Ӧǰ������Ļ�ѧ������֮����ȣ�ѹǿ������Ϊ�жϵ����ݣ�����ȷ��
��A�������������ٸı䣬����Ϊ�жϴﵽƽ������ݣ�����ȷ��
���κ�ʱ���������������ٷ����仯��������������䣬���»��������ܶȲ��ٱ仯�����Բ�����Ϊ�жϴﵽƽ������ݣ��ʴ���
��ѡ���ܣ�
��2��ʵ���ƽ��ʱB��ת����Ϊ0.04mol/L0.1mol/L%=40%��
2A��g��?B��g��+C��g��
��ʼ ��mol/L�� 0.1 0.02 0.02
ת�� ��mol/L�� 0.04 0.02 0.02
4.0min��mol/L�� 0.06 0.04 0.04
��Bƽ����Ӧ����Ϊ0.02mol/L4.0min=0.005mol/��L?min����
�ʴ�Ϊ��40%��0.005mol/��L?min����
��3��������ܼӿ컯ѧ��Ӧ�ٶ��ʣ����̴ﵽƽ���ʱ�䣬��ѧƽ�ⲻ�ƶ������Ԣ�Ϊʹ�ô������������¶ȣ���ѧ��Ӧ�ٶ��ʼӿ죬��ѧƽ���ƶ���ƽ��ʱA��Ũ�ȼ�С���ʴ�Ϊ���Ӵ������¶����ߣ�
��4��2A��g��?B��g��+C��g��
��ʼ ��mol/L�� 0.1 0.02 0.02
ת�� ��mol/L�� 0.04 0.02 0.02
ƽ�⣨mol/L�� 0.06 0.04 0.04
ƽ�ⳣ������ʽK=C(C)C(B)C2(A)=0.04��0.040.062=49��
����ϵ����Ͷ��0.028molB��0.028molC��ƽ�������ƶ�����ת����B�����ʵ���Ũ��Ϊx
2A��g��?B��g��+C��g��
��ƽ�⣨mol/L��0.0600.0400.040
����ʼ��mol/L��0.0600.040+0.0140.040+0.014
ת����mol��/L��2xxx
��ƽ�⣨mol/L��0.060+2x0.054-x0.054-x
K=(0.054-x)2(0.060+2x)2=49 x=0.006mol/L��
�ٴδﵽƽ��ʱA�����ʵ���Ũ�ȣ�c��A��=��0.060+0.006��2��mol/L=0.072mol/L��
�ʴ�Ϊ��49��0.072mol/L��
���������
�����Ѷȣ�һ��
5��ѡ���� ������A��B�ֱ�Ϊ0.6mol��0.5mol����0.4L�ܱ������з�����Ӧ��3A+B mC+2D����5min��ﵽƽ�⣬��ʱCΪ0.2mol����֪�ڴ˷�Ӧʱ��D��ƽ����Ӧ����Ϊ0.1mol��L-1��min-1�����½�����ȷ����?��?��
mC+2D����5min��ﵽƽ�⣬��ʱCΪ0.2mol����֪�ڴ˷�Ӧʱ��D��ƽ����Ӧ����Ϊ0.1mol��L-1��min-1�����½�����ȷ����?��?��
A.mֵΪ3 ?
B.B��ת����Ϊ20%?
C.A��ƽ����Ӧ����Ϊ0.1mol��L-1��min-1?
D.ƽ��ʱ��Ӧ����������ʵ���Ϊ1mol
�ο��𰸣�B
���������3A+B mC+2D
mC+2D
nʼ? 0.6mol��0.5mol? 0? 0
n��?0.3mol? 0.1mol? 0.1m? 0.2mol
nƽ?0.3mol? 0.4mol? 0.1m? 0.2mol
0.1m? =? 0.2mol? m=1B��ת����Ϊ20% ,A��ƽ����Ӧ����Ϊ0.15mol��L-1��min-1? ,B ��ȷ��C����ƽ��ʱ��Ӧ����������ʵ���Ϊ1.1,mol,D����
�����Ѷȣ���