��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ʵ���� ��14�֣�����FeCl3��ˮ��Һ��________������ԡ��������ԡ������ԡ�����ԭ����__________________________________�������ӷ���ʽ��ʾ����ʵ��������FeCl3��ˮ��Һʱ������FeCl3���������ڽ�Ũ�������У�Ȼ����������ˮϡ�͵������Ũ�ȣ���___________����ٽ����������ơ�����ˮ�⣻�����FeCl3��Һ���ɣ����գ����õ�����Ҫ���������____________________��
����ij������ȤС�����ⶨijNaOH��Һ��Ũ�ȣ�������������£�
����0.10mol/L�ı�������ϴ��ʽ�ζ���2��3��
��ȡ������ע����ʽ�ζ�������0���̶�����2��3mL��
�۰�ʢ�б��������ʽ�ζ��̶ܹ��ã����ڵζ��ܼ���ʹ֮������Һ
�ܵ���Һ������0����0���̶����£����¶���
��ȡ20.00mL����NaOH��Һע��ྻ����ƿ�У�������2��3�μ�����Һ
�ް���ƿ���ڵζ��ܵ����棬�ñ�����ζ����յ㣬��¼�ζ��ܶ���
��ش��������⣺
��1��ij�εζ�ʱ�ĵζ����е�Һ������ͼ��ʾ�������Ϊ ?mL��

��2�������������ݣ�
�����
| ����Һ���(mL)
| �����������mL��
|
�ζ�ǰ������mL��
| ��������mL��
|
��һ��
| 20.00
| 0.50
| 25.40
|
�ڶ���
| 20.00
| 4.00
| 29.10
|
���������ռ���Һ��Ũ��Ϊ?mol/L��
��3������ʵ�������ʹʵ����ƫ�ߵ���??��
A����ƿ�ô���Һ��ϴ����ע�����Һ
B����ʽ�ζ���δ�ñ�Һ��ϴ����װ���Һ
C����ʽ�ζ��ܵζ�ǰ���Ӷ������ζ������Ӷ���
D����ʽ�ζ��ܵζ�ǰ�����ݣ��ζ���������
�ο��𰸣�����1�����ԣ�Fe3����3H2O Fe(OH)3��3H�������ƣ�Fe2O3?
Fe(OH)3��3H�������ƣ�Fe2O3?
����1��22.60?��2��0.1250?��3��A��B��C��D
�������������FeCl3��Һ���ɣ�ˮ��ƽ�������ƶ�������Fe(OH)3�������գ�Fe2O3�ֽ�����Fe2O3��
����1������ʱע��ζ��ܵĿ̶��ص㣺С�̶����ϣ���̶����£��Ҷ���0.01 mL��
��2������Ҫ���������������������ƽ��ֵ��
V1=25.40-0.50=24.9mL? V2="29.10-4.00=25.10" mL
���������������ƽ��ֵ=��24.9+25.10��/2="25.00" mL
��NaOH+HCl=NaCl+H2O���ã�C��NaOH��V��NaOH��= C��HCl��V��HCl������
C��NaOH��=��0.10mol/L��25.00 mL��/20.00 mL="0.1250" mol/L��
��3�����ù�ϵʽC��NaOH��= C��HCl��V��HCl��/ V��NaOH���жϣ�
�ڴ�������ʱ��C��HCl��=0.10mol/L��V��NaOH��="20.00" mL�����ԣ����еIJ������������Ϊ����������Ķ�������C��NaOH����V��HCl�������ȣ�
��ƿ�ô���Һ��ϴ����ע�����Һ��n(NaOH)���࣬����V��HCl������ʹʵ����ƫ�ߣ�
��ʽ�ζ���δ�ñ�Һ��ϴ��������C��HCl����С������V��HCl������ʹʵ����ƫ�ߣ�
C��V��HCl��=V2-V1���ζ������Ӷ���������V2���ζ�ǰ���Ӷ���������V1��С������V��HCl������ʹʵ����ƫ�ߣ�
D������V��HCl����������������=�������������ʹʵ����ƫ�ߣ�
�����Ѷȣ�һ��
2��ѡ���� �����и����У���ʹˮ�ĵ���ƽ�����������ƶ���������Һ��pHС��7��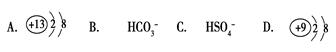
�ο��𰸣�A
���������
��ȷ��:A
A��Al3��ˮ������ԣ��ٽ�ˮ���룬pHС��7��A��ȷ��
B��ˮ�⣬�ٽ�ˮ���룬��pH����7��
C��ǿ����ʣ�����ˮ���룻
D��F�Dˮ�⣬�ٽ�ˮ���룬ˮ���pH����7.
�����Ѷȣ�һ��
3��ѡ���� ��101kPa 25��ʱ��1.0g����������ȫȼ������Һ̬ˮʱ�ų�����52.0kJ��������ȼ�յ��Ȼ�ѧ����ʽΪ
A��C2H6(g) �� 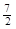 O2(g)��2CO2(g) ��3H2O(l)��H =��1560kJ��mol��1
O2(g)��2CO2(g) ��3H2O(l)��H =��1560kJ��mol��1
B��2C2H6(g) �� 7O2(g)��4CO2(g) ��6H2O(g)��H =��1560kJ��mol��1
C��2C2H6(g) �� 7O2(g)��4CO2(g) ��6H2O(l)��H =��3120 kJ��mol��1
D��C2H6(g) ��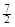 O2(g)��2CO2(g) ��3H2O(l)��H =��52.0kJ��mol��1
O2(g)��2CO2(g) ��3H2O(l)��H =��52.0kJ��mol��1
�ο��𰸣�A
�������������ȼ�����ڷ��ȷ�Ӧ����H��0����C������ݡ�1.0g����������ȫȼ������Һ̬ˮʱ�ų�����52.0kJ���á�1.0mol����������ȫȼ������Һ̬ˮʱ�ų�����52��30��1560kJ������A����ȷ��B��D�����
�����Ѷȣ�һ��
4��ѡ���� �������½����к͵ζ�����ͼ�ǡ����ȫ��Ӧʱ������˵��һ����ȷ����
A���μӷ�Ӧ����ͼ�����ʵ������
B���μӷ�Ӧ�����е�H�������ͼ��е�OH���������
C����Ӧ����Һ��pH��7
D���������ʵ������ָʾ�����ж�
�ο��𰸣�B
���������
��ȷ�𰸣�B
A������ȷ���μӷ�Ӧ����ͼ�����ʵ�����һ����ȣ�ǡ����ȫ��Ӧ���ǰ�����ʽ�ļ�����֮�ȷ�Ӧ��
B����ȷ���μӷ�Ӧ�����е�H�������ͼ��е�OH��������ȣ�
C������ȷ��ֻ��ǿ����ǿ���Ӧ����Һ��pH��7
D������ȷ�������������Χ�ڣ����ʵ������ָʾ�������жϷ�Ӧ���յ㡣
�����Ѷȣ�һ��
5��ѡ���� 25�棬a L 0.1000mol/L CH3COOH��Һ��b L 0.1000 mol/L NaOH��Һ��ϣ�����˵����ȷ���ǣ�?��
A����a��b����pHһ��С��7
B����a��b����һ�����ڣ�n(OH��)��n(H��)��0.1(b��a)
C��c(Na��)��c(CH3COO��)��c(OH��)��c(H��)����a��b
D����pH��7����a��b����c(Na��)��c(CH3COO��)��c(CH3COOH)
�ο��𰸣�B
�����������a��b����������������Һ���������ԣ�A����ȷ����a��b�����������ƹ��������ݵ���غ��֪��n(OH��)��n(H��)��n(Na��)��n(CH3COO��)�����ڴ�����ˮ�⣬������Һ��n(CH3COO��)С��0.1amol�����ѡ��B��ȷ�����������ʱ��Ҳ�����Լ��ԣ�C����ȷ����Һ������ʱ������һ���ǹ����ģ�����c(Na��)��c(CH3COO��)��c(CH3COOH)��D����ȷ����ѡB��
�����Ѷȣ�һ��