微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (10分)某化学兴趣小组要完成中和热的测定。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃棒、0.5mol・ L-1盐酸、0.55mol・L-1NaOH溶液,尚缺少的实验玻璃用品是 、 。
(2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒? (填“能”或“否”)。
(3)他们记录的实验数据如下:已知:Q=Cm(t2 -t1),反应后溶液的比热容C为4.18kJ・℃-1・ kg-1,各物质的密度均为1g・cm-3。①计算完成下表。(保留小数点后一位)

②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:
(4)若用KOH代替NaOH,对测定结果 (填“有”或“无”)影响;若用醋酸代替HCl做实验,测定所得的中和热的数值将 (填“变大”或“变小”或“无影响”)。
参考答案:(10分)(1)量筒、温度计(共2分)
(2)否;金属易导热,热量散失导致误差大;(共2分)
(3)①-56.8kJ/mol(2分)
②NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-56.8kJ/mol(2分)
(4)无,变小。(共2分)
本题解析:(1)中和热的测定实验中,需要量筒量取液体,需要温度计测量溶液的温度,所以还需要量筒、温度计;
(2)不能用环形铜丝搅拌棒代替环形玻璃搅拌棒,因为金属易导热,热量散失导致误差大;
(3)①两次实验中溶液的体积功100mL,则溶液的总质量是100g,温度升高的平均值是(23.3-20+23.5-20) ℃/2=3.4℃,根据Q=Cm(t2 -t1)计算该反应中放出的热量Q="4.18" kJ・℃-1・ kg-1×0.1kg×3.4℃=1.4212kJ,则中和热是生成1mol水放出的热量,HCl不足,按HCl的量进行计算,所以△H=-1.4212kJ/(0.5mol/L×0.05L)=-56.8kJ/mol;
②所以氢氧化钠与HCl溶液反应的热化学方程式为NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-56.8kJ/mol;
(4)KOH与NaOH都是一元强碱,所以对结果无影响;若用醋酸代替HCl做实验,因为醋酸是弱酸,电离需要吸收热量,则放出的热量少,测定所得的中和热的数值将变小。
考点:考查中和热的测定实验,仪器的选择,中和热的计算与判断,热化学方程式的书写
本题难度:一般
2、选择题 下列各分子中,化学键类型不同的是
A.H2O、CO2
B.MgF2、H2O2
C.KOH、Mg(OH)2
D.HCl、HBr
参考答案:B
本题解析:一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键,据此可知,A中都是极性键,B中前者是离子键,后者是共价键,C中都含有离子键和极性键,D中都是极性键,答案选B。
点评:该题是高考中的常见题型,属于基础性试题的考查。难度不大,主要是考查学生对化学键知识的了解掌握程度。该题的关键是明确离子键和共价键的含义以及判断依据,然后结合题意灵活运用即可。
本题难度:一般
3、选择题 化学反应N2+3H2 2NH3的能量变化如下图所示,该反应的热化学方程式是( )
2NH3的能量变化如下图所示,该反应的热化学方程式是( )
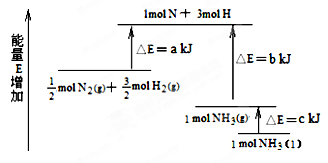
A.N2(g)+3H2(g)  2NH3(l)
2NH3(l)