| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《常见的化学电源》高频试题预测(2017年最新版)(四)
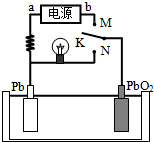 参考答案:A、K与N相接时,是原电池,Pb做负极,PbO2做正极,能量变化为化学能转化为电能,故A错误; 本题解析: 本题难度:简单 4、填空题 (6分)在银锌原电池中,以硫酸铜为电解质溶液,锌为 极,电极上发生的是________反应(“氧化”或“还原”), 银为__ ___极,电极反应式是___ _ _____,银表面上可观察到的现象是_ _______;原电池反应的离子方程式为_________。 参考答案:负 、氧化、正、Cu2++2e-=Cu、有红色物质析出、Zn+Cu2+=Zn2++Cu 本题解析:考查原电池的应该判断。在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,正极得到电子,发生还原反应。锌比银活泼,锌是负极,银是正极,溶液中的铜离子得到电子而析出铜。 本题难度:一般 5、选择题 科学家设想以N2和H2为反应物,以溶有A的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氮的新型燃料电池,装置如下图所示,下列说法不正确的是 |
参考答案:C
本题解析:A.该电池的本质是合成氨反应,所以正极是氮气发生还原反应,电极反应式为N2 + 6e- + 8H+=2NH4+,正确;B.反应过程中,H+不断消耗导致PH值变大,需要加入盐酸,正确;C.该装置是原电池装置,电流由正极通过外电路流向负极,即由通入氮气的电极沿外电路流向通入氢气的电极,错误;D.通入氢气的电极为负极,生成的铵根离子与氯化氢结合生成氯化铵,所以A是NH4Cl,正确;选C。
考点:考查新型燃料电池的工作原理。
本题难度:一般
|
||
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | ||
| 下一篇:高考化学知识点归纳《氨气》高频.. | ||