微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列实验问题的表述不正确的是
A.普通漏斗、蒸馏烧瓶、分液漏斗是高中化学实验中常用的分离仪器
B.实验室用H2还原CuO,当反应完毕时应持续通入H2一段时间
C.发现有人一氧化碳中毒时,立即将其转移到通风的地方救治
D.在萃取碘水中碘的实验时,注入碘水和萃取剂,倒转分液漏斗,反复用力震荡后立即分液
参考答案:D
本题解析:反复用力振荡后应静置,待液体分层后才能进行分液操作.
本题难度:一般
2、选择题 正确的实验操作是实验成功的基本保证。下列实验操作正确的是

A.检查装置气密性
B.蒸发
C.转移液体
D.读取气体体积
参考答案:C
本题解析:
正确答案:C
A、不正确,有两个出气口,无法检验;B、不正确,不需要用石棉网;C、正确;D、读体积时要内外压强相同。
本题难度:简单
3、选择题 下列装置能达到实验目的的是( )
 ?
? ?
? ?
?
①?②?③?④
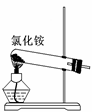
A.实验室用装置①制取氨气
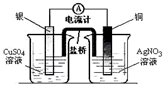
B.装置②将化学能转化为电能
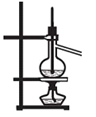
C.装置③可用于分离沸点相差较大的互溶液体混合物
D.装置④中X若为四氯化碳,可用于吸收氨气,并防止倒吸
参考答案:D
本题解析:氯化铵加热分解为氨气和氯化氢,氨气和氯化氢在稍冷却的地方重新反应生成了氯化铵,故A错误;装置②为不是原电池装置,不能够将化学能转化为电能,故B不正确,应该将两种电解质溶液对换;装置③中的温度计的末端应该位于支管口下方0.5cm处,故装置③不可以用于分离沸点相差较大的互溶液体混合物;D中,氨气不会溶于四氯化碳,但易溶于水,所以装置④中X若为四氯化碳,可用于吸收氨气,并防止倒吸,故D正确,为本题的答案。
点评:本题考查了化学实验,该知识点是高考考查的重点和难点,也是考查考查的热点,本题有一定的综合性,有一定的难度。
本题难度:一般
4、实验题 (10分)从今年3月16日下午开始,大陆“海水受日本核辐射污染,碘可防辐射”等消息疯传,从绍兴、宁波、台州地区开始出现抢盐潮,接着蔓延到多个城市,人们抢购加碘盐是因为食盐中添加了碘元素。
I.人们在即将受到核辐射前的24小时内,需在医生指导下服用碘片,成人推荐服用量为100mg碘,假设此碘盐碘元素含量为40 mg/kg,要达到上述碘含量要求,需服用该碘盐?kg,你觉得服用碘盐防辐射合理吗??
II.如图为某加碘盐标签的一部分。
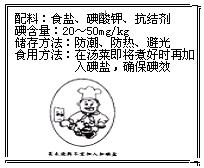
已知:①KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O②I2+2Na2S2O3=2NaI+Na2S4O6(无色)
某同学欲测定此加碘盐中碘元素的含量,进行以下实验:
步骤1:称取ag市售食盐,配成溶液,全部转移
至锥形瓶中,加入适量新制KI溶液,滴入几滴稀硫酸,溶液变黄色,再加入3滴淀粉溶液。
步骤2:取一支50mL碱式滴定管,用bmol・L-1的新制Na2S2O3 溶液润洗2~3次后,装满溶液,调节液面高度至0刻度。
步骤3:开始滴定直至终点,重复操作2~3次,实验数据记录如下:
编号
| 碱式滴定管读数
| 消耗体积(mL)
|
滴定前刻度
| 滴定后刻度
|
1
| 0
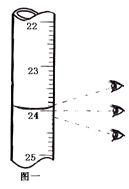
| 如图一
| ?
|
2
| 0
| 23.98
| 23.98
|
3
| 0
| 24.02
| 24.02
|
(1)第一次读数为?mL。
(2)滴定终点的判断方法?。
(3)经过计算,此加碘盐碘元素的含量为?mg/kg(用包含a、b的最简表达式表示)。
(4)下列操作可能会导致测量结果偏低的是?。
A.步骤1中称取食盐时将砝码放在左盘,食盐放在放在右盘,游码读数为0.5g
B.步骤1所配食盐溶液未完全转移至锥形瓶
C.步骤2中滴定管洗涤后未润洗
D.步骤3滴定前滴定管尖嘴处有气泡,滴定后气泡消失
参考答案:(10分) I.? 2.5?(1分)? ?不合理?(1分)
II.(1)24.00?(2分)(2)溶液颜色恰好由蓝色变为无色且半分钟内不褪色(2分)
(3)508000b/a(2分)?(4)? AB (2分)
本题解析:略
本题难度:一般
5、选择题 下列物质与常用危险化学品的类别不对应的是? ( )
A.H2SO4、NaOH ――腐蚀品
B.CH4、C2H4 ――易燃液体
C.CaC2、Na――遇湿易燃物品
D.KMnO4、K2Cr2O7 ――氧化剂
参考答案:B
本题解析:A正确,两者均具有强烈的腐蚀性;B错,两者为易燃气体;C正确,CaC2、Na易与水反应;D正确,KMnO4、K2Cr2O7 为常见的强氧化剂;
本题难度:简单