微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列计算结果正确是( )
A.标准状况下,用一充满氨气的干燥烧瓶做喷泉实验,当水充满整个烧瓶后(假设溶液不外溢),烧瓶内氨水的物质的量的浓度为(
)mol/L
B.标准状况下,将64g?铜片投入到100ml?18?mol/L的浓硫酸中加热会产生22.4?L的SO2气体
C.向1mol的碳酸钾固体中缓缓滴加少量的稀盐酸会产生1mol的CO2气体
D.向含有1mol?Ba(OH)2溶液中通入1molCO2气体就会产生1mol?Ba(HCO3)2的白色沉淀
参考答案:A、令烧瓶的容积为VL,则氨气的体积为VL,氨气的物质的量为VL22.4L/mol=V22.4mol,氨水溶液的物质的量浓度为V22.4molVL=122.4mol/L,故A正确;
B、发生反应Cu+2H2SO4?△?.?CuSO4+SO2↑+2H2O,64g铜的物质的量为1mol,硫酸的物质的量为0.1L×18mol/L=0.18mol,由方程式可知,硫酸不足量,且随反应进行浓硫酸变为稀硫酸,铜与稀硫酸不反应,故1mol铜不能完全反应,生成的SO2气体小于1mol,体积小于22.4L,故B错误;
C、向1mol的碳酸钾固体中缓缓滴加少量的稀盐酸,首先反应生成碳酸氢钾,碳酸钾反应完毕,盐酸在于碳酸氢钾反应生成二氧化碳,是否生成二氧化碳及二氧化碳体积多少,与盐酸的量有关,故C错误;
D、1mol?Ba(OH)2溶液中通入1molCO2气体,前后反应生成1mol?BaCO3白色沉淀,故D错误;
故选A.
本题解析:
本题难度:一般
2、选择题 下列变化中,必须加入氧化剂才能发生的是(?)
A.SO2→S
B.SO32-→SO2
C.Fe2+→Fe3+
D.HCO3-→CO32-
参考答案:C
本题解析:必须加入氧化剂才能发生的反应,本身一定是还原剂,还原剂在反应过程中失去电子,化合价升高,符合这个条件的只有C。。
本题难度:简单
3、选择题 (1)在一定温度和压强下,1体积X2(g)和3体积Y2(g)化合生成2体积Z(g),则Z气体的化学式是?。
(2)A、B两种气体组成的混合气体8.6 g,在标准状况下体积为8.96 L。已知A与B的物质的量之比为3∶1,相对分子质量之比为14∶1,由此可推断A可能是?,B可能是?。
(3)在标准状况下,CO和CO2的混合气体质量为36 g,体积为22.4 L,则CO所占的体积是?L,质量是??g。
参考答案:(1)XY3 (2)N2(或CO或C2H4) H2 (3)11.2 14
本题解析:(1)根据阿伏加德罗定律可写出化学方程式:X2+3Y2=2Z,再根据质量守恒定律,可得Z的化学式应为XY3。
(2)由题意可得:n(A)+n(B)=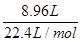 =0.4 mol,则3n(B)+n(B)=0.4 mol,即n(B)=0.1 mol,n(A)=0.3 mol。
=0.4 mol,则3n(B)+n(B)=0.4 mol,即n(B)=0.1 mol,n(A)=0.3 mol。
设B的相对分子质量为Mr,则A的相对分子质量为14Mr。
0.3×14Mr+0.1×Mr=8.6,解得Mr=2,则A、B的相对分子质量分别为28、2,A可能为N2、C2H4或CO,B可能是H2。
(3)由题意列方程组得
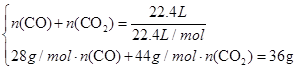
解得:n(CO)=0.5 mol,n(CO2)=0.5 mol
故V(CO)=11.2 L,m(CO)=14 g。
本题难度:一般
4、选择题 归纳与推理是化学学习常用的方法。下列推理正确的是
A.因为稀硫酸能与铁反应放出H2,所以稀硝酸与铁反应也一定能放出H2
B.因为Na可以与水反应放出H2,所以K也可以与水反应放出H2
C.因为CO2的水溶液可以导电,所以CO2是电解质
D.因为SO2可以使酸性KMnO4溶液褪色, 所以SO2具有漂白性
参考答案:B
本题解析:A项:稀硝酸是强氧化性酸,稀硝酸与铁反应不放出H2,故错;C项:CO2是非电解质,故错;D项:SO2可以使酸性KMnO4溶液褪色,是因为SO2具有还原性,故错。故选B。
点评:本题考查的知识点较多,解题关键是抓住定义和物质的性质,对于错误的推理要通过反例推翻。
本题难度:简单
5、选择题 下列有关 反应类型说法中正确的是?(?)
A. 是通过加聚反应得到的产物
是通过加聚反应得到的产物
B.乙醇在浓硫酸作催化剂,并且在加热的条件下一定发生消去反应
C.卤代烃一般来说在NaOH的水溶液中能发生取代反应,而在NaOH的醇溶液中不一定能发生消去反应
D.酯类物质在一定条件下水解一定得到相应的羧酸和醇
参考答案:C
本题解析: 是缩聚反应产物;
是缩聚反应产物;
乙醇在浓硫酸作催化剂,加热到170℃发生消去反应,但加热到140℃则发生取代反应;
酯类物质在酸性条件下水解得到相应的羧酸和醇,但在碱性条件下水解得到相应的羧酸盐和醇
本题难度:一般