微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 实验室利用图④来制乙烯时,常因温度过高而发生副反应.部分乙醇跟浓硫酸反应生成二氧化硫、二氧化碳、水蒸气和炭黑.请用下列编号为①~④的实验装置设计一个实验,以验证上述反应后的混合气中含有二氧化碳、二氧化硫和水蒸气.
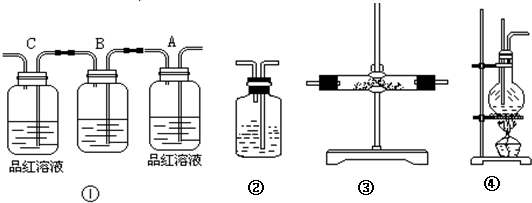
(1)装置③中的固体药品为______,用以验证的产物是______
(2)装置B中的试剂为______(填“A、B、C、D”)
A.溴水?B.酸性高锰酸钾溶液?C.NaOH溶液?D.饱和NaHCO3溶液
(3)装置②盛有______,可以验证______气体的存在.
(4)用装置的编号表示其连接顺序(按气体产物从左到右的流向) ④→______;
(5)装置A中的现象是______,验证______;
(6)装置C中的现象是______说明______.
参考答案:因水蒸气检验用无水硫酸铜,二氧化硫的检验用品红溶液,二氧化碳的检验用澄清石灰水,二氧化碳、二氧化硫都能使澄清石灰水变浑浊,水蒸气检验一般放在最前面,接着检验二氧化硫,最后检验二氧化碳,同在检验二氧化碳之前用溴水除去SO2,再通过品红溶液不褪色确认SO2已除干净.最后用澄清石灰水检验二氧化碳;
(1)因装置③用来检验水蒸气检,所用试剂为无水硫酸铜,故答案为:无水硫酸铜;水蒸气;
(2)因装置①用来检验SO2,A瓶品红溶液褪色,说明含有SO2,B瓶装有溴水除去SO2,C瓶通过品红溶液不褪色确认SO2已除干净,故答案为:A;?
(3)因装置②用来检验二氧化碳,二氧化碳能使澄清石灰水变浑浊,故答案为:澄清石灰水;CO2;
(4)因先发生反应产生混合气体,然后依次检验水蒸气、接着检验二氧化硫,最后检验二氧化碳,所以用装置的编号表示其连接顺序(按气体产物从左到右的流向)④③①②,故答案为:③①②;
(5)因装置①用来检验SO2,A瓶品红溶液褪色,说明含有SO2,B瓶装有溴水除去SO2,C瓶通过品红溶液不褪色确认SO2已除干净,故答案为:品红褪色;SO2;
(6)因装置①用来检验SO2,A瓶品红溶液褪色,说明含有SO2,B瓶装有溴水除去SO2,C瓶通过品红溶液不褪色确认SO2已除干净,故答案为:品红不褪色;SO2已被除净.
本题解析:
本题难度:一般
2、计算题 欲测定烟雾中的SO2含量,可做下列实验:取100 L该空气(标准状况下),通过盛放100 mL过氧化氢 (H2O2)水溶液的吸收瓶,使它们充分反应,生成硫酸。在吸收后的水溶液中加入BaCl2溶液,生成白色沉淀, 经测定其质量为11.65 g。
(1)试写出SO2和H2O2反应的离子方程式。
____________________________________。
(2)写出H2SO4与BaCl2反应的离子方程式。
____________________________________。
(3)求100 L空气中SO2的体积分数。
参考答案:(1)SO2+H2O2 = 2H++SO42-+2H2O+O2↑
(2)SO42-+Ba2+ = BaSO4↓
(3)1.12%
本题解析:
本题难度:一般
3、选择题 除去二氧化硫中三氧化硫不可采用的方法是( )
A.通过冰水混合物冷却
B.通过98.3%的浓硫酸
C.通过饱和的Na2SO3溶液
D.通过饱和的NaHSO3溶液
参考答案:C
本题解析:
本题难度:一般
4、简答题 (1)请针对CO2和SO2的相同点与不同点回答问题.
①它们中可以使澄清石灰水变浑浊的是______.
②它们中可以用向上排空气法收集的是______.
③它们中能使品红溶液及高锰酸钾溶液褪色的是______.
(2)现有两位同学设计了下述两个方案,并都认为如果观察到的现象和自己设计的方案一致,即可确证无色混合气体中含有CO2和SO2.
方案甲:气体通过酸性高锰酸钾溶液时溶液褪色,继续通过澄清石灰水时石灰水变浑浊.
方案乙:气体通过品红溶液时溶液红色变浅,继续通过澄清石灰水时石灰水变浑浊.
试评价上述各方案是否严密.若你认为哪个方案不严密,请简要说明理由:______.
参考答案:①使澄清石灰水变浑浊的气体是二氧化碳和二氧化硫,发生CO2+Ca(OH)2=CaCO3↓+H2O、SO2+Ca(OH)2=CaSO3↓+H2O,
故答案为:CO2、SO2 ;
②可以用向上排空气法收集的气体是比空气重,可以依据相对分子质量和空气平均相对分子质量29比较分析,大于29比空气重,小于29气体比空气轻所以二氧化硫和二氧化碳气体都比空气重,可以用向上排空气法收集,
故答案为:CO2、SO2;
③二氧化硫具有还原性和漂白性可以使高锰酸钾褪色,品红褪色.能使品红溶液及高锰酸钾溶液褪色的是二氧化硫,故答案为:SO2;
(2)方案甲若二氧化硫大量存在,通过高锰酸钾溶液后有剩余,二氧化硫也会使澄清石灰水变浑浊,所以需要在通过高锰酸钾溶液后再通过品红试液检验二氧化硫是否全部反应,所以甲不严密;方案乙通过品红溶液红色变浅,说明有二氧化硫且全部被品红吸收,再通过澄清石灰水变浑浊说明含二氧化碳,可以证明二氧化硫和二氧化碳的存在,乙严密,
故答案为:方案甲不严密,因为当只有较大量的SO2时,也会出现其中的现象,方案乙严密.
本题解析:
本题难度:一般
5、选择题 下列叙述正确的是( )
A.SO2和Cl2的漂白原理相同
B.SO3具有氧化性
C.常温下,浓硫酸不与铜反应,是因为铜被钝化
D.可用铁罐来进行贮存、运输冷的浓硫酸
参考答案:A.二氧化硫与有色物质化合,氯气与水反应生成HClO,具有强氧化性,均可使有色物质褪色,但原理不同,故A错误;
B.SO3中,S为+6价,可得到电子,具有氧化性,故B正确;
C.常温下,浓硫酸不与铜反应,而钝化发生了氧化还原反应,Cu没有发生钝化,故C错误;
D.常温下,Fe遇浓硫酸发生钝化,阻止反应的进一步发生,则可用铁罐来进行贮存、运输冷的浓硫酸,故D正确;
故选D.
本题解析:
本题难度:简单