微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列溶液中,能大量共存的离子组是
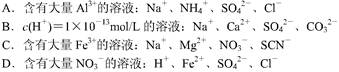
参考答案:A
本题解析:B中碳酸钙沉淀,C中Fe3+与SCN- 生成红色溶液,Fe2+在H+,NO3-中被氧化为Fe3+
本题难度:简单
2、选择题 下列各组离子溶液中因发生氧化还原反应,而不能大量共存的是
[? ]
A. Na+、Ba2+、Cl-、SO42-
B. Ca2+、HCO3-、Cl-、K+
C. MnO4-、K+、I-、H+
D. H+、Cl-、Na+、CO32-
参考答案:C
本题解析:
本题难度:一般
3、选择题 下列离子组一定能大量共存的是( )
A.能使甲基橙变红的溶液中:Na+、NH4+、I-、NO3-
B.含有0.1?mol?L-1Ba2+的溶液中:K+、Mg2+、CO32-、SO42-
C.由水电离出来的c(H+)=1×10-13mol?L-1的溶液中:K+、CH3COO-、Cl-、NO3-
D.常温下,KW/(OH-)=0.1?mol?L-1的溶液:Na+、SO42-、NH4+、NO3-
参考答案:A.能使甲基橙变红的溶液,显酸性,H+、I-、NO3-发生氧化还原反应,则不能共存,故A错误;
B.因Ba2+分别与CO32-、SO42-反应碳酸钡、硫酸钡,则不能共存,故B错误;
C.由水电离出来的c(H+)=1×10-13mol?L-1的溶液,为酸或碱溶液,酸溶液中氢离子与CH3COO-结合生成弱酸,则不能共存,故C错误;
D.常温下,KW/(OH-)=0.1?mol?L-1的溶液,即c(H+)=0.1mol/L,溶液显酸性,该组离子之间不反应,则能共存,故D正确;
故选D.
本题解析:
本题难度:一般
4、选择题 在溶液中能大量共存的离子组是?(?)
A.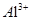 、
、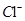 、
、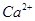
B.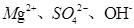
C.K+、H+、CO32-
D.Cl一、Ag+、Ba2+
参考答案:A
本题解析:A可以大量共存.
B不能,镁离子与氢氧根离子不能共存,要生成氢氧化镁沉淀.
C不能,氢离子与碳酸根离子不能大量共存.
D不能,氯离子不能与银离子大量共存.所以正确答案是A
本题难度:一般
5、填空题 (1)25 ℃时,0.1 mol・L-1NaOH溶液的pH为________;
(2)25 ℃时,0.1 mol・L-1NH4Cl溶液的pH_____7(填“<”、“=”或“>”),其原因是_________(用离子方程式表示);
(3)将上述两种溶液等体积混合后,离子浓度大小次序正确的是________(填序号)。
A.[Na+]>[Cl-]>[OH-]>[H+]
B.[Na+]=[Cl-]>[H+]>[OH-]
C.[Na+]=[Cl-]>[OH-]>[H+]
D.[Cl-]>[Na+]>[OH-]>[H+]
(4) 下列物质能导电且属于电解质的是________(填序号)。
A.铁? B.盐酸? C.氯化钠晶体? D.熔融氢氧化钠
(5) 25℃时,0.1 mol・L-1NaOH溶液中水电离出来的氢氧根的浓度为C1,0.1 mol・L-1NH4Cl溶液中水电离出来的氢离子的浓度为C2,则C1 ______C2(填“<”、“=”或“>”)。
参考答案:(1)13 (2)< NH4++H2O NH3・H2O+H+ (3)C? (4) D ?(5) <
NH3・H2O+H+ (3)C? (4) D ?(5) <
本题解析:(1)氢氧化钠是一元强碱,则25 ℃时,0.1 mol・L-1NaOH溶液中OH-浓度是0.1mol/L,所以溶液中氢离子浓度=10-14÷0.1=10-13mol/,因此溶液的pH为13。
(2)由于氯化铵是强酸弱碱盐,溶于水NH4+水解,NH4++H2O NH3・H2O+H+,溶液显酸性,则25 ℃时,0.1 mol・L-1NH4Cl溶液的pH<7。
NH3・H2O+H+,溶液显酸性,则25 ℃时,0.1 mol・L-1NH4Cl溶液的pH<7。
(3))25 ℃时,0.1 mol・L-1NaOH溶液与0.1 mol・L-1NH4Cl溶液等体积混合后,二者恰好反应生成氯化钠和弱电解质一水合氨,溶液显碱性,因此溶液中离子浓度大小关系是[Na+]=[Cl-]>[OH-]>[H+],答案选C。
(4)溶于水或在熔融状态下能够电离出离子的化合物是电解质,溶于水和在熔融状态下都不能电离出离子的化合物是非电解质,据此可以判断。A、铁是金属单质,可以导电,但不是电解质,也不是非电解质,A不正确;B、盐酸可以导电,但属于混合物,不是电解质,也不是非电解质,B不正确;C、氯化钠晶体是电解质,但不能导电,只有溶于水或在熔融状态下才能导电,C不正确;D、熔融的氢氧化钠可以导电,属于电解质,D正确,答案选D。
(5)水是弱电解质,存在电离平衡H2O H++OH-。因此酸或碱抑制水的电离,盐类水解促进水的电离。0.1 mol・L-1NaOH溶液中水电离出来的氢氧根的浓度为C1,0.1 mol・L-1NH4Cl溶液中水电离出来的氢离子的浓度为C2,则C1<C2。
H++OH-。因此酸或碱抑制水的电离,盐类水解促进水的电离。0.1 mol・L-1NaOH溶液中水电离出来的氢氧根的浓度为C1,0.1 mol・L-1NH4Cl溶液中水电离出来的氢离子的浓度为C2,则C1<C2。
本题难度:困难