微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
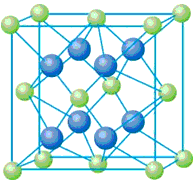
1、填空题 已知A、B、C、D和E都是元素周期表中前36号的元素,它们的原子序数依次增大。A与其他4种元素既不在同一周期又不在同一主族。B原子的L层p轨道中有5个电子;C是周期表中1-18列中的第14列元素;D和E属同一周期,又知E原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1,D跟B可形成离子化合物,其晶胞结构如右图。请回答
(1)A与C形成的共价化合物的分子式是__________,杂化轨道类型是__________,分子的立体结构是
__________。
(2)B与C比较,电负性较小的是_______(填元素符号);B与C形成的化合物晶体类型是_________。
(3)E属元素周期表中第_____周期,第______族的元素,其元素名称是________,它的+2价离子的电子排布式为__________。
(4)从图中可以看出,D跟B形成的离子化合物的化学式为__________;若设该晶胞的边长为a cm,则该离子化合物晶体的密度是__________(只要求列出算式)。
2、填空题
氯化铬酰(CrO2Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
请回答下列问题:
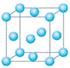
⑴写出铬原子的基态电子排布式_____________________,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有__________(填元素符号),其中一种金属的晶胞结构如右图所示,该晶胞中含有金属原子的数目为?。
⑵CrO2Cl2常温下为深红色液体,能与CCl4、CS2等互溶,据此可判断CrO2Cl2是__________(填“极性”或“非极性”)分子。
⑶在①苯、②CH3OH、③HCHO、④CS2、⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有___________(填序号),CS2分子的空间构型是__________。
3、选择题 下列各组物质状态发生变化时,所克服的微粒间作用力完全相同的是
A.碘的升华和干冰气化
B.二氧化硅和干冰熔化
C.苯和硝酸钾熔化
D.食盐的熔化和冰的融化
4、填空题 (15分)氮化硅是一种重要的结构陶瓷材料,硬度大、耐磨损。利用SiO2和C的混合粉末在N2的气氛中加热至1300℃反应制得。请回答下列问题:
(1)已知氮化硅的晶体结构中,原子间都以单键相连,且N原子和N原子,Si原子与Si原子不直接相连,同时每个原子都满足8电子稳定结构,则氮化硅的化学式____,晶体类型是?;
(2)基态Si原子的电子排布式为_________;Si和C相比,电负性较大的是_________,
(3)在SiO2晶体结构中,O-Si-O的键角是_______,Si原子和周围的四个O原子组成的空间构型为?,SiO2中Si的杂化类型_______;
(4)氮化硅抗腐蚀能力强,一般不与其他无机酸反应,但能和氢氟酸反应生成硅酸。试写出该反应的化学方程式?。
(5)晶体硅的晶胞如图所示,则每个晶体硅的晶胞中含有?个硅原子。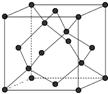
5、填空题 如图所示的甲、乙、丙三种晶体
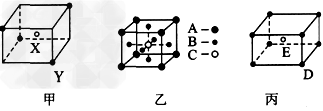
?试推断甲晶体化学式(X为阳离子)为____,乙晶体中A、B、C三种微粒的个数比是
____,丙晶体中每个D微粒周围结合E微粒的个数是________个。