微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 火法炼铜可以从黄铜矿(CuFeS2)或辉铜矿(Cu2S)中提取铜,发生如下反应:
①2CuFeS2+4O2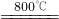 Cu2S+3SO2+2FeO
Cu2S+3SO2+2FeO
②2Cu2S+3O2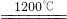 2Cu2O+2SO2
2Cu2O+2SO2
③2Cu2O+Cu2S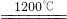 6Cu+SO2↑
6Cu+SO2↑
下列说法正确的是
A.反应②、③中,Cu2S都只做还原剂
B.1mol?CuFeS2生成1molCu,理论上消耗2.5mol?O2
C.1mol?Cu2S和O2反应生成2molCu转移的电子数为4mol
D.反应①中,共转移的电子数为16mol,CuFeS2中铜元素的化合价为+2
参考答案:B
本题解析:分析:A.②中S元素的化合价升高,O元素的化合价降低;③中,Cu2S中Cu元素的化合价降低,S元素的化合价升高;
B.由反应可知,存在6Cu~3Cu2S~6CuFeS2~15O2,以此分析;
C.Cu元素由+1价降低为0,O元素的化合价降低,而S元素的化合价由-2价升高为+4价;
D.反应①中,Cu元素的化合价降低,O元素的化合价降低,S元素的化合价升高.
解答:A.②中S元素的化合价升高,O元素的化合价降低,Cu2S只做还原剂;③中,Cu2S中Cu元素的化合价降低,S元素的化合价升高,Cu2S既是还原剂又是氧化剂,故A错误;
B.由反应可知,存在6Cu~3Cu2S~6CuFeS2~15O2,则1mol?CuFeS2生成1molCu,理论上消耗2.5molO2,故B正确;
C.Cu元素由+1价降低为0,O元素的化合价降低,而S元素的化合价由-2价升高为+4价,则转移的电子数为1mol×[4-(-2)]=6mol,故C错误;
D.反应①中,CuFeS2中铜元素的化合价为+2,Cu元素的化合价降低,O元素的化合价降低,S元素的化合价由-2价升高为+4价,2molCuFeS2反应转移电子为24mol,故D错误;
故选B.
点评:本题考查氧化还原反应及计算,明确反应中的元素的化合价变化是解答本题的关键,注意电子守恒、原子守恒的应用,选项D为易错点,题目难度较大.
本题难度:困难
2、选择题 在氧化还原反应3S+6KOH=K2SO3+2K2S+3H2O中,被氧化与被还原的硫原子个数比是
A.1:2
B.2:1
C.1:1
D.3:2
参考答案:A
本题解析:
正确答案:A
一个硫原子由0价升高为+4价(K2SO3),被氧化,二个硫原子由0价降低为-2价(K2S)
本题难度:困难
3、选择题 实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:负极Pb+SO42-=PbSO4+2e-正极PbO2+4H++SO42-+2e-=PbSO4+2H2O,今若制Cl20.050 mol,这时电池内消耗H2SO4的物质的量至少是
[? ]
A.0.025 mol
B.0.050 mol
C.0.10 mol
D.0.20 mol
参考答案:C
本题解析:
本题难度:一般
4、填空题 4HCl(浓)+MnO2
MnCl2+Cl2↑+2H2O反应中,MnO2与被氧化的HCl的物质的量之比是______;若有6mol?Cl2生成时,反应中转移______mol?e-.
参考答案:盐酸中氯元素的化合价在反应前后如下:HCl→MnCl2,化合价-1→-1,化合价没变化,起酸的作用;
?HCl→Cl2化合价由-1→0,失电子,作还原剂;所以在反应中盐酸有氧化性和酸性.
由方程式知,盐酸有一半参加氧化还原反应,
2HCl(浓)(酸性)+2HCl(浓)(还原剂)+MnO2 ?△?.??MnCl2 +Cl2↑+2H2O? 转移电子
?2? 1? ?1? ? 2
? ? 6mol? 12mol
?故答案为:1:2; 12;
本题解析:
本题难度:一般
5、选择题 将11.2g的Mg-Cu混合物完全溶解于足量的硝酸中,收集反应产生的x气体.再向所得溶液中加入适量的NaOH溶液,产生21.4g沉淀.根据题意推断气体x的成分可能是
A.0.3mol?NO2?和0.3mol?NO
B.0.2mol?NO2和0.1mol?N2O4
C.0.1mol?NO、0.2mol?NO2和0.05mol?N2O4
D.0.6mol?NO
参考答案:C
本题解析:分析:向Mg-Cu混合物与足量的硝酸反应所得溶液中加入足量的NaOH溶液,产生21.4g沉淀为氢氧化镁、氢氧化铜,所以沉淀中氢氧根的质量为21.4g-11.2g=10.2g,物质的量为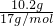 =0.6mol,根据电荷守恒可知,11.2g的Mg-Cu提供的电子为0.6mol,结合选项根据电子转移守恒判断.
=0.6mol,根据电荷守恒可知,11.2g的Mg-Cu提供的电子为0.6mol,结合选项根据电子转移守恒判断.
解答:向Mg-Cu混合物与足量的硝酸反应所得溶液中加入足量的NaOH溶液,产生21.4g沉淀为氢氧化镁、氢氧化铜,所以沉淀中氢氧根的质量为21.4g-11.2g=10.2g,物质的量为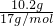 =0.6mol,根据电荷守恒可知,11.2g的Mg-Cu提供的电子为0.6mol,
=0.6mol,根据电荷守恒可知,11.2g的Mg-Cu提供的电子为0.6mol,
A、生成0.3mo1NO2和0.3mo1NO,N元素获得电子为0.3mol×(5-4)+0.3mol×(5-2)=1.2mol,得失电子不相等,故A错误;
B、生成0.2mo1NO2和0.1mo1N2O4,N元素获得电子为0.2mol×(5-4)+0.1mol×2×(5-4)=0.4mol,得失电子不相等,
故B错误;
C、生成0.1mol NO、0.2mol NO2和0.05mol N2O4,N元素获得电子为0.1mol×(5-2)+0.2mol×(5-4)+0.05mol×2×(5-4)=0.6mol,得失电子相等,故C正确;
D、生成0.6molNO,N元素获得电子为0.6mol×(5-2)=1.8mol,故D错误.
故选:C.
点评:考查混合物的计算、氧化还原反应计算等,难度中等,计算金属提供的电子的物质的量是解题的关键,注意守恒思想的运用.
本题难度:一般