��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���б仯������������������ڷ�Ӧ�������������
A��H + H = H��H
B��H��Cl =" H" + Cl
C��Mg + 2HCl = MgCl2 + H2 ��
D��H2SO4 + 2NaOH = Na2SO4 + 2H2O
�ο��𰸣�B
�������������������������ڷ�Ӧ���������Ϊ���ȷ�Ӧ
A��ԭ�Ӽ��γ��¹��ۼ���Ҫ�ų�����
B����ɼ�����Ҫ������������������
C�������û����е������ķ�ӦΪ���ȷ�Ӧ
D������кͷ�ӦΪ���ȷ�Ӧ
�����Ѷȣ�һ��
2��ѡ���� ��ӦA(g)��B(g)?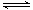 ?C(g)��D(g)�����е������仯��ͼ��ʾ���ɴ˿��жϣ�?��
?C(g)��D(g)�����е������仯��ͼ��ʾ���ɴ˿��жϣ�?��
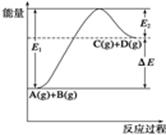
A��1molA��1molB��ַ�Ӧ�������仯Ϊ��E
B�����������Ӧ�ӿ죬��E��С
C����Ӧ����ܼ���С����������ܼ���
D����Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת��������
�ο��𰸣�D
���������A��1molA(g)��1molB(g)��ַ�Ӧ������1mol?C(g)��1molD(g)�������仯Ϊ��E������B�����������Ӧ�ӿ죬E1��E2��С����E���䣬����C�������ͼ��֪����Ӧ����ܼ��ܴ�����������ܼ��ܣ�����D�������ͼ��֪���÷�ӦΪ���ȷ�Ӧ����Ӧ�ﵽƽ��ʱ�������¶ȣ�ƽ�������ƶ���A��ת����������ȷ��
�����Ѷȣ�һ��
3��ѡ���� ������ͼ�������仯ʾ��ͼ������ѡ����ȷ����

A��2C====2A+B����H��0
B��2A+B====2C����H��0
C��2C(g)="===" 2A(g)+B(g)����H��0
D��2A(g)+B(g)====2C(g)����H��0
�ο��𰸣�D
����������������ͼ��֪��2A��g��+B��g������������2C��g������������CΪ��Ӧ���Ӧ2A��g��+B��g���T2C��g���ͷ���������H��0�����CΪ��Ӧ���Ӧ2C��g���T2A��g��+B��g��������������H��0��ѡD��
�����Ѷȣ�һ��
4������� ��16�֣�һ�ֻ�϶����������Էֱ��õ綯������ȼ�����߶��߽���ƶ����֡��������»����ʱ���綯���ṩ�ƶ������������͵����ģ���ɲ��������ʱ��ȼ���ṩ�ƶ�����ʹ�綯�����ڳ��״̬��Ŀǰ��ȼ��������Ϊȼ�ϣ��綯��һ��ʹ�������أ�KOH�����Һ����
�Է����ش��������⣺
��1����֪������ɲ��������ʱ�����������缫��Ӧ�ֱ�Ϊ��
�缫��M+H2O+e-��MH+OH��MΪ����Ͻ�MHΪ��������ԭ�ӵĴ���Ͻ�
�ҵ缫��Ni��OH��2+OH--e����NiOOH+H2O
������һ�����мס������缫�����Ʒֱ��ǣ��ף�?���ң�?��
��2�����������»����ʱ�����������缫��Ӧ�ֱ�Ϊ��
�缫��?���ҵ缫��?��
�缫��Χ��Һ��pH�仯�ǣ�ѡ������䡱��С"����ͬ����?����?��
��3����ȼ������ʱ��Ϊ�������Ͳ���ȫȼ�ջ������Ⱦ������CO����֪�ڳ��³�ѹ�£�
C8 H18��1��+25��2 O2��g��=8CO2��g��+9 H2O��g������H=-5121.9kJ��mol
2CO��g��+O2��g��=2CO2��g������H=-566.0kJ��mol
H2 O��g��=H2 O��1������H=-44.0kJ��mol
д�����Ͳ���ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��?��
��4��Ϊ��������β���е�һ����̼��Ũ�ȣ��ɲ�ȡ��������������������һ����ȼ����ͨ�����з�Ӧ��ʵ��ת����2 CO��g��+O2��g�� 2CO2��g��
2CO2��g��
��֪���¶�ΪT�������£�����ȼ���л�ѧ��Ӧ����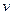 ������=v���棩ʱ��������Ũ�ȴ������к㶨��ϵ��
������=v���棩ʱ��������Ũ�ȴ������к㶨��ϵ��
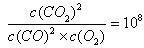
���¶�ΪT�������£���ij�������˲�ȼ����CO��CO2��Ũ�ȷֱ�Ϊ1.0��10-5mol��L-1��1.01��10-4mol��L-1��Ҫ�ڸ��¶���ʹ����β����CO��Ũ�Ƚ�Ϊ1.0��10-6mol��L-1����ȼ����Ӧ���ϲ���O2����ʹO2Ũ�ȱ�����?mol��L-1��
�ο��𰸣���16�֣�

�����������
�����Ѷȣ�һ��
5��ѡ���� ����˵����ȷ����
A����Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ
B�����ȷ�Ӧ�ķ�Ӧ���������֮��С���������������֮��
C��ͬһ��ѧ��Ӧ������Ӧ������ͬ���ȿ��ܲ�ͬ
D�����������ܸı䷴Ӧ���ʣ�Ҳ�ܸı䷴Ӧ���е���
�ο��𰸣�C
���������A�����ȷ�Ӧ�е�����ȣ��еIJ�����ȣ���ľ̿��ȼ����һ�����ȷ�Ӧ������Ҫ��ȼ����ȼ��Ŀ����ʹ��ﵽ�Ż�㣮�������ȷ�ӦҲ�ǣ��ʴ���
B�����ȷ�Ӧ�ķ�Ӧ���������֮�ʹ����������������֮�ͣ��ʴ���
D�������ܸı仯ѧ��Ӧ���ʣ������ܸı仯ѧ��Ӧ���ȣ�������ʹ��ѧƽ���ƶ����ʴ���
��ѡC��
���������⿼���˻�ѧ��Ӧ�������뻯ѧ��Ӧ����ЧӦ��Ĺ�ϵ����ѧ��Ӧ���ʺ��ȵ�֪ʶ������ȷ����������ȵı��ʣ��ǽ���Ĺؼ���
�����Ѷȣ�һ��