��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
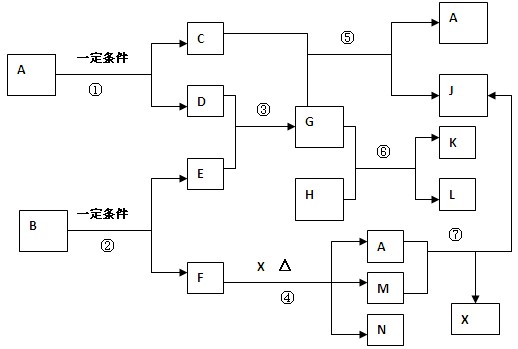
1������� ��(15�֣���ͼ�У�������A,? B��G��M, L, J ��������Ԫ����ɣ�����A��һ����ɫҺ�壬 G�Ǽ�������ˮ�ij������壬L�����еĵ�����Ϊ18(L����Է�����������34)����Ӧ���ǹ�ҵ����X����Ҫ��Ӧ֮һ��������H����ǿ�������ԣ����ɳ���±����������Լ���Һ�ڳ����·�Ӧ���Ƶá�N����Һ��dz��ɫ��(ע����Щ��Ӧ��ˮҲ��ȥ)
�밴Ҫ����գ�
��1��д���������ʵĻ�ѧʽ��
L��?��X��?��
��2����Ӧ�ܵ����ӷ���ʽΪ��?��
��3����Ӧ�����ӷ���ʽΪ��?��
��4���Թ�����H��Һ��N��Һ����д����ij��������������ӷ���ʽΪ��
?��
��5��B��F����������Ϊ30.77%����B�Ļ�ѧʽΪ��?��
�ο��𰸣���1��N2H4? HNO3
(2)Fe��4H����2NO3��=Fe2����2NO2����2H2O
(3) Cl����2NH3=N2H4��Cl����H2O
(4)5ClO����2Fe2����5H2O=2Fe(OH)3����4HClO��Cl��
(5) FeN9
���������A��һ����ɫҺ�壬��Ϊˮ��ˮ�����������������N����Һ��dz��ɫ˵�������������ӡ�������H����ǿ�������ԣ����ɳ���±����������Լ���Һ�ڳ����·�Ӧ���Ƶã����H��KClO��G�Ǽ�������ˮ�ij������壬���G�ǰ�����HCl����G��HCl����L�Ǵ�������Ȼ��أ���������18���ӣ���G�ǰ���������H��������18���ӵ�����N2H4����L��N2H4������ʽΪCl����2NH3=N2H4��Cl����H2O��D��E���ɰ�������D��������E�ǵ�����C��������������������������ˮ��NO��J��NO��ͨ����Ӧ�߿ɵó�M�Ƕ�������������ˮ���������NO����XΪ���ᣬ�ڼ���ʱ������ԭ���ɶ������������F������B��F����������Ϊ30.77%������B��N��Fe�ĸ�������
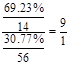 ?�����Ի�ѧʽΪFeN9
?�����Ի�ѧʽΪFeN9
�����Ѷȣ�һ��
2������� X��Y��Z�������������µ���ʾ��ϵ��
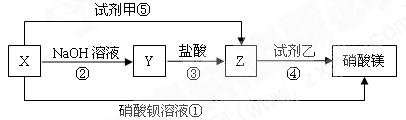
��1����������ת����ϵ���ƶ��������ʵĻ�ѧʽ��
X?��Y?��Z?���Լ���?���Լ���??��
��2��д��������~�ݲ���Ӧ�����ӷ���ʽ��
��?����?��
��? ?����?��
?����?��
��?��
�ο��𰸣���ÿС���1�֣���10�֣�
��1�� MgSO4? Mg(OH)2? M gCl2? BaCl2? AgNO3
gCl2? BaCl2? AgNO3
(2) Ba2+ + 2H+ = BaSO4��
Mg2+ + 2OH- = Mg(OH
Mg(OH )2��
)2��
Mg(OH)2 + 2H+ = Mg2+ + 2H2O
Ag+ + Cl- = AgCl��
 ?Ba2+ + 2H+ = BaSO4��
?Ba2+ + 2H+ = BaSO4��
�����������
�����Ѷȣ�һ��
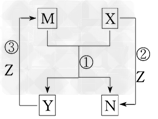
3��ѡ���� X��Y��Z����ѧ���������ֵ��ʣ�M��N����ѧ���������ֻ��������M�ڳ�����ΪҺ̬������֮�������ͼ��ʾ��ת����ϵ�������й�˵���������
[? ]
A���ù������漰�ķ�Ӧ��Ϊ������ԭ��Ӧ
B����X����Ϊ����ʱ��������Na��Fe
C����X����Ϊ�ǽ���ʱ��������F2��C
D����Ӧ�ٿ����ڳ����½��У�Ҳ������Ҫ�ڸ����²��ܷ���
�ο��𰸣�B
���������
�����Ѷȣ�һ��
4������� X��Y��Z��W��ԭ��������������Ķ�����Ԫ�أ�����ͬ�壬����ֻ������Ϊ����Ԫ�أ�Xԭ�ӵ������������������������ȣ�X��W��Y��Z������ԭ�ӵ�����������֮�;�Ϊ9��Y��W�ĵ��ʶ�����NaOH��Һ��Ӧ����ش��������⣺
��1��XԪ�ص�������_________��Y��Z��W��ԭ�Ӱ뾶��С�����˳����________����Ԫ�ط��ű�ʾ����
��2��WԪ�������ڱ��е�λ����__________��YԪ�ص�ԭ�ӽṹʾ��ͼ��___________��
��3��Z��W��һ�����������γɻ�����ZW2�������и�ԭ�Ӿ��ﵽ��8�����ȶ��ṹ����ZW2�ĵ���ʽ��_______�����ڳ����³�Һ̬���γɾ���ʱ������________���塣
��4��X�ĵ�����Y�ĵ��ʻ�ѧ�������ƣ���X�ĵ�����NaOH��Һ��Ӧ�����ӷ���ʽ��_______________��ע���������У�����XԪ�صĻ�����Ļ�ѧʽ�к���2����ԭ�ӣ�
��5��0.1mol W�ĵ�����50 mL 1.5 mol��L-1��FeBr2��Һ��Ӧ����������Fe2+��Br-�����ʵ���֮����____________��
�ο��𰸣�
��1���루1�֣���Cl<S<Al��2�֣�
��2���������ڢ�A�壻 ����2�֣�
����2�֣�
��3��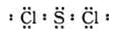 ��2�֣������ӣ�1�֣�
��2�֣������ӣ�1�֣�
��4��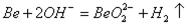 ��2�֣�
��2�֣�
��5��3�U5��3�֣�
�����������
�����Ѷȣ�һ��
5������� 2016����˻Ὣ����Լ����¬���У���ͼ���ư����廷����ʾA��B��C��D��E���ֻ���������沿�ִ������ֻ����ﺬ��һ����ͬԪ�أ��ҽ��沿���������ĵ�Ԫ�ظ�����ͬ�����ֻ����������ֶ�����Ԫ����ɣ���ÿ�ֻ������������Ԫ����ɡ�A�ǿ�ȼ������Ҫ�ɷ֣�B��E�������������������������(SiH4)���ӵĵ�������ȣ�B���ȶ������н�ǿ�����ԣ��ܷ�������������ԭ��Ӧ��E����Է�������Ϊ32�����л�ԭ�ԣ��ҳ�������������ȼ�ϣ�D���������ǽ������ϣ�����������Ԫ�ص�ԭ�Ӹ���֮��Ϊ3��4��������֮��Ϊ3��2��
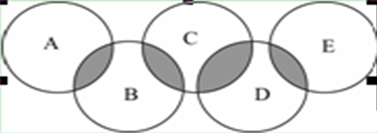
��1�� D�Ļ�ѧʽΪ________��
��2��A��B��E�к���һ����ͬ��Ԫ�أ�������Ϊ________��
��3��B��E��Ӧ������һ�ֵ��ʺ�һ�ֳ�����Һ̬�����д����ѧ����ʽ________��
��4��д��C������������Һ��Ӧ�����ӷ���ʽ___________��
�ο��𰸣�.��1��Si3N4?��2����
��3��N2H4+2H2O=N2��+H2O
��4��SiO2+2OH-=SiO32-+H2O
���������A�ǿ�ȼ������Ҫ�ɷ֣�˵��A�Ǽ��飬B��E�������������������������(SiH4)���ӵĵ�������ȣ�˵����18���ӣ�B���ȶ������н�ǿ�����ԣ��ܷ�������������ԭ��Ӧ��˵��B��H2O2��E����Է�������Ϊ32�����л�ԭ�ԣ��ҳ�������������ȼ�ϣ�˵����N2H4��D���������ǽ������ϣ�����������Ԫ�ص�ԭ�Ӹ���֮��Ϊ3��4��������֮��Ϊ3��2��D��E������ͬ��Ԫ�أ������ж�ΪN�����Խ��ԭ�Ӹ����ȿ���֪���ϼ�Ϊ+4�ۣ��ٽ��ԭ�Ӹ����ȣ����Լ����D��Si3N4����C��SiO2��
�����Ѷȣ�һ��