微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (8分)二氧化氯(ClO2)是一种在水处理等方面有广泛应用的高效安全消毒剂。比Cl2更好。
⑴在ClO2的制备方法中,有下列两种制备方法:
方法一:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O
方法二:2NaClO3+H2O2+H2SO4=2ClO2↑+Na2SO4+O2↑ +2H2O
+2H2O
用方法二制备的ClO2更适合用于饮用水消毒,其主要原因是?。
⑵用ClO2处理过的饮用水(pH 5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(ClO2-)。
饮用水中的ClO2、ClO2-含量可用连续碘量法进行测定。ClO2被I-还原为ClO2-、Cl-的转化率与溶液pH的关系如下图所示。当pH≤2 .0时,ClO2-也能被I-完全还原为Cl-。反应生成的I2用标准Na2S2O3溶液滴定;2Na2S2O3+ I2= Na2S4O6 + 2NaI
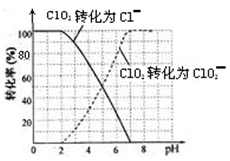
①请写出pH≤2 .0时ClO2--与I-反应的离子方程式?。
②请完成相应的实验 步骤:
步骤:
步骤1:准确量取V mL水样加入到锥形瓶中。
步骤2:调节水样的pH为7.0~8.0。
步骤3:加入足量的KI晶体。
步骤4:加入少量淀粉溶液,用c mol・L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V1mL。
步骤5:?。
步骤6:再用c mol・L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2?mL。
③根据上述分析数据,测得该饮用水中ClO2-的浓度为? ?mol・L-1(用含字母的代数式表示)。
?mol・L-1(用含字母的代数式表示)。
参考答案:(8分)⑴方法 二制备的ClO2中不含Cl2(2分)
二制备的ClO2中不含Cl2(2分)
⑵①ClO2-+4H++4I-=Cl-+2I2+2H2O(2分)
②调节溶液的pH≤2.0(2分)?③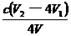 (2分)
(2分)
本题解析:略
本题难度:一般
2、实验题 某化学学习小组对铝与酸和碱的反应进行探究,过程如下。
实验I:
(1)取形状、大小均相同的铝丝分别与等体积的、PH相同的盐酸、稀硫酸反应,随反应进行,盐酸中生成气体的速率明显比硫酸中生成气体的速率快,对此原因,你认为合理的猜测是下列的?(填写相应的字母);
a. 盐酸的物质的量浓度大于硫酸的物质的量浓度
b. Cl-能促进此反应的进行
c. SO42-能抑制此反应的进行
d. 硫酸使铝发生钝化
(2)为了探究反应速率不同的原因,请你根据所提供的药品,填写实验方案中的空白部分。
药品:氯化钠固体、硫酸钠固体、硫酸铜固体、氯化铜固体、6mol/L盐酸、3mol/L硫酸、18.4mol/L硫酸、5mol/L硝酸。
方案:取两支试管,分别加入形状、大小均相同的铝丝和等体积的?(填写相应的试剂,下同),再向其中的一支试管中加入适量的?固体并振荡使固体溶解,观察实验现象。
实验探究:略。
实验II:
取足量的形状、质量均相同的铝丝分别与等体积的6mol/L的盐酸、6mol/L氢氧化钠溶液反应,待反应停止后取出剩余的铝丝洗净、干燥、称量,剩余铝丝的质量关系是前者?后者(填“大于”或“小于”或“等于”);观察反应后的液体,发现铝与盐酸反应后所得的液体是黑色浑浊的,试管底部有少量黑色沉淀,对此现象,同学们进行了如下探究:
(1)提出猜想
同学们查找资料后获得如下信息:工业上用电解法冶炼铝所用的原料氧化铝是从铝土矿中提取的,所以得到的氧化铝中可能还含有微量的氧化铁和二氧化硅两种杂质,据此,同学们提出如下猜想:
猜想1:此黑色固体是铁单质,可能是电解得到的铝与杂质反应生成的,相应的化学反应方程式为??;
猜想2:此黑色固体是硅单质,是电解得到的铝与二氧化硅反应生成的。
猜想3:此黑色固体是铝单质,是铝与盐酸反应时因反应过快而变成粉末分散到溶液中;
猜想4:此黑色固体可能是上述若干种单质组成的混合物。
(2)设计实验方案并完成相关实验:
将反应后所得的液体进行过滤、洗涤,分别取少量固体置于两支试管中,完成下列实验:
① 向其中的一支试管中加入足量的稀盐酸,观察固体是否溶解。实验时发现固体完全溶解,证明猜想?一定不正确(填“1”、“2”、“3”、“4”)。
② 向另一试管中加入足量的氢氧化钠溶液,观察固体是否溶解。实验时发现固体完全溶解,证明猜想?一定不正确(填“1”、“2”、“3”、“4”);
(3)得出结论
综合实验①②的现象,可推知猜想?(填“1”、“2”、“3”、“4”)是正确的,固体溶解在氢氧化钠溶液中的离子方程式为:?。
参考答案:实验I:(1)bc;(2分)(2)3mol/LH2SO4、氯化钠固体(或6mol/LHCl、硫酸钠固体)(2分)
实验II:大于(2分)(1)2Al+Fe2O3 2Fe + Al2O3;(3分)
2Fe + Al2O3;(3分)
(2)①2(1分);②1(1分);
(3)3(1分),2Al+2OH-+2H2O=2AlO2-+3H2↑;(3分);
本题解析:实验I:(1)两实验现象的差异原因应从反应物组成的不同点去寻找,此题中其他条件均相同,不同的是盐酸中含有Cl-而硫酸中含有SO42-,所以从这个方面思考即可得答案;
(2)根据控制变量法和对比实验法,在控制其他条件相同时,只让两实验中有一个变量不同。如:都用稀硫酸,但其中一份加入Cl-而另一份不加Cl-,即可得出结论(类似方法亦可)。
实验II:由化学方程式可知,等物质的量的HCl与NaOH相比,NaOH消耗的铝更多,所以留下的铝就少,故“前者大于后者”;
(1)根据信息和有关物质的性质,可以看出黑色固体可能是铝、铁、硅三种单质中的一种或几种,从而提出猜想。猜想1中铁的生成是由于电解法时生成的铝能与氧化铁发生铝热反应,由此可写出相应的化学反应方程式;猜想2的化学反应方程式根据题意就可直接写出;
(2)①在盐酸中固体完全溶解,证明一定不含硅,所以猜想2一定不正确;
②在氢氧化钠溶液中固体完全溶解,证明一定不含铁,所以猜想1一定不正确;
(3)综合(1)(2)中相应的结论,可知此固体只含有铝,故猜想3正确,猜想4不正确,固体是铝,铝与氢氧化钠溶液反应的离子方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。
本题难度:一般
3、选择题 下列物质不能由单质直接化合而成的是( )
A.FeCl3
B.Fe3O4
C.Cu2S
D.CuS
参考答案:A、Fe和氯气点燃时直接化合生成FeCl3,故A正确;
B、铁在氧气气中燃烧生成Fe3O4,故B正确;
C、铜和硫粉混合加热即生成硫化亚铜(Cu2S),故C正确;
D、铜和硫粉混合加热即生成硫化亚铜(Cu2S),故D错误;
故选D.
本题解析:
本题难度:简单
4、选择题 下列说法不正确的是?
[? ]
A.?采用原煤脱硫技术,可减少燃煤燃烧时产生的SO2 ?
B.?自来水可用氯气来杀菌消毒,说明氯气无毒 ?
C.?氮氧化物可以破坏臭氧层,也能形成酸雨
D.?化石燃料燃烧产生大量CO2,会导致温室效应
参考答案:B
本题解析:
本题难度:简单
5、选择题 2008年浙江在线09月08日讯 “铁罐吐气熏黄了绿化带 余姚成功处置液氯泄漏事件”。下列有关说法合理的是(?)
A.液氯泄漏将公路两旁的绿化带熏黄,这是由于Cl2的漂白性所致
B.泄漏的液氯应该用大量碱性溶液或石灰中和
C.液氯泄漏后立即挥发成氯气而扩散到空气中,所以事故现场不必进行特别的处理
D.这次事故说明液氯不能用铁罐盛装
参考答案:B
本题解析:液氯可以用铁罐储存。氯气是一种黄绿色、有毒、密度比空气大、易液化、能溶于水和碱液的气体。
本题难度:一般