微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应的离子方程式书写正确的是( )
A.过量CO2和Ca(OH)2溶液反应:2OH-+Ca2++CO2═CaCO3↓+2H2O
B.碳酸钙与醋酸溶液反应:CaCO3+2H+═Ca2++CO2↑+H2O
C.硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2═Fe3++2H2O
D.向硫酸铜溶液中滴加氢氧化钡溶液至SO42-恰好沉淀完全:Cu2++SO42-+2OH-+Ba2+═Cu(OH)2↓+BaSO4↓
参考答案:A、过量CO2通入Ca(OH)2中最终产物为Ca(HCO3)2,溶于水并完全电离,反应为CO2+OH-=HCO3-,故A错误;
B、醋酸为弱酸,应写成化学式,碳酸钙不溶于水,离子方程式中应写成化学式,正确的离子方程式为CaCO3+2CH3COOH═2CH3COO-+CO2↑+Ca2++H2O,故B错误;
C、该项离子方程式电荷不守恒,正确的离子方程式为2Fe2++2H++H2O2═2Fe3++2H2O,故C错误;
D、向硫酸铜溶液中滴加氢氧化钡溶液至SO42-恰好沉淀完全,反应中Cu2+与OH-离子反应生成Cu(OH)2,SO42-与Ba2+离子反应生成BaSO4,
反应的离子方程式为Cu2++SO42-+2OH-+Ba2+═Cu(OH)2↓+BaSO4↓,故D正确;
故选D.
本题解析:
本题难度:一般
2、选择题 下列离子方程式不正确的是
[? ]
A.在30 mL 1 mol/L Na2SO3溶液中通入标准状况下的Cl2 224 mL:H2O+SO32-+Cl2===SO42-+2Cl-+2H+
B.硝酸银溶液中滴加过量氨水:Ag++2NH3·H2O===[Ag(NH3)2]++2H2O
C.饱和碳酸钠溶液中通入二氧化碳后溶液变浑浊: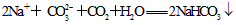
D.碳酸氢镁溶液中加入足量的澄清石灰水:
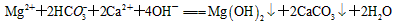
参考答案:A
本题解析:
本题难度:一般
3、选择题 在下列反应的离子方程式中,正确的是
A.二氧化硫与水反应:SO2 + H2O = 2H+ + SO32-
2H+ + SO32-
B.碳酸钙溶液与盐酸反应: CO32- +2H+ = CO2↑+ H2O
C.铁与稀硫酸反应:Fe + 2H+ =Fe2+ + H2↑
D.硫酸铜溶液与氢氧化钡溶液反应: SO42-+Ba2+ = BaSO4↓
参考答案:C
本题解析:略
本题难度:一般
4、简答题 将2.5g碳酸钠、碳酸氢钠和氢氧化钠的固体混合物完全溶解于水,制成稀溶液,然后向该溶液中逐滴加入1mol?L-1的盐酸,所加入盐酸的体积与产生CO2的体积(标准状况)关系如图所示:
(1)写出OA段所发生反应的离子方程式______、______.
(2)当加入35mL盐酸时,产生CO2的体积为______mL(标准状况).
(3)计算原混合物中NaOH的质量及碳酸钠的质量分数______.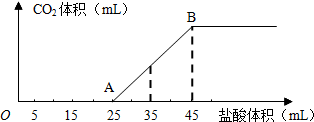
参考答案:(1)在溶液中碳酸氢钠与氢氧化钠反应生成碳酸钠,结合图象可知,开始没有二氧化碳气体生成,则制成的稀溶液中的溶质为碳酸钠和氢氧化钠,则OA段0~5mL先发生酸碱中和,
其离子反应方程式为H++OH-═H2O,再发生碳酸钠与盐酸反应生成碳酸氢钠与氯化钠,其离子反应方程式为CO32-+H+═HCO3-,
故答案为:H++OH-═H2O;CO32-+H+═HCO3-;
(2)结合图象可知,当加入35mL盐酸时,25~35mL发生碳酸氢钠与盐酸的反应生成二氧化碳气体,
设生成二氧化碳的物质的量为n,生成气体时消耗的酸的物质的量为(35-25)×10-3L×1mol?L-1=0.01mol,则
? HCO3-+H+═CO2↑+H2O
? 1? 1
?0.01mol ?n
11=0.01moln,解得n=0.01mol,标准状况下其体积为0.01mol×22.4L/mol=0.224L=224mL,
故答案为:224;
(3)设碳酸钠、碳酸氢钠和氢氧化钠的物质的量分别为x、y、z,则
①x+y=1mol/L×(0.045-0.025)L
②x+z=1mol/L×0.025L
③84g/mol?x+106g/mol?y+40g/mol?z=2.5g
联立①②③式解得x=0.01mol,y=0.01mol,z=0.015mol
故NaOH的质量为0.015mol×40g/mol=0.6g,
Na2CO3的质量分数为0.01mol×106g/mol2.5g×100%=42.4%,
答:原混合物中NaOH的质量为0.6g,碳酸钠的质量分数为42.4%.
本题解析:
本题难度:一般
5、选择题 离子反应方程式能表示物质在溶液中进行离子反应的实质.下列反应的离子方程式的书写中,正确的是( )
A.硫酸溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
B.将少量过氧化钠放入水中:Na2O2+H2O=2Na++2OH-+O2↑
C.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O
D.向氢氧化钠溶液中通入足量SO2气体:2OH-+SO2=SO32-+H2O
参考答案:A、硫酸溶液与氢氧化钡溶液反应:2OH-+Ba2++2H++SO42-=BaSO4↓+2H2O,故A错误;
B、将少量过氧化钠放入水中反应的离子方程式为:2Na2O2+2H2O=4Na++4OH-+O2↑,故B错误;
C、用小苏打治疗胃酸过多,是碳酸氢钠和胃酸中的盐酸反应:HCO3-+H+=CO2↑+H2O,故C正确;
D、向氢氧化钠溶液中通入足量SO2气体:OH-+SO2=HSO3-+H2O,故D错误;
故选C.
本题解析:
本题难度:简单