微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一定条件下,在某一密闭容器中发生如下反应:N2 (g)+3H2 (g)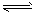 2NH3 (g)。下列有关该反应的说法中,正确的是
2NH3 (g)。下列有关该反应的说法中,正确的是
[? ]
A.降低温度可加快反应速率
B.使用催化剂可加快反应速率
C.平衡时,N2能完全转变成NH3
D.平衡时,正反应和逆反应均停止
参考答案:B
本题解析:
本题难度:一般
2、选择题 可逆反应2SO2(g)+O2(g)?2SO3(g),根据下表中的数据判断下列图像错误的是( )
压强
转化率
温度
| p1(MPa)
| p2(MPa)
|
400℃
| 99.6
| 99.7
|
500℃
| 96.9
| 97.8
|
?
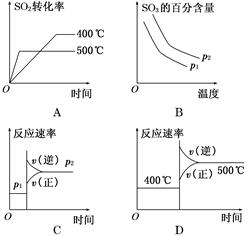
参考答案:C
本题解析:从表中数据可知,升高温度,转化率降低,故正反应放热,ΔH<0;增大压强,平衡正向移动,转化率增大,故有p1<p2;A项,温度越高,反应速率越快,转化率越小,正确;B项,温度升高,平衡逆向移动,SO3百分含量降低,增大压强,平衡正向移动,SO3的百分含量升高,正确;C项,增大压强,正逆反应速率均增大,平衡向正向移动,故v(正)>v(逆),错误;D项,升高温度,正逆反应速率均增大,平衡逆向移动,正确。
本题难度:一般
3、选择题 下列表述与示意图相符的是
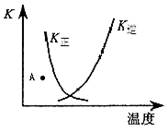
A.正反应为吸热反应
B.升高温度,有利于反应向正方向进行
C.A点时,反应向逆反应方向移动
D.K正与K逆的关系是:K正=1/K逆
参考答案:D
本题解析:A、根据图像可知,随着温度的升高,正方应的平衡常数逐渐减小,而逆反应的平衡常数逐渐增大,这说明升高温度平衡向逆反应方向移动,因此正方应是放热反应,A不正确;B、正方应是放热反应,升高温度有利于平衡向逆反应方向移动,B不正确;C、A点在温度不变的情况下要达到平衡状态,正方应的平衡常数增大,这说明反应向正反应方向移动,即正反应速率大于逆反应速率,C不正确;D、化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,因此正逆反应速率的平衡常数互为倒数,D正确,答案选D。
本题难度:一般
4、选择题 下列有关工业生产的叙述正确的是( )
A.合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率
B.硫酸工业中,为了提高SO2的转化率,用五氧化二钒作催化剂
C.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室
D.电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量小
参考答案:A、合成氨生产过程中将NH3液化分离,减小氨气的浓度会导致正化学反应速率减慢,化学平衡向右移动,提高N2、H2的转化率,故A错误;
B、硫酸工业中,用五氧化二钒作催化剂催化剂,只能加快反应速率,不会引起化学平衡的移动,不会提高SO2的转化率,故B错误;
C、电解饱和食盐水时,在阴极上产生的是氢气和氢氧化钠,在阳极上产生的是氯气,采用离子交换膜法,可防止阳极室产生的C12进入阴极室,故C错误;
D、电解精炼铜时,在阳极上是金属锌、铁、镍先失去电子,在阴极上是铜离子得电子生成金属Cu的过程,同一时间内阳极溶解铜的质量比阴极析出铜的质量小,溶液中铜离子浓度减小,故D正确.
故选D.
本题解析:
本题难度:简单
5、选择题 下列过程需要增大化学反应速率的是( )。
A.钢铁腐蚀
B.食物腐败
C.塑料老化
D.工业合成氨
参考答案:D
本题解析:对人类生活或研究有利的,我们就要增大其化学反应速率,如工业合成氨;对人类生活或研究不利的,我们就要抑制反应的发生,减小其反应速率,如钢铁腐蚀、食物腐败、塑料老化等。
本题难度:简单