微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 含NaOH 20.0g的稀溶液与足量稀盐酸反应,放出28.7 kJ的热量,表示该反应的热化学方程式正确的是
A.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H=" +28.7" kJ・mol-1
B.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H= _28.7 kJ・mol-1
C.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H="+57.4" kJ・mol-1
D.NaOH(aq)+HCl(aq)==NaCl(aq)+H2O(l);△H= _57.4 kJ・mol-1
参考答案:D
本题解析:20.0gNaOH是0.5mol,与足量稀盐酸反应,放出28.7 kJ的热量,则1molNaOH反应,放热28.7*2=57.4kJ。根据热化学方程式的书写原则进行判断。
A项,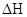 的符号和数值均不正确。
的符号和数值均不正确。
B项,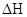 的数值不正确。
的数值不正确。
C项,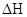 的符号不正确。
的符号不正确。
D项,符合热化学方程式的书写原则,正确。
故选D
本题难度:一般
2、填空题 能源是现代社会发展的支柱之一。
(1)化学反应中的能量变化,通常主要表现为热量的变化。
①下列反应中,属于放热反应的是___________(填序号)。
a. Ba(OH)2・8H2O与NH4Cl混合搅拌
b. 高温煅烧石灰石
c. 铝与盐酸反应
②某同学进行如下图所示实验,测量稀盐酸与烧碱溶液中和反应的能量变化。实验表明:反应温度升高,由此判断该反应是_______(填“吸热”或“放热”)反应,其离子方程式是_______________。

(2)电能是现代社会应用最广泛的能源之一。
下图所示的原电池装置中,其负极是_____________________,正极上能够观察到的现象是____________________________,正极的电极反应式是_________________________。
原电池工作一段时间后,若消耗锌6.5g,则放出气体__________g。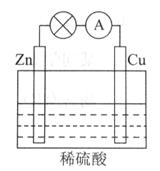
参考答案:(1)①c?(1分)?②放热(1分)? H++OH-=H2O(2分)
(2)Zn(1分)?铜片表面产生无色气泡(1分)? 2H++2e-=H2↑(2分)? 0.2(2分)
本题解析:(1)①金属和酸的反应是放热反应,因此选项c正确,a和b中反应均是吸热反应,答案选c。
②反应温度升高,由此判断该反应是放热反应,反应的离子方程式是H++OH-=H2O。
(2)原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。根据装置图可知,锌的金属性强于铜,所以锌是负极,失去电子,发生氧化反应。铜是正极,溶液中的氢离子在正极得到电子生成氢气,正极上能够观察到的现象是铜片表面产生无色气泡,其中正极电极反应式是2H++2e-=H2↑;电池总反应为:Zn+2H+=Zn2++H2↑,n(H2)=n(Zn)=6.5g÷65g/mol=0.1mol,则m(H2)=0.1mol×2g/mol=0.2g。
本题难度:一般
3、填空题 (4分)指出下列变化能量是怎样转化的:
(1)学校燃烧煤煮饭?,
(2)给手机的电池充电?,
(3)用畜电池点亮灯泡?,
(4)电解水得到O2和H2?。
参考答案:化学能转化为电能;电能转化为化学能;电能转化为光能和热能;电能转化为化学能。
本题解析:考查常见的能量变化。燃烧是化学能转化为电能;电池充电是电能转化为化学能;蓄电池点亮灯泡是电能转化为光能和热能;电解水是电能转化为化学能。
本题难度:简单
4、选择题 相同温度下,甲(恒容)、乙(恒压)、丙(恒容)3个密闭容器中发生可逆反应:
2SO2(g)+O2(g) 2SO3(g)ΔH =" -197" kJ/mol。实验测得起始、平衡时的有关数
2SO3(g)ΔH =" -197" kJ/mol。实验测得起始、平衡时的有关数
据如下表。下列正确的是
容器
| 起始各物质的物质的量/mol
| 达到平衡时体系能量的变化
|
SO2
| O2
| Ar
|
甲
| 2
| 1
| 0
| 放出热量:Q1
|
乙
| 2
| 1
| 0
| 放出热量:Q2
|
丙
| 2
| 1
| 0.5
| 放出热量:Q3
|
?
A.Q1 =Q3<Q2
B.达到平衡时,乙容器中SO2的体积分数最大
C.平衡时,甲、乙、丙3个容器中甲的平衡常数最小
D.若在上述条件下,反应生成1molSO3(s),则反应放热为98.5kJ
参考答案:A
本题解析:A、甲容器与丙容器均为恒温恒容,Ar对平衡无影响,所以甲、丙平衡状态相同,则放出热量相同,Q1 =Q3,随着反应的进行,气体的物质的量逐渐减小,因为乙容器为恒压,所以反应后甲容器压强小于仪器乙,根据化学平衡移动原理,容器乙平衡向右移动程度大,所以Q1 =Q3<Q2,正确;B、根据平衡移动程度,SO2的体积分数甲=丙>乙,错误;C、温度相同,平衡常数相同,错误;D、在上述条件下反应生成1molSO3(s),气体转化为固体放热,所以反应放热应大于98.5kJ,错误。
本题难度:一般
5、选择题 已知N2(g)+3H2(g) 2NH3(g)?△H=― 92.4kJ?mo1―1,下列结论正确的是
2NH3(g)?△H=― 92.4kJ?mo1―1,下列结论正确的是
A.在密闭容器中加入1mol N2和3mol H2充分反应放热92.4kJ
B.N2(g)+3H2(g) 2NH3(l)△H=― QkJ?mo1―1,则Q>92.4
2NH3(l)△H=― QkJ?mo1―1,则Q>92.4
C.增大压强,平衡向右移动,平衡常数增大
D.若一定条件下反应达到平衡,N2的转化率为20%,则H2的转化率一定为60%
参考答案:B
本题解析:A、可逆反应不能进行到底,错误;B、氨气变为液氨放热,正确;C、平衡常数只与温度有关,错误;D、转化率为变化浓度占起始浓度的百分数,N2、H2的变化浓度之比等于1∶3,而起始浓度之比不一定为1∶3,错误。
本题难度:一般