微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列溶液中不能存放在带玻璃塞的试剂瓶中的是
①?氢氟酸 ②? NaCl ③? KNO3 ④? Na2SiO3 ⑤? CuSO4 ⑥? NaOH ⑦? Na2CO3 ⑧? NaHSO4
A.①④⑥⑦
B.①③⑤⑧
C.②③④⑦
D.①④⑥⑧
参考答案:A
本题解析:略
本题难度:一般
2、选择题 在实验室中,下列处理方法将会污染空气的是:
A.将Fe(NO3)2溶液和稀盐酸同时倒入废液缸中的试剂瓶
B.用热纯碱溶液清洗盛过植物油的试管
C.用酒精洗涤做碘升华实验后的烧杯
D.用稀盐酸清洗长期存放过FeCl3溶液的试剂瓶
参考答案:A
本题解析:A处理时会产生污染空气的NO有毒气体。将Fe(NO3)2溶液和稀盐酸同时倒入废液缸中时,溶液中存在Fe2+、H+、NO3―离子的混合物,Fe2+具有还原性,而H+、NO3―具有强氧化性,它们不能共存会发生氧化还原反应。
本题难度:一般
3、选择题 用固体NaOH配制物质的量浓度溶液时,下列操作会导致溶液浓度偏高的是(?)
A.在烧杯中溶解时,有少量液体溅出
B.样品中含有少量Na2O杂质
C.容量瓶使用前未干燥
D.定容时仰视视容量瓶刻度线
参考答案:B
本题解析:具体分析操作对溶质的物质的量及溶液体积的影响,根据c=n/v判断误差。A、在烧杯中溶解时,有少量液体溅出,氢氧化钠的实际质量减少了,溶质的物质的量减少,所以浓度偏低,错误;样品中含有少量NaCl杂质,氢氧化钠的实际质量偏小,溶质的物质的量减少,所以浓度偏低,错误;B、样品中含有少量Na2O杂质,Na2O与水反应生成氢氧化钠,氢氧化钠的实际质量偏大,溶质的物质的量偏大,所以浓度偏高,正确;C、由于最后需要加蒸馏水定容,容量瓶使用前未干燥,对结果无影响,错误;D、定容时仰视容量瓶刻度线,使最后溶液的体积偏大,所以溶液浓度偏低,错误。
本题难度:一般
4、实验题 (13分)某含少量FeCl2杂质的FeCl3样品,现要测定其中铁元素的含量。实验步骤如下:
①准确称量m g样品(2~3g);
②向样品中加入10mL 5mol/L的盐酸,再加入蒸馏水,配制成250mL溶液;
③量取25mL操作②中配得的溶液,加入3 mL溴水,加热使Fe2+完全被氧化;
mL溴水,加热使Fe2+完全被氧化;
④趁热迅速加入浓度为10%的氨水至过量,充分搅拌,使之完全沉淀;
⑤过滤,将沉淀洗涤、灼烧、冷却称量,反复操 作至恒重。
作至恒重。
请根据上面的叙述回答:
(1)若称量前,托盘天平的指针偏向标尺左方;称量读数时,指针刚好在标尺的中间,则所得样品的质量?。
A.比m g多? B.比m g少? C.恰好为m g
(2)溶解样品时要加入盐酸,原因是?。
(3)配250mL溶液时,除需250mL容量瓶、烧杯外,还需用到的玻璃仪器是?、?。
(4)加入溴水时发生反应的离子方程式是?。
(5)若坩埚质量为W1 g,坩埚与灼烧后固体的总质量是W2 g,则样品中铁元素的质量分数是?。
(6)若在配制250mL溶液时,所用的容量瓶没有洗干净。当含有下列物质时,最终会使铁元素的测定含量:①NaCl?;②Fe2(SO4)3?(填“偏高”、“偏低”或“不变”)。
参考答案:(1)B (1分);
(2)抑制Fe2+、Fe3+的水解(2分);
(3)玻璃棒(1分)、胶头滴管(1分);
(4)2Fe2++Br2=2Fe3++2Br-(2分);
(5)7(W2-W1)/m(2分);
(6)①不变(2分)、 ②偏高(2分)。
②偏高(2分)。
本题解析:略
本题难度:简单
5、选择题 下列实验数据记录和实验方法正确的是
A.用天平称取4.0g NaOH固体,用100mL量筒配制1.00 mol・L-1的NaOH溶液
B.使用25mL碱式滴定管(内装有标准NaOH溶液),滴定未知浓度的盐酸,用去NaOH溶液22.32mL
C.使用pH试纸测得新制氯水的pH为4
D.常温常压下,收集500mLNO2气体,则NO2气体的物质的量为(0.5/22.4)mol
参考答案:B
本题解析:A、配制1.00 mol?L-1的NaOH溶液不能在量筒中进行,应该选用100mL容量瓶配制,故A错误;B、滴定管的精确度达到0.01?mL,消耗的氢氧化钠溶液的体积可以为22.32mL,故B正确;C、由于氯水具有漂白性,所以不能用pH试纸来测定pH,故C错误;D、在常温下气体的摩尔体积不是22.4?L?mol-1,所以500?mL?NO2气体的物质的量不是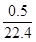 mol,故D错误,故答案选B。
mol,故D错误,故答案选B。
本题难度:一般