微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 (10分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂志,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)判断BaCl2已过量的方法是?。
(2)第④步中,相关的例子方程式? 。
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是?。
(4)为检验精盐纯度,需配制200ml0.1mol/LnaCl(精盐)溶液,下图是该同学转移溶液的示意图,图中的错误是?。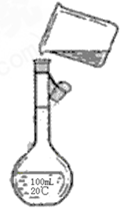
填空题 (10分)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂志,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):

(1)判断BaCl2已过量的方法是?。
(2)第④步中,相关的例子方程式?。
(3)若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是?。
(4)为检验精盐纯度,需配制200ml0.1mol/LnaCl(精盐)溶液,下图是该同学转移溶液的示意图,图中的错误是?。
本题答案:(1)取第②步后的上层清液1~2滴于滴定板上,再滴入1~2滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
(2)Ca2+ + CO32- = CaCO3↓;? Ba2+ + CO32-= BaCO3↓
(3)在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度
(4)①容量瓶不是200ml的,②没有用玻璃棒引流。
本题解析:(1)检验氯化钡过量的方法是继续滴加氯化钡溶液,即取第②步后的上层清液1~2滴于滴定板上,再滴入1~2滴BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
(2)加入的碳酸钠用来除去钙离子以及过量的钡离子,方程式为Ca2+ + CO32- = CaCO3↓;? Ba2+ + CO32-= BaCO3↓。
(3)如果先加盐酸再过滤,则盐酸能溶解沉淀从而影响制得精盐的纯度。
(4)根据装置图可知,主要错误是①容量瓶不是200ml的,②没有用玻璃棒引流。
本题所属考点:【物质的分离、提纯】
本题难易程度:【一般】
All for one, one for all. 人人为我,我为人人.