|
|
|
钡盐生产中排出大量的钡泥[主要含BaCO3、BaSO3、Ba(FeO2)2等],?【物质的分离、提纯】
2017-04-04 10:05:28
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 钡盐生产中排出大量的钡泥[主要含BaCO3、BaSO3、Ba(FeO2)2等],某主要生产BaCO3的化工厂利用钡泥制取Ba(NO3)2晶体及其他副产物,其部分工艺流程如下:
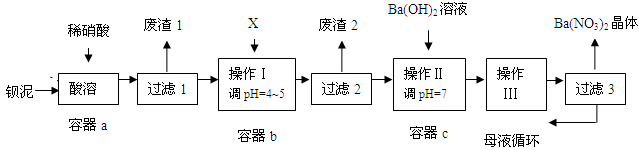
已知:① Fe(OH)3和Fe(OH)2完全沉淀时,溶液的pH分别为3.2和9.7
② Ba(NO3)2在热水中溶解度较大,在冷水中溶解度较小
③ KSP(BaSO4)=1.1×10-10,KSP (BaCO3)=5.1×10-9
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。用离子方程式说明提纯原理:?。
(2)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,化学方程式为:
?。
(3)该厂结合本厂实际,选用的X为?;
A.BaCl2
B.BaCO3
C.Ba(NO3)2
D.Ba(OH)2
| (4)废渣2为?。
(5)操作III为?。
(6)过滤3后的母液应循环到容器?中。(填“a”、“b”或“c”)
(7)称取w克晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量沉淀质量为m克,则该Ba(NO3)2的纯度为??(相对分子质量:Ba(NO3)2为261,BaSO 4为233)。
实验题 钡盐生产中排出大量的钡泥[主要含BaCO3、BaSO3、Ba(FeO2)2等],某主要生产BaCO3的化工厂利用钡泥制取Ba(NO3)2晶体及其他副产物,其部分工艺流程如下:

已知:① Fe(OH)3和Fe(OH)2完全沉淀时,溶液的pH分别为3.2和9.7
② Ba(NO3)2在热水中溶解度较大,在冷水中溶解度较小
③ KSP(BaSO4)=1.1×10-10,KSP (BaCO3)=5.1×10-9
(1)该厂生产的BaCO3因含有少量BaSO4而不纯,提纯的方法是:将产品加入足量的饱和Na2CO3溶液中,充分搅拌,过滤,洗涤。用离子方程式说明提纯原理:?。
(2)上述流程酸溶时,Ba(FeO2)2与HNO3反应生成两种硝酸盐,化学方程式为:
?。
(3)该厂结合本厂实际,选用的X为?;
A.BaCl2
B.BaCO3
C.Ba(NO3)2
D.Ba(OH)2
|
(4)废渣2为
?。
(5)操作III为
?。
(6)过滤3后的母液应循环到容器
?中。(填“a”、“b”或“c”)
(7)称取w克晶体溶于蒸馏水,加入足量的硫酸,充分反应后,过滤、洗涤、干燥,称量沉淀质量为m克,则该Ba(NO3)2的纯度为
??(相对分子质量:Ba(NO3)2为261,BaSO4为233)。
本题答案:(16分)
(1)BaSO4(s)+CO32-(aq)

BaCO3(s) +SO42-(aq)(3分)(不写(s)、(aq)不扣分)
(2)Ba(FeO2)2+8HNO3 = Ba(NO3)2+2Fe(NO3)3+4H2O (2分)
(3)B?(2分)
(4)Fe(OH)3?(2分)
(5)蒸发浓缩、冷却结晶?(2分)
(6)c?(2分)
(7)
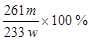
?(3分)
本题解析:(1)根据已知信息可知,5.1×10-9约为1.1×10-10的46倍,虽然Ksp(BaCO3)> Ksp(BaSO4),因此BaSO4可以转化为BaCO3,前提是增大碳酸根离子的浓度,使碳酸根离子与钡离子结合生成碳酸钡沉淀,导致BaSO4 (s)

Ba2++SO42-的平衡向右移动,总反应为BaSO4(s)+CO32-

BaCO3(s)+SO42-;(2)依题意推断,酸溶时Ba(FeO2)2与HNO3反应生成的两种硝酸盐分别是硝酸钡、硝酸铁,不涉及氧化还原反应,利用观察法可以配平该复分解反应方程式,即Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;(3)氯化钡不能与氢离子反应,不能调节pH,且引入氯离子,故A选项错误;碳酸钡与氢离子能反应,生成钡离子、二氧化碳气体和水,既能调节溶液pH在4~5之间,又不引入新的杂质,且该厂实际上生产碳酸钡,故B选项正确;硝酸钡不能与氢离子反应,故C选项错误;氢氧化钡与氢离子能反应,可以调节溶液pH,但是氢氧化钡是强碱,成本高,且容易导致溶液pH升高过快,超出中和I要求的pH范围,故D选项错误;(4)根据已知信息推导,硝酸是氧化性酸,钡泥酸浸之后溶液中无亚铁离子,加入碳酸钡溶液pH在4~5之间,既能减小氢离子溶液,又能促进铁离子完全水解,导致铁离子完全变为氢氧化铁沉淀,则滤渣2的主要成分是氢氧化铁沉淀;(5)操作III的目的是制备硝酸钡晶体,因此操作名称为蒸发浓缩、冷却结晶;(6)过滤3所得母液是硝酸钡的饱和溶液,因为硝酸钡的过饱和溶液析出硝酸钡晶体后,变为硝酸钡的饱和溶液,因此母液中含有的硝酸钡饱和溶液可以循环利用,应使其进行容器c中;(7)由于硝酸是强酸、强氧化性酸,则BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O、3BaSO3+2HNO3=3BaSO4+2NO↑+H2O,Ba(OH)2+2HNO3= Ba(NO3)2+2H2O,则最后的废渣中除原有的难溶性杂质外,还含有BaSO4、Fe(OH)3;(5)由于硫酸钡的式量为233,n=m/M,则硫酸钡的物质的量为m/233 mol;由于反应Ba(NO3)2+H2SO4= BaSO4↓+2HNO3中Ba(NO3)2与BaSO4的系数之比等于物质的量之比,则晶体中Ba(NO3)2的物质的量为m/233 mol;由于硝酸钡的式量为261,m=n?M,则晶体中硝酸钡的质量为261 m/233g;由于晶体的质量为wg,则晶体中硝酸钡的纯度计算表达式为261m/233w×100%。
本题所属考点:【物质的分离、提纯】
本题难易程度:【困难】
Anything for a quiet life. 悠然自在最难求.
 BaCO3(s) +SO42-(aq)(3分)(不写(s)、(aq)不扣分)
BaCO3(s) +SO42-(aq)(3分)(不写(s)、(aq)不扣分)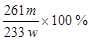 ?(3分)
?(3分) Ba2++SO42-的平衡向右移动,总反应为BaSO4(s)+CO32-
Ba2++SO42-的平衡向右移动,总反应为BaSO4(s)+CO32- BaCO3(s)+SO42-;(2)依题意推断,酸溶时Ba(FeO2)2与HNO3反应生成的两种硝酸盐分别是硝酸钡、硝酸铁,不涉及氧化还原反应,利用观察法可以配平该复分解反应方程式,即Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;(3)氯化钡不能与氢离子反应,不能调节pH,且引入氯离子,故A选项错误;碳酸钡与氢离子能反应,生成钡离子、二氧化碳气体和水,既能调节溶液pH在4~5之间,又不引入新的杂质,且该厂实际上生产碳酸钡,故B选项正确;硝酸钡不能与氢离子反应,故C选项错误;氢氧化钡与氢离子能反应,可以调节溶液pH,但是氢氧化钡是强碱,成本高,且容易导致溶液pH升高过快,超出中和I要求的pH范围,故D选项错误;(4)根据已知信息推导,硝酸是氧化性酸,钡泥酸浸之后溶液中无亚铁离子,加入碳酸钡溶液pH在4~5之间,既能减小氢离子溶液,又能促进铁离子完全水解,导致铁离子完全变为氢氧化铁沉淀,则滤渣2的主要成分是氢氧化铁沉淀;(5)操作III的目的是制备硝酸钡晶体,因此操作名称为蒸发浓缩、冷却结晶;(6)过滤3所得母液是硝酸钡的饱和溶液,因为硝酸钡的过饱和溶液析出硝酸钡晶体后,变为硝酸钡的饱和溶液,因此母液中含有的硝酸钡饱和溶液可以循环利用,应使其进行容器c中;(7)由于硝酸是强酸、强氧化性酸,则BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O、3BaSO3+2HNO3=3BaSO4+2NO↑+H2O,Ba(OH)2+2HNO3= Ba(NO3)2+2H2O,则最后的废渣中除原有的难溶性杂质外,还含有BaSO4、Fe(OH)3;(5)由于硫酸钡的式量为233,n=m/M,则硫酸钡的物质的量为m/233 mol;由于反应Ba(NO3)2+H2SO4= BaSO4↓+2HNO3中Ba(NO3)2与BaSO4的系数之比等于物质的量之比,则晶体中Ba(NO3)2的物质的量为m/233 mol;由于硝酸钡的式量为261,m=n?M,则晶体中硝酸钡的质量为261 m/233g;由于晶体的质量为wg,则晶体中硝酸钡的纯度计算表达式为261m/233w×100%。
BaCO3(s)+SO42-;(2)依题意推断,酸溶时Ba(FeO2)2与HNO3反应生成的两种硝酸盐分别是硝酸钡、硝酸铁,不涉及氧化还原反应,利用观察法可以配平该复分解反应方程式,即Ba(FeO2)2+8HNO3=Ba(NO3)2+2Fe(NO3)3+4H2O;(3)氯化钡不能与氢离子反应,不能调节pH,且引入氯离子,故A选项错误;碳酸钡与氢离子能反应,生成钡离子、二氧化碳气体和水,既能调节溶液pH在4~5之间,又不引入新的杂质,且该厂实际上生产碳酸钡,故B选项正确;硝酸钡不能与氢离子反应,故C选项错误;氢氧化钡与氢离子能反应,可以调节溶液pH,但是氢氧化钡是强碱,成本高,且容易导致溶液pH升高过快,超出中和I要求的pH范围,故D选项错误;(4)根据已知信息推导,硝酸是氧化性酸,钡泥酸浸之后溶液中无亚铁离子,加入碳酸钡溶液pH在4~5之间,既能减小氢离子溶液,又能促进铁离子完全水解,导致铁离子完全变为氢氧化铁沉淀,则滤渣2的主要成分是氢氧化铁沉淀;(5)操作III的目的是制备硝酸钡晶体,因此操作名称为蒸发浓缩、冷却结晶;(6)过滤3所得母液是硝酸钡的饱和溶液,因为硝酸钡的过饱和溶液析出硝酸钡晶体后,变为硝酸钡的饱和溶液,因此母液中含有的硝酸钡饱和溶液可以循环利用,应使其进行容器c中;(7)由于硝酸是强酸、强氧化性酸,则BaCO3+2HNO3=Ba(NO3)2+CO2↑+H2O、3BaSO3+2HNO3=3BaSO4+2NO↑+H2O,Ba(OH)2+2HNO3= Ba(NO3)2+2H2O,则最后的废渣中除原有的难溶性杂质外,还含有BaSO4、Fe(OH)3;(5)由于硫酸钡的式量为233,n=m/M,则硫酸钡的物质的量为m/233 mol;由于反应Ba(NO3)2+H2SO4= BaSO4↓+2HNO3中Ba(NO3)2与BaSO4的系数之比等于物质的量之比,则晶体中Ba(NO3)2的物质的量为m/233 mol;由于硝酸钡的式量为261,m=n?M,则晶体中硝酸钡的质量为261 m/233g;由于晶体的质量为wg,则晶体中硝酸钡的纯度计算表达式为261m/233w×100%。