微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 从回收的含铜电缆废料中提取铜时,假若设计如下两种方案,回答有关问题。
方案甲:

方案乙:

(1)两个方案中,符合当前生产中绿色化学理念的是方案?,理由是?方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾。
(2)方案乙中铜溶解生成蓝色溶液时发生反应的离子方程式为________________ _? ______。
(3)为了提高原料的利用率,最后一步所得浅绿色滤液通过蒸发浓缩、冷却结晶、过滤、洗涤、自然干燥可得到一种结晶水合物的晶体。获得晶体后对其进行检测:
①先取a g的晶体进行脱水实验,获得无水固体为(a―1.26)g
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加10.00mL溶液时,沉淀恰好完全。通过计算测知该晶体的化学式是?。
(4)氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.5% 。工业上用硫酸铜等原料常通过下列反应制备CuCl :
2CuSO4+ Na2SO3 + 2 NaCl + Na2CO3=2 CuCl ↓+ 3 Na2SO4 + CO2↑
测定CuCl质量分数时先准确称取所制备的0.2500g CuCl样品置于一定量的0.5mol・L-1 FeCl3溶液中,待 样品完全溶解后,加水20mL,用0.1000mol・L-1 Ce(SO4)2溶液滴定到终点,消耗24.60mL Ce(SO4)2溶液。有关反应的离子方程式为:Fe 3++CuCl=Fe 2++Cu2++Cl- ,Ce4+ + Fe 2+=Fe 3+ + Ce3+
计算上述样品中CuCl的质量分数为?。
填空题 从回收的含铜电缆废料中提取铜时,假若设计如下两种方案,回答有关问题。
方案甲:

方案乙:

(1)两个方案中,符合当前生产中绿色化学理念的是方案?,理由是?方案第一步“灼烧”会产生污染空气的气体、粉尘、烟雾。
(2)方案乙中铜溶解生成蓝色溶液时发生反应的离子方程式为________________ _? ______。
(3)为了提高原料的利用率,最后一步所得浅绿色滤液通过蒸发浓缩、冷却结晶、过滤、洗涤、自然干燥可得到一种结晶水合物的晶体。获得晶体后对其进行检测:
①先取a g的晶体进行脱水实验,获得无水固体为(a―1.26)g
②将无水固体溶于足量的水配成溶液后滴加1.00mol/L的氯化钡溶液,当滴加10.00mL溶液时,沉淀恰好完全。通过计算测知该晶体的化学式是?。
(4)氯化亚铜(CuCl)是重要的化工原料。国家标准规定合格的CuCl产品的主要质量指标为CuCl的质量分数大于96.5% 。工业上用硫酸铜等原料常通过下列反应制备CuCl :
2CuSO4+ Na2SO3 + 2 NaCl + Na2CO3=2 CuCl ↓+ 3 Na2SO4 + CO2↑
测定CuCl质量分数时先准确称取所制备的0.2500g CuCl样品置于一定量的0.5mol・L-1 FeCl3溶液中,待样品完全溶解后,加水20mL,用0.1000mol・L-1 Ce(SO4)2溶液滴定到终点,消耗24.60mL Ce(SO4)2溶液。有关反应的离子方程式为:Fe 3++CuCl=Fe 2++Cu2++Cl- ,Ce4+ + Fe 2+=Fe 3+ + Ce3+
计算上述样品中CuCl的质量分数为?。
本题答案:(10分)(1)乙 ;甲 (2)2Cu + O2 +4H+ 2Cu2+ + 2H2O (3)FeSO4・7H2O (4)97.9%
2Cu2+ + 2H2O (3)FeSO4・7H2O (4)97.9%
本题解析:(1)方案甲中电缆废料在空气中燃烧时能产生污有毒的气体、粉尘、烟雾而污染空气;而方案乙中不燃烧,所以不能产生有毒气体,因此方案乙符合绿色化学理念。
(2)在加热的条件下铜和氧气反应生成氧化铜,氧化铜溶解在稀硫酸中生成硫酸铜,反应的离子方程式为2Cu + O2 +4H+ 2Cu2+ + 2H2O。
2Cu2+ + 2H2O。
(3)取a g的晶体进行脱水实验,获得无水固体为(a―1.26)g,这说明反应中生成的水的质量是1.26g,物质的量是1.26g÷18g/mol=0.07mol;消耗氯化钡的物质的量是0.01mol,白色沉淀是硫酸钡,则根据原子守恒可知,晶体中SO42-的物质的量是0.01mol,所以晶体中硫酸亚铁和结晶水的个数之比是1:7,因此晶体的化学式为FeSO4・7H2O。
(4)根据离子方程式Fe 3++CuCl=Fe 2++Cu2++Cl- ,Ce4+ + Fe 2+=Fe 3+ + Ce3+可知,
CuCl~Fe 2+~Ce4+
1mol? 1mol
n? 0.0246L×0.1000mol/L
解得n=0.00246mol
所以CuCl的质量=0.00246mol×99.5g/mol=0.24477g
因此 上述样品中CuCl的质量分数为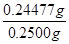 ×100%=97.9%。
×100%=97.9%。
本题所属考点:【物质的分离、提纯】
本题难易程度:【一般】
Life is not all beer and skittles. 人生并非只是啤酒和九柱戏./ 人生并不全是吃喝玩乐.