微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
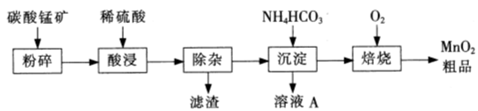
填空题 工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下:
有关氢氧化物开始沉淀和沉淀完全的pH如下表:

请问答下列问题 :?
(1)酸浸前将碳酸锰矿粉碎的作用是??。
(2)酸浸后的溶液中含有Mn2+、 SO42-,另含有少量Fe2+、Fe3+.A13+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其离子反应方程式为 ?。?
②加入CaO将溶液的pH调到5.2~6.0,其主要目的是 ??。
③加入BaS,除去Cu2~、Pb2+后,再加入NaF溶液,除去 ?。
(3)从溶液A中回收的主要物质是?,该物质常用作化肥。?
(4)MnO2粗品中含有少量Mn3O4,可以用稀硫酸处理,将其转化为MnSO4和MnO2,然后再用氧化剂将Mn2+转化为MnO2,制得优质MnO2。写出Mn3O4与稀硫酸反应韵化学方程式:
??。
填空题 工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下:

有关氢氧化物开始沉淀和沉淀完全的pH如下表:

请问答下列问题:?
(1)酸浸前将碳酸锰矿粉碎的作用是??。
(2)酸浸后的溶液中含有Mn2+、 SO42-,另含有少量Fe2+、Fe3+.A13+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其离子反应方程式为 ?。?
②加入CaO将溶液的pH调到5.2~6.0,其主要目的是 ??。
③加入BaS,除去Cu2~、Pb2+后,再加入NaF溶液,除去 ?。
(3)从溶液A中回收的主要物质是?,该物质常用作化肥。?
(4)MnO2粗品中含有少量Mn3O4,可以用稀硫酸处理,将其转化为MnSO4和MnO2,然后再用氧化剂将Mn2+转化为MnO2,制得优质MnO2。写出Mn3O4与稀硫酸反应韵化学方程式:
??。
本题答案:
(1)增大接触面积,加快反应速率(使反应更充分)
(2)@2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O?②除去Fe3~,A13+?③Ca2+
(3)(NH4)2SO4 ?
(4)Mn3O4+2H2SO4=2M nSO4+MnO2+2H2O? (每空2分,本题共12分)
本题解析:化工流程题,(1)将反应物粉碎的作用是增大接触面积,加快反应速率,使反应更充分;(2)pH调到5.2~6.0,其主要目的是除去Fe3~A13+和部分Cu2+;③溶液中除去Fe2+、Fe3+、A13+、Cu2+、Pb2+,但第②加入了Ca2+,再加入NaF溶液,显然是除去Ca2+;(3)流程得到的是碳酸锰沉淀,溶液中主要剩余NH4+和SO42-,故回收的物质是(NH4)2SO4 。
本题所属考点:【物质的分离、提纯】
本题难易程度:【困难】
A man may woo where he will, but he will wed where his hap is. 向谁求爱由自己,与谁结婚靠机遇.