|
|
|
某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜【物质的分离、提纯】
2017-05-10 11:51:00
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿(主要成份:CuO ZnO)的方案,实现废物综合利用,方案如下图所示。
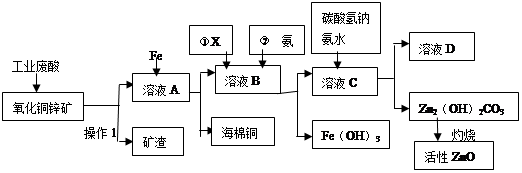
请回答下列问题:
(1)操作1的名称是:?
(2)向溶液A中加入Fe粉发生的主要的反应离子方程式为:?、?。
(3)向溶液B中加入物质X的目的是?,物质X可用下列物质中的?。(填字母)?
A.KMnO4
B.O2
C.H2O2
D.NaOH
| (4)向溶液B中加入氨水的目的是调节溶液的pH,pH应控制在?范围之间。
(5)溶液D中主要溶质的化学式是?。
(6)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(Cu S)??Ksp(ZnS)(选填“>”“<”或“=”)。
填空题 某科研小组设计出利用工业废酸(10%H2SO4)来堆浸某废弃的氧化铜锌矿(主要成份:CuO ZnO)的方案,实现废物综合利用,方案如下图所示。

请回答下列问题:
(1)操作1的名称是:?
(2)向溶液A中加入Fe粉发生的主要的反应离子方程式为:?、?。
(3)向溶液B中加入物质X的目的是?,物质X可用下列物质中的 ?。(填字母)?
A.KMnO4
B.O2
C.H2O2
D.NaOH
|
(4)向溶液B中加入氨水的目的是调节溶液的pH,pH应控制在
?范围之间。
(5)溶液D中主要溶质的化学式是
?。
(6)氧化铜锌矿中含有少量的CuS和ZnS,在H2SO4的作用下ZnS可以溶解而CuS不溶,则相同温度下:Ksp(CuS)
??Ksp(ZnS)(选填“>”“<”或“=”)。
本题答案:(1)过滤(2分)
(2)Fe + 2H+=Fe2+ + H2↑(2分 Fe + Cu2+=Fe2+ + Cu(2分)
(3)将Fe2+氧化成Fe3+,以便除去 (2分)B C (2分)
(4)3.2 <PH< 6.2(2分)?
(5)(NH4)2SO4?(2分)?(6)<?(2分)
本题解析:(1)操作1为固液分离操作,所以名称为过滤。
(2)氧化铜锌矿加入硫酸后,氧化物溶解生成Cu2+、Zn2+,同时为了使矿物充分溶解,加入的酸要过量,所以酸浸后的滤液为酸性溶液,再加入Fe粉,发生反应Fe + 2H+=Fe2+ + H2↑、 Fe + Cu2+=Fe2+ + Cu。
(3)因为得到的B溶液要析出沉淀Fe(OH)3 ,所以须把二价铁氧化为三价铁以便更好的除去,所以除了加碱性氨水溶液外,还应该加入氧化剂,并且不引入杂质,所以可以选择O2、H2O2,故选BC。
(4)加入氨水主要是使Fe3+完全沉淀而不能使Zn2+沉淀,所以应该控制PH范围在3.2 <PH< 6.2之间
(5)由于过程中两次加入氨水,且C溶液中的Zn2+和碳酸根离子生成了沉淀碱式碳酸锌,所以剩余D溶液中含有的大量阳离子为NH4+,大量阴离子为SO42-,所以主要溶质为(NH4)2SO4 。
(6)在H2SO4的作用下ZnS可以溶解而CuS不溶,说明CuS更难溶,所以相同温度下,Ksp(CuS)<Ksp(ZnS)。
本题所属考点:【物质的分离、提纯】
本题难易程度:【一般】
In every beginning think of the end. 凡事一开始就要想到结果.