微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙。以粗CuO为原料制备胆矾的主要流程如下:
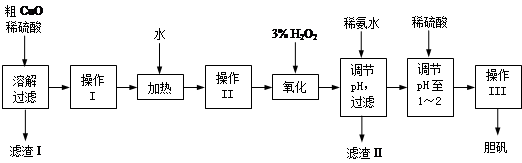
经操作I得到粗胆矾,操作III得到精制胆矾。两步操作相同,具体包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤。
已知: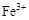 、
、 、
、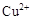 转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
?
| 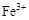
| 
| 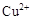
|
开始沉淀时的pH
| 2.7
| 7.6
| 5.2
|
完全沉淀时的pH
| 3.7
| 9.6
| 6.4
|
?
(1)溶解、过滤需要用到玻璃棒,它的作用是 。
(2)写出加入3% H2O2后发生反应的离子方程式 ? 。(原溶液显酸性)。
(3)加稀氨水调节pH应调至范围 。下列物质可用来替代稀氨水的是 。(填字母)
A.NaOH? B.Cu(OH)2? C.CuO? D.NaHCO3
(4)操作III析出胆矾晶体后,溶液中还可能存在的溶质为CuSO4、H2SO4、________________。
(5)某学生用操作III所得胆矾进行“硫酸铜晶体结晶水含量”的测定,数据记录如下表所示:
?
| 第一次实验
| 第二次实验
|
坩埚质量(g)
| 14.520
| 14.670
|
坩埚质量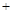 晶体质量(g) 晶体质量(g)
| 17.020
| 18.350
|
第一次加热、冷却、称量(g)
| 16.070
| 16.989
|
第二次加热、冷却、称量(g)
| 16.070
| 16.988
|
两次都无须再做第三次加热、冷却、称量,理由是 ,该生此次实验的相对误差为 %(保留1位小数),产生实验误差的原因可能是
(填字母)。
A.加热前称量时坩埚未完全干燥? B.该胆矾中含有受热不分解的杂质
C.加热后坩埚放在干燥器中冷却? D.玻璃棒上沾有的固体未刮入坩埚
实验题 粗CuO是将工业废铜、废铜合金等高温焙烧而成的,杂质主要是铁的氧化物及泥沙。以粗CuO为原料制备胆矾的主要流程如下:
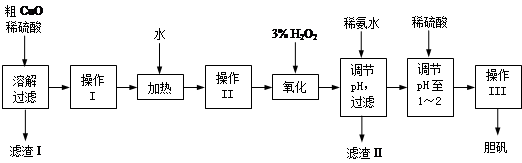
经操作I得到粗胆矾,操作III得到精制胆矾。两步操作相同,具体包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤。
已知: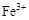 、
、 、
、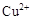 转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
转化为相应氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
?
| 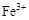
| 
| 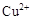
|
开始沉淀时的pH
| 2.7
| 7.6
| 5.2
|
完全沉淀时的pH
| 3.7
| 9.6
| 6.4
|
?
(1)溶解、过滤需要用到玻璃棒,它的作用是 。
(2)写出加入3% H2O2后发生反应的离子方程式 ? 。(原溶液显酸性)。
(3)加稀氨水调节pH应调至范围 。下列物质可用来替代稀氨水的是 。(填字母)
A.NaOH? B.Cu(OH)2? C.CuO? D.NaHCO3
(4)操作III析出胆矾晶体后,溶液中还可能存在的溶质为CuSO4、H2SO4、________________。
(5)某学生用操作III所得胆矾进行“硫酸铜晶体结晶水含量”的测定,数据记录如下表所示:
?
| 第一次实验
| 第二次实验
|
坩埚质量(g)
| 14.520
| 14.670
|
坩埚质量 晶体质量(g) 晶体质量(g)
| 17.020
| 18.350
|
第一次加热、冷却、称量(g)
| 16.070
| 16.989
|
第二次加热、冷却、称量(g)
| 16.070
| 16.988
|
两次都无须再做第三次加热、冷却、称量,理由是 ,该生此次实验的相对误差为 %(保留1位小数),产生实验误差的原因可能是
(填字母)。
A.加热前称量时坩埚未完全干燥? B.该胆矾中含有受热不分解的杂质
C.加热后坩埚放在干燥器中冷却? D.玻璃棒上沾有的固体未刮入坩埚
本题答案:(1)搅拌、引流 (1分)
(2)2Fe2+ +H2O2 +2H+ →2Fe3+ +2H2O? (2分)
(3)3.7~5.2? (1分)?; BC(2分)
(4)(NH4)2SO4或NH4HSO4? (1分,写到一个即给分)
(5)已达恒重? (1分);+4.2%? (2分);AD (2分)
本题解析:(1)溶解、过滤需要用到玻璃棒,它的作用是搅拌、引流。
(2)由于双氧水不稳定,加热易分解生成氧气和水。由于在加入双氧水之前溶液的温度较高,所以加入3% H2O2之前必须进行冷却操作。由于亚铁离子沉淀的pH较大,所以必须将其氧化成铁离子沉淀,因此加入双氧水的目的是氧化亚铁离子,反应的离子方程式为2Fe2+ + H2O2 + 2H+= 2Fe3+ +2H2O。
(3)要得到胆矾,就必须除去溶液中的铁离子,则根据沉淀时的pH值可知,调节溶液pH的目的是使Fe3+完全转变成Fe(OH)3沉淀;铁离子完全沉淀时的pH=3.7,而铜离子开始沉淀时的pH=5.2,所以溶液的pH应调节到3.7~5.2之间。由于在调节pH的同时,不能引入杂质,因此应该选择氧化铜,Cu(OH)2?来调节溶液的pH。
(4)操作III析出胆矾晶体后,溶液中还可能存在的溶质为CuSO4、H2SO4、(NH4)2SO4或NH4HSO4。
(5)根据表中的数据两次实验都已达恒重故没必要再进行第三称量。坩埚质量(g)(14.52+14.67)/2=" 14.595" 实验1:晶体质量:17.02-14.595=2.425水的质量:17.02-16.07=0.95,水的质量分数:0.95/2.425=0.3917,实验2:晶体质量:18.35-14.595=3.755水的质量:18.35-16.99=1.36,水的质量分数:1.36/3.755=0.3622,两次平均水的质量分数:0.3769,五水硫酸铜中水的理论质量数:0.36,相对误差(0.3769-0.360/0.36=0.042。产生实验误差是偏大,即水的质量较多或剩余固体的质量较少,其原因可能是A.加热前称量时坩埚未完全干燥有了多余的水,正确。B.该胆矾中含有受热不分解的杂质会使结果偏低。C.加热后坩埚放在干燥器中冷却,不会带来误差。D.玻璃棒上沾有的固体未刮入坩埚,有一部分固体没有得到称量,相当于剩余的固体质量减小,正确。
本题所属考点:【物质的分离、提纯】
本题难易程度:【一般】
Drawn wells are seldom dry. 水井常用不枯竭.