��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
����� ��(Sr)������������Ԫ�أ��䵥�ʺͻ�����Ļ�ѧ������ơ��������ơ�ʵ�����ú�̼���ȵķ���(��SrCO3 38.40%��SrO12.62%��CaCO3 38.27%��BaCO3 2.54%���������������������8.17%)�Ʊ������ȴ�Ʒ�IJ���ʵ��������£�

��1������Ũ�������������Ϊ65%���ܶ�Ϊ1.4g/cm3��Ҫ����30%ϡ����500mL������Ҫ���ĵ�������?�������ƹ����в�ʹ����ƽ�������Ҫ�����������?������Ҫʹ�õ�������?��
��֪�����ε��ܽ��(g/100 gˮ)���±�
�¶�/������
| 0
| 20
| 30
| 45
| 60
| 80
| 100
|
Sr(NO3)2
| 28.2
| 40.7
| 47
| 47.2
| 48.3
| 49.2
| 50.7
|
Ca(NO3)2��4H2O
| 102
| 129
| 152
| 230
| 300
| 358
| 408
|
?
��2���ɽ�ȡ��õ��Ļ�����Ʊ������ȴ�Ʒ��ʵ�鲽������Ϊ�����ˡ�?��?��ϴ�ӣ����
��֪��������������л��ܼ�A�С�ʽ����Sr(NO3)2�C212��Ba(NO3)2�C261��Ca(NO3)2�C164
��3���Ƶõ������ȴ�Ʒ�к�����Ca(NO3)2��Ba(NO3)2�����ʡ��ⶨ�����ȴ��ȵ�ʵ�����£���ȡ5.39g��������Ʒ�������������л��ܼ�A�������ˡ�ϴ�ӡ������ʣ�����5.26g�����˹������250 mL����Һ��ȡ��25.00 mL������pHΪ7������ָʾ������Ũ��Ϊ0.107mol/L��̼������Һ�ζ����յ㣬����̼������Һ22.98mL��
�ζ����̵ķ�Ӧ��Sr2����CO32���� SrCO3������Ba2����CO32���� BaCO3��
�ٵζ�ѡ�õ�ָʾ��Ϊ? ���ζ��յ�۲쵽������Ϊ?��
�ڸ������ȴ�Ʒ�У������ȵ���������Ϊ?��С���������λ�������ζ�ǰ��Ʒ��Ca(NO3)2û�г��������ⶨ�������ȴ��Ƚ���??(�ƫ�ߡ�����ƫ�͡����䡱)��
����� ��(Sr)������������Ԫ�أ��䵥�ʺͻ�����Ļ�ѧ������ơ��������ơ�ʵ�����ú�̼���ȵķ���(��SrCO3 38.40%��SrO12.62%��CaCO3 38.27%��BaCO3 2.54%���������������������8.17%)�Ʊ������ȴ�Ʒ�IJ���ʵ��������£�

��1������Ũ�������������Ϊ65%���ܶ�Ϊ1.4g/cm3��Ҫ����30%ϡ����500mL������Ҫ���ĵ�������?�������ƹ����в�ʹ����ƽ�������Ҫ�����������?������Ҫʹ�õ�������?��
��֪�� ���ε��ܽ��(g/100 gˮ)���±�
�¶�/������
| 0
| 20
| 30
| 45
| 60
| 80
| 100
|
Sr(NO3)2
| 28.2
| 40.7
| 47
| 47.2
| 48.3
| 49.2
| 50.7
|
Ca(NO3)2��4H2O
| 102
| 129
| 152
| 230
| 300
| 358
| 408
|
?
��2���ɽ�ȡ��õ��Ļ�����Ʊ������ȴ�Ʒ��ʵ�鲽������Ϊ�����ˡ�?��?��ϴ�ӣ����
��֪��������������л��ܼ�A�С�ʽ����Sr(NO3)2�C212��Ba(NO3)2�C261��Ca(NO3)2�C164
��3���Ƶõ������ȴ�Ʒ�к�����Ca(NO3)2��Ba(NO3)2�����ʡ��ⶨ�����ȴ��ȵ�ʵ�����£���ȡ5.39g��������Ʒ�������������л��ܼ�A�������ˡ�ϴ�ӡ������ʣ�����5.26g�����˹������250 mL����Һ��ȡ��25.00 mL������pHΪ7������ָʾ������Ũ��Ϊ0.107mol/L��̼������Һ�ζ����յ㣬����̼������Һ22.98mL��
�ζ����̵ķ�Ӧ��Sr2����CO32���� SrCO3������Ba2����CO32���� BaCO3��
�ٵζ�ѡ�õ�ָʾ��Ϊ?���ζ��յ�۲쵽������Ϊ?��
�ڸ������ȴ�Ʒ�У������ȵ���������Ϊ?��С���������λ�������ζ�ǰ��Ʒ��Ca(NO3)2û�г��������ⶨ�������ȴ��Ƚ���??(�ƫ�ߡ�����ƫ�͡����䡱)��
����𰸣���1��30%ϡ������ܶ� Ũ���������ˮ�����?��Ͳ���ձ���������
��2�������ᾧ?���ȹ���
��3���ٷ�̪?��Һ��Ϊ��ɫ��30s����ɫ?��0.95��212x+261y=5.26? x+y=0.0246��?ƫ��
�����������1����������������ȣ�����Ҫ���ĵ�������30%ϡ������ܶ��������ƹ����в�ʹ����ƽ�������Ҫ�����������Ũ���������ˮ�����������Ҫʹ�õ���������Ͳ���ձ�����������
��2���ɱ��е����ݿ��Կ�����Sr(NO3)2���ܽ�������¶ȵ����߱仯��������Ƶ��ܽ�����¶ȱ仯�ϴ���˿�ͨ���ɽ�ȡ��õ��Ļ�����Ʊ������ȴ�Ʒ��ʵ�鲽������Ϊ�������ᾧ�����ȹ��ˣ�ϴ�ӣ�����õ���
��3���ٷ����ζ����̿�֪����Ʒ��Һ��ɫ������̼���Ƴ�����ȫ���Ե����̪��Һָʾ�յ㣬�������һ����Һ�ʺ�ɫ��������ڲ���ɫ���ʴ�Ϊ����̪����Һ���ޱ�Ϊdz��ɫ30���ڲ���ɫ�������ζ�ǰ��Ʒ��Ca��NO3��2û�г����������ı���Һ̼���ƣ����ݵζ���������c������Һ��=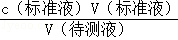 �����ı�Һ�࣬���ⶨ�������ȴ��Ȼ�ƫ�ߣ��ʴ�Ϊ��ƫ�ߡ���֪��������������л��ܼ�A�У�����Ϊ5.39-5.26=0.03g����̼�����Ӧ��ֻ�б����Ӻ������ӣ�Ũ��Ϊ0.107mol/L��̼������Һ22.98mL�����ʵ���Ϊ0.00246mol�������ᱵ�������ȵ����ʵ���Ϊy��x����������ʽΪ212x+261y=5.26? x+y=0.0246�����������ȵ�������������5.39��ȥ����ƺ����ᱵ�������������������Ϊ0.95��
�����ı�Һ�࣬���ⶨ�������ȴ��Ȼ�ƫ�ߣ��ʴ�Ϊ��ƫ�ߡ���֪��������������л��ܼ�A�У�����Ϊ5.39-5.26=0.03g����̼�����Ӧ��ֻ�б����Ӻ������ӣ�Ũ��Ϊ0.107mol/L��̼������Һ22.98mL�����ʵ���Ϊ0.00246mol�������ᱵ�������ȵ����ʵ���Ϊy��x����������ʽΪ212x+261y=5.26? x+y=0.0246�����������ȵ�������������5.39��ȥ����ƺ����ᱵ�������������������Ϊ0.95��
�����������㣺�����ʵķ��롢�ᴿ��
�������׳̶ȣ���һ�㡿
Brevity is the soul of wit. ���Լ�Ϊ��.