��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
ʵ���� �ú���A12O3��SiO2������FeO��xFe2O3�������Ʊ�A12(SO4)3��18H2O�������������£����ֲ����������ԣ�
���������м������ϡH2SO4������:
������Һ�м������KMnO4��Һ��������Һ��pHԼΪ3��
���ȣ�����������ɫ���������ã��ϲ���Һ���Ϻ�ɫ:
��������MnSO4���Ϻ�ɫ��ʧ������;
����Ũ�����ᾧ�����룬�õ���Ʒ��
��1��H2SO4�ܽ�A12O3�����ӷ���ʽ��?
��2��KMnO4����Fe2+�����ӷ���ʽ����������
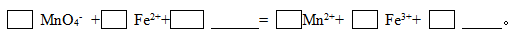
��3����֪�������������������pH
?
| Al(OH)3
| Fe(OH)2
| Fe(OH)3
|
��ʼ����ʱ
| 3.4
| 6.3
| 1.5
|
��ȫ����ʱ
| 4.7
| 8.3
| 2.8
|
ע���������ӵ���ʼŨ��Ϊ0.1mol��L-1
���ݱ������ݽ��Ͳ�����Ŀ��?��
��4����֪��һ������ �£�MnO4-����Mn2+��Ӧ����MnO2,
�����ij����м���ŨHCI�����ȣ���˵�������д���MnO2��������?��
�ڢ��м���MnSO4��Ŀ����?��?
ʵ���� �ú���A12O3��SiO2������FeO��xFe2O3�������Ʊ�A12(SO4)3��18H2O�������������£����ֲ����������ԣ�
���������м������ϡH2SO4������:
������Һ�м������KMnO4��Һ��������Һ��pHԼΪ3��
���ȣ�����������ɫ���������ã��ϲ���Һ���Ϻ�ɫ:
��������MnSO4���Ϻ�ɫ��ʧ������;
����Ũ�����ᾧ�����룬�õ���Ʒ��
��1��H2SO4�ܽ�A12O3�����ӷ���ʽ��?
��2��KMnO4����Fe2+�����ӷ���ʽ����������
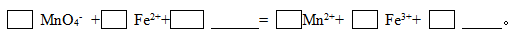
��3����֪�������������������pH
?
| Al(OH)3
| Fe(OH)2
| Fe(OH)3
|
��ʼ����ʱ
| 3.4
| 6.3
| 1.5
|
��ȫ����ʱ
| www.91exAm.org4.7
| 8.3
| 2.8
|
ע���������ӵ���ʼŨ��Ϊ0.1mol��L-1
���ݱ������ݽ��Ͳ�����Ŀ��?��
��4����֪��һ�������£�MnO4-����Mn2+��Ӧ����MnO2,
�����ij����м���ŨHCI�����ȣ���˵�������д���MnO2��������?��
�ڢ��м���MnSO4��Ŀ����?��?
����𰸣���1��A12O3+6H+=2A13++3H2O
��2��MnO4-+5Fe2++8H+=Mn2++5Fe3++4H2O
��3����ȥ��Ԫ�ء�
��4����Ũ������MnO2�������ɻ���ɫ����Cl2�����ж�MnO2�Ƿ���ڡ�
�ڳ�ȥMnO4�C��
�����������1����A12O3+6H+=2A13++3H2O
��2��������������ķ�Ӧ��Fe2+��MnO4-�ķ�Ӧ��Ϊ�������ӷ�Ӧ
��3��pH=3ʱ����������ȫ��������ȥ��Ԫ�ء�
��4������MnO2�����ʣ�Ũ������MnO2�������ɻ���ɫ����Cl2�����ж�MnO2�Ƿ���ڣ�������Ŀ�е���ϢMnO4-����Mn2+��Ӧ����MnO2�����������̵�Ŀ����Ϊ�˳�ȥMnO4�C��
�����������㣺�����ʵķ��롢�ᴿ��
�������׳̶ȣ���һ�㡿
One gives nothing so liberally as advice. ����Ǯ�����⣬˭�˲����⡣