微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
填空题 工业上常以软锰矿、闪锌矿(除主要成分为MnO2、ZnS外还含有少量的FeS、CuS、Al2O3等物质)为原料制取Zn和MnO2。
(1)已知将MnO2、ZnS浸在硫酸溶液中有少量黄色物质析出,写出并配平该化学反应方程式:?。
(2)在酸浸的过程中还会发生以下反应:
a. 3MnO2 +2FeS +6H2SO4=3MnSO4 +Fe2(SO4)3+2S+ 6H2O
b. MnO2+CuS+4H2SO4=MnSO4+CuSO4+S+2H2O?
c. Al2O3+3H2SO4=Al2(SO4)3+3H2O
将酸浸所得的酸性溶液按以下的工业流程进行操作处理得溶液(Ⅳ),电解溶液(Ⅳ)即得MnO2和Zn。

①操作①中加Zn粉后发生反应的离子方程式为:Zn+2H+=Zn2++H2↑、
Zn+Cu2+=Zn2++Cu、?。
②操作②中加入适量X的作用是:?。
③操作③中所加碳酸盐的化学式是:?。
(3)为了从上述流程中产生的Fe(OH)3 、Al(OH)3沉淀混合物中回收Al(OH)3,某化学兴趣小组设计了如下两种方案图。
方案Ⅰ
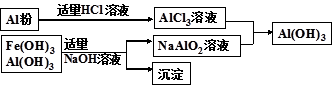
方案Ⅱ
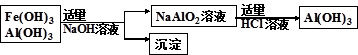
①方案Ⅰ中,AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为:
?。若总共得到n molAl(OH)3,则消耗的NaOH和HCl的理论量分别为:?mol、?mol。
②从消耗酸碱的用量角度考虑,方案? (填“Ⅰ”或“Ⅱ”)所消耗的酸碱少些。
填空题 工业上常以软锰矿、闪锌矿(除主要成分为MnO2、ZnS外还含有少量的FeS、CuS、Al2O3等物质)为原料制取Zn和MnO2。
(1)已知将MnO2、ZnS浸在硫酸溶液中有少量黄色物质析出,写出并配平该化学反应方程式:?。
(2)在酸浸的过程中还会发生以下反应:
a. 3MnO2 +2FeS +6H2SO4=3MnSO4 +Fe2(SO4)3+2S+ 6H2O
b. MnO2+CuS+4H2SO4=MnSO4+CuSO4+S+2H2O?
c. Al2O3+3H2SO4=Al2(SO4)3+3H2O
将酸浸所得的酸性溶液按以下的工业流程进行操作处理得溶液(Ⅳ),电解溶液(Ⅳ)即得MnO2和Zn。

①操作①中加Zn粉后发生反应的离子方程式为:Zn+2H+=Zn2++H2↑、
Zn+Cu2+=Zn2++Cu、?。
②操作②中加入适量X的作用是:?。
③操作③中所加碳酸盐的化学式是:?。
(3)为了从上述流程中产生的Fe(OH)3 、Al(OH)3沉淀混合物中回收Al(OH)3,某化学兴趣小组设计了如下两种方案图。
方案Ⅰ
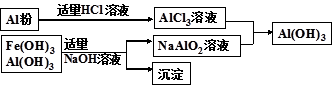
方案Ⅱ
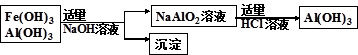
①方案Ⅰ中,AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为:
?。若总共得到n molAl(OH)3,则消耗的NaOH和HCl的理论量分别为:?mol、?mol。
②从消耗酸碱的用量角度考虑,方案? (填“Ⅰ”或“Ⅱ”)所消耗的酸碱少些。
本题答案:(1)MnO2 +ZnS +2H2SO4=MnSO4+ZnSO4+S↓+2H2O(2分)
(2)①Zn+2Fe3+=Zn2++2Fe2+(2分) ②将Fe2+氧化成Fe3+ (2分) ③MnCO3或ZnCO3或MnCO3和ZnCO3(2分)?
(3)① Al3++3AlO2-+6H2O=4Al(OH)3 ↓(2分); 3n/4(1分)、3n/4 (1分)②Ⅰ(1分)
本题解析:(1)由信息将MnO2、ZnS浸在硫酸溶液中有少量黄色物质S析出,故MnO2+ZnS+2H2SO4=MnSO4+ZnSO4+S↓+2H2O。
(2 )从电解溶液(Ⅳ)即得MnO2和Zn可知反应①中的Mn2+置换出来,故①中还有Zn+2Fe3+=Zn2++2Fe2+;②后面得到Fe(OH)3沉淀,说明X是将Fe2+氧化成Fe3+的氧化剂;为了不引进新杂质,调节溶液pH的最好用MnCO3或ZnCO3。
(3)方案I的最终反应是AlCl3+3NaAlO2+6H2O=4Al(OH)3↓+3NaCl,可以得出①Al3++3AlO2-+6H2O=4Al(OH)3↓;因4Al(OH)3↓~3NaCl~3NaOH~3HCl,故总共得到n molAl(OH)3,则消耗的NaOH和HCl的理论量都 3n/4mol。
本题所属考点:【物质的分离、提纯】
本题难易程度:【一般】
A proud man hath many crosses. 骄傲者挫折多。