微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
实验题 实验室模拟回收某废旧含镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等)生产Ni2O3。其工艺流程为:
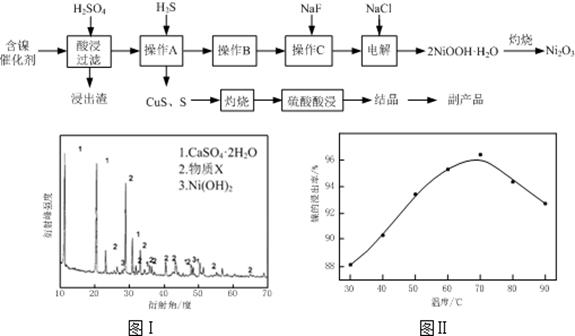
(1)根据图Ⅰ所示的X射线衍射图谱,可知浸出渣含有三种主要成分,其中“物质X”为?。图Ⅱ表示镍的浸出率与温度的关系,当浸出温度高于70℃时,镍的浸出率降低,浸出渣中Ni(OH)2含 量增大,其原因是?。
(2)工艺流程中“副产品”的化学式为?。
(3)已知有关氢氧化物开始沉淀和沉淀完全的pH如下表:
氢氧化物
| Fe(OH)3
| Fe(OH)2
| Ni(OH)2
|
开始沉淀的pH
| 1.5
| 6.5
| 7.7
|
沉淀完全的pH
| 3.7
| 9.7
| 9.2
|
操作B是为了除去滤液中的铁元素,某同学设计了如下实验方案:向操作A所得的滤液中加入NaOH溶液,调节溶液pH为3.7~7.7,静置,过滤。请对该实验方案进行评价
?(若原方案正确,请说明理由;若原方案错误,请加以改正)。
(4)操作C是为了除去溶液中的Ca2+,若控制溶液中F-浓度为3×10- 3mol・L-1,则Ca2+的浓度为?mol・L-1。(常温时CaF2的溶度积常数为2.7×10-11)
(5)电解产生2NiOOH・H2O的原理分两步:
①碱性条件下Cl-在阳极被氧化为ClO-;
②Ni2+被ClO-氧化产生2NiOOH・H2O沉淀。
第②步反应的离子方程式为?。
实验题 实验室模拟回收某废旧含镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等)生产Ni2O3。其工艺流程为:

(1)根据图Ⅰ所示的X射线衍射图谱,可知浸出渣含有三种主要成分,其中“物质X”为?。图Ⅱ表示镍的浸出率与温度的关系,当浸出温度高于70℃时,镍的浸出率降低,浸出渣中Ni(OH)2含 量增大,其原因是?。
(2)工艺流程中“副产品”的化学式为?。
(3)已知有关氢氧化物开始沉淀和沉淀完全的pH如下表:
氢氧化物
| Fe(OH)3
| Fe(OH)2
| Ni(OH)2
|
开始沉淀的pH
| 1.5
| 6.5
| 7.7
|
沉淀完全的pH
| 3.7
| 9.7
| 9.2
|
操作B是为了除去滤液中的铁元素,某同学设计了如下实验方案:向操作A所得的滤液中加入NaOH溶液,调节溶液pH为3.7~7.7,静置,过滤。请对该实验方案进行评价
?(若原方案正确,请说明理由;若原方案错误,请加以改正)。
(4)操作C是为了除去溶液中的Ca2+,若控制溶液中F-浓度为3×10-3mol・L-1,则Ca2+的浓度为?mol・L-1。(常温时CaF2的溶度积常数为2.7×10-11)
(5)电解产生2NiOOH・H2O的原理分两步:
①碱性条件下Cl-在阳极被氧化为ClO-;
②Ni2+被ClO-氧化产生2NiOOH・H2O沉淀。
第②步反应的离子方程式为?。
本题答案:(12分)(1)BaSO4?温度升高,Ni2+的水解程度增大
(2)CuSO4・5H2O
(3)方案错误。在调节pH前,应先在滤液中加入H2O2,使溶液中的Fe2+氧化为Fe3+
(4)3×10-6
(5)ClO-+2Ni2++4OH-=2NiOOH・H2O+Cl-
由题意知,含镍催化剂与硫酸反应后,Ca2+和Ba2+形成沉淀,通入硫化氢气体将Cu2+沉淀,操作B除去Fe3+,操作C除去Ca2+。最后加氯化钠电解硫酸镍溶液得到2NiOOH・H2O。
本题解析:(1)与硫酸反应产生沉淀的除硫酸钙、氢氧化镍外还有就是硫酸钡,所以物质X为BaSO4;由于随着温度升高,Ni2+的水解程度增大,从而导致镍的浸出率降低,浸出渣中Ni(OH)2含量增大;
(2)由于CuS、S灼烧后溶于稀硫酸中生成硫酸铜,所以副产品应该是胆矾,即CuSO4?5H2O,
(3)由于用氢氧化钠溶液调节溶液 的pH值,容易引入杂质,而且pH为3.7~7.7,亚铁离子沉淀不完全,所以方案是错误的;正确的操作应该是在调节pH前,应先在滤液中加入H2O2,使溶液中的Fe2+氧化为Fe3+,
(4)根据常温时CaF2的溶度积常数为2.7×10-11可知,溶液中F-浓度为3×10-3 mol?L-1,则Ca2+的浓度为2.7×10-11/(3×10-3)2= 3×10-6mol?L-1;
(5)Ni2+被ClO-氧化产生2NiOOH?H2O沉淀,其还原产物是氯离子,则根据电子的得失守恒可知,第②步反应的离子方程式为ClO-+2Ni2++4OH-=2NiOOH?H2O+Cl-。
本题所属考点:【物质的分离、提纯】
本题难易程度:【一般】
Bacchus hath drowned more men than Neptune. 在酒里淹死的人比在海里淹死的人多。